Úvod
Divertikulární choroba tlustého střeva představuje nejčastější onemocnění postihující tlusté střevo v západním světě. Prevalence divertikulární choroby se v průběhu minulého století celosvětově zvýšila, pravděpodobně v důsledku změn životního stylu, jako je kouření, nadváha a celkově fyzická nečinnost a strava s nízkým obsahem vlákniny. Prevalence se zvyšuje s věkem a pohybuje se od přibližně 5 % u dospělých mladších 40 let až po 50-70 % u osob starších 80 let; 80 % pacientů, u nichž se divertikulitida objeví, je starších 50 let. Divertikly se mohou vyskytovat v počtu od solitérních až po stovky, obvykle mají průměr 5-10 mm, ale jejich velikost může přesáhnout 2 cm. Divertikulóza se vyskytuje především v esovitém a sestupném tračníku u více než 90 % pacientů, ale může být v různé míře rozšířena i v ostatních částech tlustého střeva.1
Existuje několik termínů souvisejících s divertikulózou, které budou použity v tomto přehledu. Přítomnost divertiklů v tlustém střevě při absenci zjevného zánětu se nazývá divertikulóza nebo nekomplikovaná divertikulární choroba (UDD). Může být symptomatická nebo asymptomatická. Termín „akutní divertikulitida tlustého střeva“ (ACD) se používá pro označení zánětu divertiklů, který může, ale nemusí progredovat do komplikací (komplikovaná ACD). Existuje také chronická divertikulitida, a to z důvodu recidivující divertikulitidy nebo z důvodu rozvoje segmentální kolitidy spojené s divertikly. Souhrnně lze říci, že klinické spektrum divertikulární choroby je široké.
Studie zabývající se přirozeným průběhem onemocnění poukazují na to, že velká většina pacientů s divertikly (přibližně 80 %) zůstane po celý život asymptomatická. Z 15-20 %, u nichž se objeví příznaky, přibližně 1/4 nakonec prodělá epizodu symptomatické bolestivé divertikulární choroby bez zánětu a až 10-25 % prodělá epizodu ACD. Přibližně 1-2 % z nich bude vyžadovat hospitalizaci a 0,5 % operaci. Divertikly jsou zodpovědné za většinu (24-42 %) epizod krvácení z dolní části gastrointestinálního traktu.2-4
Fyziopatologie a rozvoj symptomů
Divertikul tlustého střeva je herniace sliznice a submukózy, která odpovídá slabému místu, kde vasa recti proniká do tunica muscularis. Patogenetické mechanismy divertikulární choroby jsou stále málo známé, nicméně obecně se uznává, že pravděpodobně souvisejí s komplexními interakcemi mezi stravou, mikrobiotou tlustého střeva, genetickými faktory, motilitou a strukturou tlustého střeva, které v průběhu času vedou k jejich vzniku.5 Viz obr. 1. V roce 1971 Painter a Burkitt publikovali svou slavnou hypotézu, že divertikulární choroba je způsobena nadměrným tlakem v tlustém střevě v důsledku segmentace na základě nedostatečného příjmu vlákniny. V reakci na zvýšený intraluminální tlak mohou v místech potenciální slabosti vznikat outpouchery, které se vysouvají.6 Stáza nebo obstrukce v divertiklu s úzkým hrdlem může vést k přemnožení bakterií a lokální tkáňové ischemii vedoucí nakonec k perforaci.7 Od té doby se četné observační studie snažily prokázat možný vliv vlákniny na prevenci divertikulární choroby. Většina z nich dospěla k závěru, že riziko UDD je nepřímo úměrné příjmu vlákniny ve stravě.8-10 Na základě těchto důkazů je ve většině současných doporučení a stanovisek doporučována dieta s vysokým obsahem vlákniny k prevenci divertikulární choroby.11-15 Tato hypotéza je však v poslední době zpochybňována, protože: (1) inverzní souvislost příjmu vlákniny a divertikulózy byla v některých nedávných epidemiologických studiích16,17 zpochybněna a (2) objevují se nové patogenetické hypotézy, jako je neuropatická a myopatická hypotéza.18-22 Mezi další faktory, které byly spojeny se zvýšeným rizikem divertikulární choroby, patří fyzická nečinnost, zácpa, obezita a kouření23.-27
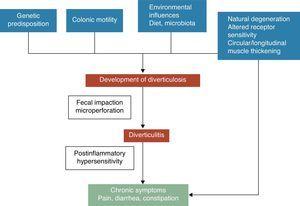
Rozvoj příznaků u divertikulární choroby pravděpodobně souvisí s komplexními interakcemi mezi genetickými vlastnostmi, strukturou tlustého střeva, střevní motilitou zánětem nízkého stupně a pozánětlivou hypersenzitivitou.
Souvislost mezi nekomplikovanou divertikulární chorobou (UDD) a symptomy je nejistá. Existují důkazy, které naznačují, že bolestivá divertikulární choroba může být stavem souvisejícím se zánětem a jeho vlivem na neuromuskulární funkci v tlustém střevě.22-28 Přítomnost chronického střevního zánětu nízkého stupně by vyvolávala senzoricko-motorickou dysfunkci, která by vedla k rozvoji a/nebo přetrvávání symptomů. Změny střevní mikroflóry by mohly být jedním z předpokládaných mechanismů odpovědných za zánět nízkého stupně. Přemnožení bakterií, kterému napomáhá stagnace stolice uvnitř divertiklů, by mohlo přispívat k chronickému zánětu nízkého stupně, který senzibilizuje jak vnitřní primární eferentní, tak vnější primární aferentní neurony. Tyto změny by mohly vést k hypertrofii hladké svaloviny a zvýšené citlivosti na distenzi břicha a nakonec k rozvoji symptomů.3,22 Viz obr. 1.
Jak jsme uvedli výše, většina lidí s divertikulózou tlustého střeva zůstává asymptomatická, ale nakonec se u nich mohou vyvinout komplikace jako ACD nebo krvácení z divertiklů. V tomto článku se zaměříme na ACD. Klinická manifestace této příhody bude záviset na řadě faktorů, včetně velikosti perforace, míry extrakolonické kontaminace a schopnosti organismu tuto kontaminaci zadržet.29,30
Management divertikulární chorobyManagement nekomplikované divertikulární choroby (UDD)
U pacientů s asymptomatickou UDD2 lze doporučit dietu s vysokým obsahem vlákniny vzhledem k jejímu možnému profylaktickému přínosu v prevenci symptomatické UDD a komplikací. Neexistují důkazy, že by u těchto pacientů byly užitečné jiné léky.
O přínosu léčby symptomatické UDD existuje více důkazů. Nejčastějším příznakem je bolest břicha, která se může zhoršovat jídlem a zmírňovat defekací nebo pasáží flatusu. Dalšími příznaky jsou nevolnost, průjem, zácpa a nadýmání. U více než 61 % pacientů se symptomatickou UDD, kteří neužívají žádná léčebná opatření k prevenci recidivy symptomů, se do 1 roku objeví symptomy a přibližně u 4 % se vyvinou komplikace.31
Pro léčbu bylo navrženo pět přípravků (viz obr. 2):

Léčba nekomplikované divertikulární choroby. Mechanismy účinku.
A) Dieta s vysokým obsahem vlákniny nebo objemové látky
Několik randomizovaných kontrolovaných studií (RCT) a dalších intervenčních studií hodnotí účinek vlákniny u symptomatické UDD, avšak s rozporuplnými výsledky.32-37 Každopádně vlákninu v prevenci a léčbě symptomatické UDD i v prevenci ACD doporučuje většina současných doporučení a stanovisek.11-15
B) Antibiotická léčba
Důvody pro použití antibiotik u symptomatické UDD nejsou jednoznačně stanoveny. Nedávné studie naznačují, že změny střevní mikrobioty (přerůstání střevních bakterií) by mohly přispět k rozvoji symptomů v důsledku nadměrné produkce střevního plynu fermentací sacharidů. Aby se předešlo systematickým účinkům, zdají se být nejvhodnějšími antibiotiky špatně vstřebatelná antimikrobiální léčiva, která působí proti střevním patogenům, ale mají minimální riziko systematické toxicity nebo vedlejších účinků. Byl navržen rifaximin.
Rifaximin
Rifaximin je nesystematický analog rifamycinu se širokým spektrem aktivity in vitro. Rifaximin může snižovat metabolickou aktivitu střevní flóry, zvyšovat hmotnost stolice a může také eradikovat bakteriální přerůstání. Toto antibiotikum má vysoký bezpečnostní profil a vysokou snášenlivost.33,38 Plazmatická hladina rifaximinu je minimální, proto nejsou neenterické patogeny vystaveny selekčnímu tlaku a riziko bakteriální rezistence je nízké.39 Tři otevřené a dvě dvojitě zaslepené RCT40-44 zkoumaly účinnost cyklického podávání rifaximinu a vlákniny na snížení symptomů ve srovnání se samotnou vlákninou. Systematický přehled a dvě metaanalýzy analyzovaly tyto studie.44-46 Došly k závěru, že kombinovaná léčba je účinná při dosažení úlevy od příznaků po dobu 1 roku u pacientů s UDD. U 35 % pacientů léčených pouze vlákninou byly příznaky asymptomatické ve srovnání s 64 % ve skupinách s kombinovanou léčbou. Počet potřebných léčebných dávek byl tři pro rifaximin vs. placebo ke zmírnění symptomů a devět k zamezení komplikací. Souhrnně lze říci, že nejlepších výsledků bylo dosaženo při použití kombinace rozpustné vlákniny, jako je glukomannan, a rifaximinu 1 týden každý měsíc.
C) Probiotika
Probiotika jsou živé mikroorganismy, které mohou obnovit komenzální střevní flóru, která mohla být u divertikulární choroby změněna v důsledku stáze a zkrácení tranzitního času tlustým střevem.47 Bohužel je k dispozici jen málo údajů o jejich použití u symptomatické UDD a většina studií je malá a nekontrolovaná. Většina z nich ukazuje zlepšení symptomů.48-50
Probiotika byla studována také v kombinaci s 5-aminosalicylátem (5-ASA). Tursi a jeho kolegové provedli tři RCT srovnávající samotný 5-ASA, samotné probiotikum nebo kombinovanou léčbu.51-53 Jak 5-ASA, tak probiotika se ukázala být účinná v prevenci symptomatické UDD, ale jejich kombinace byla lepší. Nedávná dvojitě vázaná RCT publikovaná stejnou vědeckou skupinou dospěla k závěru, že jak cyklický mesalazin, tak Lactobacillus casei subsp DG, zejména v kombinaci, se zdají být lepší než placebo pro udržení remise symptomatické UDD.54 Souhrnně však lze říci, že špatný design studií a jejich malý rozsah neumožňují definitivní závěry.
D) 5-ASA: mesalazin
Mesalazin má protizánětlivé a antioxidační účinky. V roce 2010 publikovali Gatta a spol.55 systematický přehled Cochrane, který hodnotil úlohu 5-ASA u pacientů s divertikulární chorobou. Autoři dospěli k závěru, že 5-ASA může být v léčbě tohoto onemocnění účinný a že každodenní podávání mesalazinu je pro prevenci recidivy lepší než cyklické podávání. K potvrzení jejich pozorování je třeba provést kvalitní dobře navržené RCT. První placebem kontrolovaná dvojitě zaslepená studie totiž zjistila, že mesalazin je účinný při dosažení úlevy od bolesti u pacientů s akutní UDD.56 Existují také dvě zajímavé RCT, které prokázaly přínos mesalazinu ve srovnání s rifaximinem, pokud jde o prevenci symptomatické recidivy, a podobnou úspěšnost při udržování dlouhodobé remise ve srovnání s probiotikem Lactobacillus casei.53,57
E) Anticholinergní/antiespasmodika
Hermotilita tlustého střeva při divertikulóze naznačuje, že než antispazmodika, jako je dicyklomin a hyoscyamin, by mohla zlepšit příznaky snížením svalové kontrakce. Neexistují však žádné RCT, které by tento přínos potvrdily.
F) Vyhněte se léčbě NSA
Několik kontrolovaných studií prokázalo, že NSA jsou rizikovým faktorem pro rozvoj symptomů, ACD, perforace a krvácení.7,58-60 Uživatelé NSA mají větší riziko rozvoje symptomatické divertikulární choroby než neuživatelé (RR: 1,5, CI 95%: 1,1-2,1).58 A u pacientů s komplikovanou divertikulární chorobou bylo zjištěno větší užívání NSA ve srovnání s kontrolami bez onemocnění. Předpokládalo se, že toto zvýšené riziko je způsobeno poškozením sliznice, které má za následek zhoršenou bariérovou funkci sliznice tlustého střeva umožňující translokaci bakterií, které vyvolávají zánět.
G) Hladiny vitaminu D
Zdá se, že výskyt ACD souvisí s geografickými a sezónními výkyvy. Z tohoto důvodu Maguire et al. provedli dvě zajímavé observační studie, které ukázaly, že nižší hladiny vitaminu D a nízká expozice UV záření (expozice UV záření určuje stav vitaminu D) jsou spojeny s významně vyšším rizikem ACD. Před vydáním doporučení je třeba provést více kvalitních studií.61,62
Léčba akutní divertikulitidy tlustého střeva (ACD)
Ačkoli většina lidí s divertikulózou zůstává asymptomatická, odhaduje se, že přibližně u 10-25 % z nich se vyvine epizoda ACD vlevo.63 Obecně platí, že klinická diagnostika není dostatečně přesná a jsou indikovány radiologické techniky. U pacientů s mírnými příznaky (většina) a bez známek komplikované ACD může být pro diagnózu dostačující kombinace bolesti v levém podbřišku, nepřítomnosti zvracení a C reaktivního proteinu >50mg/l.64,65 Pokud je indikováno zobrazovací vyšetření, může pravděpodobně nejúčinnější přístup představovat podmíněná strategie s ultrazvukem jako technikou první linie a následně počítačovou tomografií (CT), pokud je ultrazvuk neprůkazný nebo pochybný. Počet CT vyšetření může být snížen o 50 %. V roce 1978 Hinchey a kol. navrhli klasifikaci ACD, která byla později modifikována.66,67 Rozlišuje pět stadií ACD; stadium 0, klinicky mírná divertikulitida, stadium I (a: perikolický zánět a b: abces
cm v blízkosti primárního zánětu), stadium II, intraabdominální, pánevní nebo retroperitoneální abces nebo abces vzdálený od primárního zánětu, stadium III, generalizovaná purulentní peritonitida a stadium IV, fekální peritonitida. Viz obr. 3.

Algoritmus pro léčbu akutní divertikulitidy tlustého střeva.
Léčba nekomplikované ACD (Hincheyho stadium 0 nebo Ia)
Většinu nekomplikované ACD lze bezpečně léčit konzervativně s úspěšností mezi 70 a 100 %.14 Ambulantní léčba může umožnit významné úspory nákladů zdravotnických systémů. V případě nekomplikované ACD jsou kritérii pro hospitalizaci významný zánět (včetně přítomnosti horečky nebo peritonitidy), intolerance perorálních tekutin, věk nad 80-85 let, imunosuprese nebo závažné komorbidity. Ve většině případů postačí krátký pobyt v nemocnici. Neexistují žádné důkazy o tom, že by dietní omezení ovlivňovala výsledky léčby, ačkoli většina lékařů obvykle doporučuje čistou tekutou stravu.
Jednou z největších změn v léčbě nekomplikované ACD v poslední době je snižující se používání antibiotik. Nedávný Cochraneův přehled, pouze kvalitativní přístup (bez metaanalýzy), zjistil, že nejlepší dostupné údaje nepodporují jeho rutinní používání.68 Antibiotika neurychlují zotavení ani nezabraňují komplikacím či recidivám. Proto je použití antibiotik v tomto případě sporné. Pravděpodobně by byla vhodná u pacientů s příznaky generalizované infekce, příznaky sepse nebo bakteriémie a u imunokompromitovaných pacientů. Doporučené režimy jsou založeny na klinickém konsenzu. Lze použít různá antibiotika, od ampicilinu po cefalosporiny třetí generace, pokud jsou účinná proti grampozitivním, gramnegativním a anaerobním bakteriím. Kombinace ciprofloxacinu a metronidazolu je pravděpodobně nejčastěji předepisovanou perorální léčbou. Pokud je tato kombinace špatně tolerována, může být dobrou volbou ampicilin-sulfabaktam. Na druhou stranu nedávné údaje ukázaly, že neexistují žádné výhody intravenózní léčby oproti perorálním antibiotikům a intravenózní 4denní léčby oproti 7denní léčbě.69-71 Obvykle je klinické zlepšení pozorováno během 3-4 dnů léčby. Nakonec se doporučuje hospitalizace s intravenózním antibiotikem, pokud pacient není schopen přijímat potravu perorálně, je postižen závažnou komorbiditou nebo se jeho stav nezlepší při ambulantní léčbě.
Léčba komplikované ACD (Hincheyho stadium Ib až IV)ACD Hinchey Ib nebo II: abces
Přibližně u 15 % pacientů s ACD se vyvine absces.67 Neexistují žádné vysoce kvalitní důkazy o nejoptimálnější léčbě ACD s tvorbou abscesu. Hospitalizace je indikována. Velikost je důležitým faktorem určujícím úspěšnost léčby. U menších abscesů (
cm) se doporučuje konzervativní léčba širokospektrými antibiotiky. Ta bude úspěšná až v 70 %.72 Při selhání konzervativní léčby nebo u větších abscesů by měla být provedena perkutánní drenáž. Ta je úspěšná až v 80 %.73 Chirurgický zákrok bude záchrannou léčbou při selhání dříve uvedených léčebných postupů.74 ACD Hinchey III nebo IV: purulentní nebo fekální peritonitida
Peritonitida je nejzávažnější komplikací s mortalitou 14 %. Ačkoli pro to neexistují žádné důkazy, je u těchto pacientů za standardní léčbu považována časná operace. Výběr operace je ovlivněn stavem pacienta, operačním nálezem a zkušenostmi chirurga. U kriticky nemocných pacientů s hemodynamickou nestabilitou se doporučuje Hartmannův postup. U hemodynamicky stabilních pacientů je však třeba za vhodnější volbu považovat primární anastomózu s proximální fekální diverzí nebo bez ní.14,74
Tradičně se v mezinárodních doporučeních doporučuje po epizodě ACD použít endoskopii k vyloučení kolorektálního karcinomu. Toto doporučení vychází pouze z názorů odborníků. Nedávné retrospektivní studie a systematický přehled75-80 ukazují, že míra výskytu karcinomu u těchto pacientů je poměrně nízká. Na základě těchto nejnovějších důkazů může být nejúčinnější strategií odeslat ke kolonoskopii pouze pacienty s přetrvávajícími symptomy nebo pacienty s podezřelým CT nálezem. K jednoznačnému doporučení je však třeba provést další studie.
Léčba po epizodě ACDPrevence opakovaných ACD
Po jedné epizodě ACD se přibližně u třetiny pacientů objeví druhá ACD a po druhé epizodě se u další třetiny pacientů objeví další záchvat.73,74 Důkazů, které by definovaly optimální léčbu po epizodě ACD s cílem zabránit nové epizodě, je však málo.
A) Dieta s vysokým obsahem vlákniny
Po odeznění akutní epizody se běžně doporučuje dieta s vysokým obsahem vlákniny s cílem snížit počet recidiv. RCT týkající se diety s vysokým obsahem vlákniny u pacientů s ACD však měly rozporuplné výsledky. Nedávno publikovaný systematický přehled diet s vysokým obsahem vlákniny nemohl zahrnout žádnou studii, která by zkoumala roli vlákniny v prevenci recidiv ACD.26,81 Klasicky se vyhýbáme některým potravinám (semínka, popcorn a ořechy), protože teoreticky vstupují do divertiklu, blokují ho nebo dráždí. Strate et al. však ve své rozsáhlé prospektivní studii nezjistili žádnou souvislost se zvýšeným rizikem ACD. Proto by se vyloučení těchto potravin z jídelníčku nemělo doporučovat.82 Také snížení hmotnosti a zanechání kouření může mít příznivý vliv na prevenci ACD.9,83
B) Antibiotika
Existují tři nedávné systematické přehledy, které hodnotily úlohu cyklického rifaximinu v prevenci recidivy ACD, ale neprokázaly jasný přínos.46,84,85 Z patofyziologického hlediska by pravděpodobným vysvětlením neúčinnosti rifaximinu v prevenci recidivy mohlo být to, že cyklická léčba nemusí kontrolovat populaci bakterií tlustého střeva během celého měsíce, protože populace bakterií tlustého střeva se obnoví během 7-14 dnů po ukončení podávání rifaximinu. Nedávná španělská otevřená RCT však ukázala, že cyklický rifaximin může zlepšit symptomy a udržet období remise po ACD.86 K recidivám došlo u 10,4 % pacientů, kterým byl podáván rifaximin plus vláknina, oproti 19,3 % pacientů, kterým byla podávána pouze vláknina. Navíc pacienti, u kterých byla poprvé diagnostikována od ≥ 1 roku, měli vyšší riziko exacerbace (OR 3,34, 95% CI: 0,01-12,18). Je však třeba provést další studie, protože v současné době nelze vydat žádné doporučení. Neexistují žádné důkazy, které by podporovaly použití jiných antibiotik v této situaci.
C) Probiotika
Některé otevřené studie zkoumaly roli probiotik v prevenci recidivy ACD. Giaccari a kol. před více než 20 lety hodnotili roli Lactobacillus sp. po rifaximinu u 79 pacientů se stenózou tlustého střeva po divertikulitidě. Po dobu 12 měsíců zůstalo 88 % pacientů asymptomatických.87 Tato observační studie byla první, která naznačila možnou roli probiotik v této situaci. Novější studie hodnotila kombinovanou léčbu; balsalazid a VSL#3 (směs osmi druhů probiotik). Po 12 měsících bylo 73 % subjektů na kombinované léčbě asymptomatických ve srovnání s 53 % na monoterapii probiotiky (p>0,05).52 Souhrnně lze říci, že probiotika se zdají být účinná v prevenci recidivy ACD, ale chybí dobře navržené studie.
D) 5-ASA
Několik dvojitě zaslepených a otevřených RCT hodnotilo roli mesalazinu v prevenci recidivy ACD. Bohužel většina z nich nezjistila přínos mesalazinu oproti placebu v prevenci rekurence.88-90 Raskin a kol. nedávno publikovali dvě zajímavé a identické dvojitě slepé RCT fáze 3 s placebem (PREVENT1 a PREVENT2), které rovněž ukazují, že mesalazin není v prevenci rekurence ACD lepší než placebo.91 Také kombinovaná léčba, 5-ASA plus rifaximin, byla hodnocena v několika studiích. Trivedi a Das přezkoumali údaje z pěti RCT a jedné otevřené studie, které dohromady zahrnovaly více než 600 pacientů, a dospěli k závěru, že kombinace se zdá být v prevenci rekurentní ACD lepší než samotný rifaximin.92
E) Chirurgický zákrok
Ještě před několika lety se doporučoval elektivní chirurgický zákrok po dvou atakách nekomplikované ACD nebo jedné atace komplikované ACD, aby se snížila morbidita a mortalita rekurencí. Elektivní operace však s sebou nese i zvýšené riziko morbidity a mortality.93 Z tohoto důvodu je důležité zvážit morbiditu a mortalitu způsobenou operací ve srovnání s rizikem komplikovaných recidiv a závažností příznaků.94
Nejnovější údaje ukazují, že přirozený průběh ACD je mnohem benignější, než se myslelo v minulosti.95
Přirozený průběh ACD je mnohem benignější, než se myslelo v minulosti.96 Dlouhodobé riziko recidivy je nižší, než se dříve předpokládalo, a dlouhodobé riziko následné urgentní operace (3-7 %), úmrtí (95 ukázalo, že 16 % případů s první ACD bylo urgentně operováno ve srovnání s pouhými 6 % u recidivujících případů a že 30denní mortalita u první epizody byla také vyšší ve srovnání s recidivami (3 % vs. 0 %). Ve skutečnosti u většiny pacientů, kteří se dostaví s komplikovanou ACD, chybí anamnéza onemocnění.96 Rovněž se předpokládá, že recidivující ACD může chránit před perforací, pravděpodobně v důsledku tvorby adhezí způsobených zánětem.95 Politika elektivní operace po ACD tedy nesnižuje pravděpodobnost další operace (až 3 %) a nechrání plně před recidivou. Na druhou stranu zlepšení diagnostiky a léčebných postupů snížilo morbiditu komplikovaných ACD. Vzhledem k těmto novým údajům Americká společnost chirurgů tlustého střeva a konečníku ve svých nejnovějších pokynech doporučuje, aby se elektivní resekce sigmatu po vyléčení ACD prováděla případ od případu14 , a domnívá se, že počet předchozích epizod není dobrým ukazatelem pro výběr kandidátů k elektivní operaci. Lékaři by měli zvážit zdravotní stav a věk pacienta, četnost a závažnost záchvatu (záchvatů) a přítomnost přetrvávajících příznaků po akutní epizodě.14
Je velmi obtížné předvídat, které případy ACD budou recidivovat. Závažnost první epizody ACD odstupňovaná podle CT se zdá být prediktorem nepříznivého přirozeného průběhu. Levostranná ACD, >5 cm postiženého tlustého střeva a retroperitoneální absces jsou prediktory recidivy a je třeba je brát v úvahu.97 Neexistuje shoda ohledně toho, zda by měl být mladý věk (82 Podle současných poznatků by věk neměl být považován za indikaci k elektivní operaci, protože se nezdá, že by souvisel se závažným průběhem onemocnění po medikamentózně léčené ACD. Avšak s ohledem na to, že u mladších pacientů je zvýšený výskyt ACD, jsou k objasnění této specifické otázky nutné další studie.
Speciálními případy jsou imunokompromitovaní jedinci. Kohortové studie naznačují, že tito pacienti mají vysoké riziko komplikované recidivy ACD (5krát vyšší riziko perforace) a vysoké riziko urgentní operace.98 Nižší práh pro elektivní operaci jim proto může prospět.14 Biondo a kol. však ve své nedávné studii ukazují, že imunokompromitovaní pacienti měli významně vyšší mortalitu, ale pouze v první epizodě. Proto je zde přítomna kontroverze.99
Léčba následkůA) Fistula
Fistula vzniká, když divertikulární flegmóna nebo absces praskne do sousedního orgánu. Píštěl se objeví u méně než 5 % pacientů s ACD. Nejčastější jsou kolovezikální a kolovaginální píštěle. Pravděpodobně u většiny pacientů by bylo možné provést jednostupňovou operační resekci s uzavřením píštěle a primární anastomózou. Jiné píštěle jako koloenterická nebo koluterinní jsou vzácné.100,101
B) Obstrukce
Rekurentní epizody ACD, které mohou být subklinické, mohou způsobit chronické zúžení tlustého střeva bez probíhajícího zánětu. Může dojít k vysokému stupni nebo úplné obstrukci. Z léčby obstrukce je nutné nejprve vyloučit maligní etiologii. Pokud je neoplazie dostatečně vyloučena a není přítomna ACD, může být terapeutickou možností endoskopická dilatace nebo dočasná dekomprese pomocí kovového stentu.102 Později lze realizovat následnou jednostupňovou resekci bez diverze.103
Léčba segmentální kolitidy spojené s divertikulózou
Je definována jako chronický zánět interdivertikulární sliznice některého segmentu tlustého střeva zahrnuje. Konečník a pravé tlusté střevo jsou ušetřeny. Stala se výraznou klinickou a patologickou poruchou a často se projevuje krvavou stolicí. Patogeneze není známa. Spektrum histologických změn sahá od mírného nespecifického zánětu až po změny podobné zánětlivému onemocnění střev. Z tohoto důvodu je diferenciální diagnostika často obtížná. Většina pacientů se během několika týdnů nebo měsíců zcela zotaví. Někteří z nich jsou zpočátku léčeni perorálními 5-ASA, ale pravděpodobně tyto léky nejsou nutné, protože většina případů spontánně odezněla.103
Závěry
U symptomatické UDD je cílem léčby zabránit komplikacím a zmírnit příznaky. Podle současných poznatků se jako nejúčinnější terapie jeví vláknina plus cyklický rifaximin nebo mesalazin plus probiotika. U UDD se zdá, že antibiotika zůstávají základem léčby a ambulantní léčba je považována za optimální přístup u naprosté většiny pacientů s nekomplikovanou UDD. U komplikovaných ACD je však nutná hospitalizace a intravenózní podávání antibiotik. V současné době se mění úloha urgentní chirurgie. Většinu abscesů spojených s divertikulitidou lze léčit intravenózními antibiotiky a/nebo perkutánní drenáží a urgentní operace bude považována za standardní léčbu pouze u pacientů s peritonitidou. Konečně, elektivní operace po zotavení z ACD by měla být prováděna případ od případu.
Příspěvky autorů
Gargallo CJ, Sopeña F a Lanas A se rovným dílem podíleli na návrhu, redakční přípravě a recenzním řízení tohoto článku.
Střet zájmů
Dr. Carla J. Gargallo a Dr. Federico Sopeña neuvádějí střet zájmů. Dr. Angel Lanas byl poradcem společnosti AlfaWasserman.
Doktor Angel Lanas byl poradcem společnosti AlfaWasserman.
