![]()
Osoby používající asistivní technologie nemusí mít plný přístup k informacím v tomto souboru. V případě potřeby pomoci zašlete e-mail na adresu: [email protected]. Do předmětu e-mailu napište 508 Ubytování a název zprávy.
![]() PDF
PDF
Radní výbor pro očkovací postupy (ACIP) každoročně přezkoumává doporučený očkovací kalendář pro dospělé, aby zajistil, že tento kalendář odráží aktuální doporučení pro používání licencovaných vakcín. V červnu 2005 schválil ACIP očkovací kalendář dospělých na období říjen 2005-září 2006. Tento plán schválila také Americká akademie rodinných lékařů a Americká vysoká škola porodníků a gynekologů.
Změny v očkovacím plánu na období říjen 2005-září 2006
Očkovací plán na období 2005-2006 se od předchozího plánu liší takto:
- Očkovací látky uvedené v očkovacím plánu podle věku (obrázek 1) jsou zobrazeny tak, aby bylo možné odlišit očkovací látky doporučené pro běžné použití od očkovacích látek doporučených pro dospělé s určitými rizikovými ukazateli (podobně jako v očkovacím plánu pro děti). To je znázorněno jak barevným schématem, tak přerušovanou čarou.
- Žluté pruhy („Pro všechny osoby v této skupině“) a zelené pruhy („Pro osoby, které nemají doklad o očkování nebo doklad o onemocnění“) z předchozího schématu byly sloučeny do jednoho žlutého pruhu, který nyní zní: „Pro všechny osoby v této kategorii, které splňují věkové požadavky a nemají doklad o imunitě (např, nemají doklad o očkování nebo nemají doklad o předchozí infekci).“
- Fialový pruh byl změněn z „Pro osoby v riziku (např. se zdravotními/expozičními indikacemi)“ na „Doporučeno, pokud je přítomen nějaký další rizikový faktor (např. na základě zdravotních, profesních, životních nebo jiných indikací)“. Do sloupců pro věkové skupiny 50–64 let a >65 let byl přidán fialový pruh pro vakcínu proti spalničkám, příušnicím a zarděnkám (MMR).
- Sloupec „Diabetes, srdeční onemocnění, chronické plicní onemocnění nebo chronické onemocnění jater včetně chronického alkoholismu“ byl přesunut se sloupcem „Vrozená imunodeficience, leukémie, lymfom, generalizovaná malignita, léčba alkylačními látkami, antimetabolity, únik mozkomíšního moku, ozařování nebo velké množství kortikosteroidů“ na schématu zdravotních/jiných indikací (obrázek 2), takže kontraindikace pro vakcíny proti MMR a varicelle jsou nyní vedle sebe.
- Řádek pro vakcínu proti planým neštovicím byl na obou obrázcích posunut nahoru (tj, hned za vakcínu MMR), protože tato vakcína je nyní všeobecně doporučována pro určité věkové skupiny.
- Vakcína proti meningokokům byla přidána do schématu lékařských/jiných indikací (obrázek 2). Poznámka pod čarou byla upravena tak, aby zahrnovala nedávno zveřejněná doporučení ACIP pro tuto vakcínu (1).
- Poznámka k tetanu a záškrtu (č. 1) byla přeformulována.
- Poznámka k varicelle (č. 3) byla přeformulována v souladu s doporučeními ACIP přijatými v červnu 2005.
- Poznámka pod čarou k chřipce (č. 4) byla přepracována a doplněna o nejnovější vysoce rizikový stav: neuromuskulární stavy, které ohrožují respirační funkce (2).
- Byla přidána desátá poznámka pod čarou týkající se očkování proti Haemophilus influenzae typu b u vysoce rizikových skupin obyvatelstva (tj, osoby s asplenií, leukémií a infekcí virem lidského imunodeficitu).
Očkovací plán pro dospělé je k dispozici v angličtině a španělštině na adrese http://www.cdc.gov/nip/recs/adult-schedule.htm. Obecné informace o očkování dospělých, včetně doporučení týkajících se očkování osob s HIV a jinými imunosupresivními stavy, jsou k dispozici na státních a místních zdravotnických odděleních a v Národním imunizačním programu na adrese http://www.cdc.gov/nip. Informační prohlášení o očkování jsou k dispozici na adrese http://www.cdc.gov/nip/publications/vis. Prohlášení ACIP ke každé doporučené vakcíně si můžete prohlédnout, stáhnout a vytisknout z webových stránek Národního imunizačního programu na adrese http://www.cdc.gov/nip/publications/acip-list.htm. Pokyny pro hlášení nežádoucích příhod do systému hlášení nežádoucích příhod vakcín jsou k dispozici na adrese http://www.vaers.hhs.gov nebo na telefonním čísle 800-822-7967.
- CDC. Prevence a kontrola meningokokových onemocnění: doporučení Poradního výboru pro očkovací postupy (ACIP). MMWR 2005;54(No. RR-7).
- CDC. Prevence a kontrola chřipky: doporučení Poradního výboru pro imunizační praxi (ACIP). MMWR 2005;54(No. RR-8).
Obrázek 1
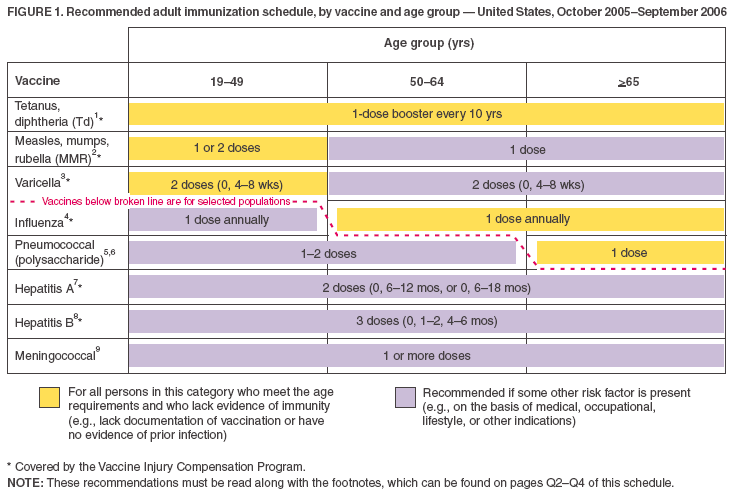
Zpět na začátek.
Obrázek 2

Zpět na začátek.
Schváleno Poradním výborem pro očkovací praxi, Americkou akademií porodníků a gynekologů a Americkou akademií rodinných lékařů
1. Očkování proti tetanu a záškrtu (Td). Dospělí s nejistou historií kompletní primární očkovací série s vakcínami obsahujícími difterický a tetanový toxoid by měli podstoupit primární sérii s použitím kombinovaného Td toxoidu. Primární série pro dospělé představuje 3 dávky; první 2 dávky podávejte s odstupem nejméně 4 týdnů a třetí dávku 6-12 měsíců po druhé dávce. Podejte 1 dávku, pokud osoba obdržela primární sérii a pokud poslední očkování proběhlo před >10 lety. Doporučení pro podávání Td jako profylaxe při léčbě ran konzultujte s prohlášením ACIP (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). Pracovní skupina American College of Physicians pro imunizaci dospělých podporuje druhou možnost použití Td u dospělých: jednorázové přeočkování Td ve věku 50 let u osob, které absolvovaly celou pediatrickou sérii, včetně přeočkování dospívajících/mladých dospělých. Pro dospělé je k dispozici nově licencovaná vakcína proti tetanu, difterii a celulárnímu kašli. Doporučení ACIP pro její použití budou zveřejněna.
2. Očkování proti spalničkám, příušnicím a zarděnkám (MMR). Složka proti spalničkám: dospělé narozené před rokem 1957 lze považovat za imunní vůči spalničkám. Dospělí narození v průběhu roku 1957 nebo po něm by měli obdržet >1 dávku MMR, pokud nemají zdravotní kontraindikaci, dokumentaci >1 dávky, anamnézu spalniček na základě diagnózy poskytovatele zdravotní péče nebo laboratorní důkaz imunity. Druhá dávka MMR se doporučuje dospělým, kteří 1) byli nedávno vystaveni spalničkám nebo v prostředí epidemie; 2) byli dříve očkováni usmrcenou vakcínou proti spalničkám; 3) byli očkováni neznámým typem vakcíny proti spalničkám v letech 1963-1967; 4) jsou studenty postsekundárních vzdělávacích institucí; 5) pracují ve zdravotnickém zařízení nebo 6) plánují cestovat do zahraničí. Odmítněte očkování vakcínou MMR nebo jinými vakcínami obsahujícími spalničky u osob infikovaných HIV s těžkou imunosupresí. Složka proti příušnicím: 1 dávka vakcíny MMR by měla být dostatečnou ochranou pro osoby narozené v roce 1957 nebo později, které nemají příušnice v anamnéze na základě diagnózy od poskytovatele zdravotní péče nebo nemají laboratorně prokázanou imunitu. Složka proti zarděnkám: Podejte 1 dávku vakcíny MMR ženám, jejichž anamnéza očkování proti zarděnkám je nespolehlivá nebo u nichž chybí laboratorní důkaz imunity. U žen ve fertilním věku, bez ohledu na rok narození, rutinně stanovte imunitu proti zarděnkám a poskytněte ženám poradenství ohledně vrozeného syndromu zarděnek. Neočkujte ženy, které jsou těhotné nebo by mohly otěhotnět během 4 týdnů po podání vakcíny. Ženy, které nemají prokázanou imunitu, by měly být očkovány vakcínou MMR po ukončení nebo přerušení těhotenství a před propuštěním ze zdravotnického zařízení.
3. Očkování proti planým neštovicím. Očkování proti varicelle se doporučuje všem dospělým bez průkazu imunity proti varicelle. Zvláštní pozornost je třeba věnovat osobám, které 1) jsou v úzkém kontaktu s osobami s vysokým rizikem závažného onemocnění (zdravotničtí pracovníci a rodinné kontakty imunokompromitovaných osob) nebo 2) jsou vystaveny vysokému riziku expozice nebo přenosu (např. učitelé malých dětí; zaměstnanci zařízení péče o děti; obyvatelé a zaměstnanci ústavních zařízení včetně nápravných zařízení; vysokoškolští studenti; vojenský personál; dospívající a dospělí žijící v domácnostech s dětmi; netěhotné ženy v plodném věku a zahraniční cestovatelé). Důkazem imunity proti varicelle u dospělých je některý z následujících údajů: 1) doložené očkování proti varicelle odpovídající věku (tj. obdržení 1 dávky před 13. rokem věku nebo obdržení 2 dávek po 13. roce věku); 2) narození v USA před rokem 1966 nebo anamnéza onemocnění varicellou před rokem 1966 u osob, které nejsou občany USA.narozených v USA; 3) anamnéza varicelly na základě diagnózy poskytovatele zdravotní péče nebo hlášení rodičů či sebe sama o typickém onemocnění varicelou u osob narozených v letech 1966-1997 (u pacienta uvádějícího v anamnéze atypický, mírný případ by poskytovatelé zdravotní péče měli hledat buď epidemiologickou souvislost s typickým případem varicelly, nebo důkaz laboratorního potvrzení, pokud bylo provedeno v době akutního onemocnění); 4) anamnéza herpes zoster na základě diagnózy poskytovatele zdravotní péče; nebo 5) laboratorní důkaz imunity. Neočkujte ženy, které jsou těhotné nebo které by mohly otěhotnět během 4 týdnů po podání vakcíny. Vyhodnoťte těhotné ženy z hlediska průkazu imunity proti varicelle. Ženy, které nemají důkaz imunity, by měly dostat 1. dávku vakcíny proti varicelle po ukončení nebo přerušení těhotenství a před propuštěním ze zdravotnického zařízení. Dávka 2 by měla být podána 4-8 týdnů po dávce 1.
4. Očkování proti chřipce. Zdravotní indikace: chronické poruchy kardiovaskulárního nebo plicního systému, včetně astmatu; chronická metabolická onemocnění, včetně diabetes mellitus, renální dysfunkce, hemoglobinopatie nebo imunosuprese (včetně imunosuprese způsobené léky nebo HIV); jakýkoli stav (např, kognitivní dysfunkce, poranění míchy, záchvatové onemocnění nebo jiná neuromuskulární porucha), který zhoršuje respirační funkce nebo manipulaci s dýchacími sekrety nebo který může zvýšit riziko aspirace; a těhotenství během chřipkové sezóny. Neexistují žádné údaje o riziku závažného nebo komplikovaného chřipkového onemocnění u osob s asplenií; chřipka je však rizikovým faktorem pro sekundární bakteriální infekce, které mohou u osob s asplenií způsobit závažné onemocnění. Profesní indikace: zdravotničtí pracovníci a zaměstnanci zařízení dlouhodobé péče a domovů pro seniory. Další indikace: obyvatelé domovů pro seniory a jiných zařízení dlouhodobé péče a domovů s pečovatelskou službou; osoby, které mohou přenášet chřipku na osoby s vysokým rizikem (tj. kontaktní osoby v domácnosti a osoby pečující o děti ve věku 0-23 měsíců nebo osoby všech věkových kategorií s vysoce rizikovými stavy), a všichni, kteří si přejí být očkováni. Zdravým, netěhotným osobám ve věku 5-49 let bez vysoce rizikových stavů, které nejsou kontaktními osobami těžce imunokompromitovaných osob na odděleních speciální péče, může být místo inaktivované vakcíny podána intranazálně aplikovaná vakcína proti chřipce (FluMist®).
5. Očkování proti pneumokokovým polysacharidům. Lékařské indikace: chronické poruchy plicního systému (s výjimkou astmatu); kardiovaskulární onemocnění; diabetes mellitus; chronické onemocnění jater, včetně onemocnění jater v důsledku zneužívání alkoholu (např. cirhóza); chronické selhání ledvin nebo nefrotický syndrom; funkční nebo anatomická asplenie (např, srpkovitá anémie nebo splenektomie ); imunosupresivní stavy (např. vrozená imunodeficience, infekce HIV , leukémie, lymfom, mnohočetný myelom, Hodgkinova choroba, generalizovaná malignita nebo transplantace orgánů či kostní dřeně); chemoterapie alkylačními látkami, antimetabolity nebo dlouhodobými systémovými kortikosteroidy a kochleární implantáty. Další indikace:
6: Domorodci z Aljašky a někteří američtí indiáni; obyvatelé domovů důchodců a jiných zařízení dlouhodobé péče. Revakcinace pneumokokovou polysacharidovou vakcínou. Jednorázové přeočkování po 5 letech u osob s chronickým selháním ledvin nebo nefritickým syndromem; funkční nebo anatomickou asplenií (např. srpkovitá anémie nebo splenektomie); imunosupresivními stavy (např, vrozená imunodeficience, infekce HIV, leukémie, lymfom, mnohočetný myelom, Hodgkinova choroba, generalizovaná malignita nebo transplantace orgánů či kostní dřeně); nebo chemoterapie alkylačními látkami, antimetabolity nebo dlouhodobými systémovými kortikosteroidy. U osob ve věku >65 let jednorázové přeočkování, pokud byly očkovány před >5 lety a v době primárního očkování byly ve věku <65 let.
7. Očkování proti hepatitidě A. Lékařské indikace: osoby s poruchami srážlivosti krve nebo chronickým onemocněním jater. Behaviorální indikace: muži mající sex s muži nebo uživatelé nelegálních drog. Profesní indikace: Osoby pracující s primáty infikovanými virem hepatitidy A (HAV) nebo s HAV ve výzkumných laboratořích. Další indikace: Osoby cestující nebo pracující v zemích s vysokou nebo střední endemičností hepatitidy A (seznam zemí vizhttp://www.cdc.gov/travel/diseases.htm#hepa) a všechny osoby, které chtějí získat imunitu. Současné vakcíny by měly být podávány v sérii 2 dávek buď ve věku 0 a 6-12 měsíců, nebo 0 a 6-18 měsíců. Pokud se používá kombinovaná vakcína proti hepatitidě A a hepatitidě B, podávejte 3 dávky v 0, 1 a 6 měsících.
8. Očkování proti hepatitidě B. Lékařské indikace: hemodialyzovaní pacienti (použijte speciální přípravek nebo dvě dávky 20 µg/ml) nebo pacienti, kteří dostávají koncentráty srážecího faktoru. Profesní indikace: zdravotničtí pracovníci a pracovníci veřejné bezpečnosti, kteří jsou na pracovišti vystaveni působení krve, a osoby vzdělávající se na lékařských, stomatologických, ošetřovatelských a laboratorních školách a v dalších příbuzných zdravotnických profesích. Behaviorální indikace: injekční uživatelé drog; osoby s více než jedním sexuálním partnerem během posledních 6 měsíců; osoby s nedávno získanou pohlavně přenosnou chorobou (STD) a muži, kteří mají sex s muži. Další indikace: kontakty v domácnosti a sexuální partneři osob s chronickou infekcí virem hepatitidy B (HBV); klienti a zaměstnanci ústavů pro osoby s vývojovým postižením; všichni klienti klinik pro pohlavně přenosné choroby; chovanci nápravných zařízení; a zahraniční cestovatelé, kteří budou v zemích s vysokým nebo středním výskytem chronické infekce HBV déle než 6 měsíců (seznam zemí viz http://www.cdc.gov/travel/diseases.htm#hepa).
9. Očkování proti meningokokům. Lékařské indikace: dospělí s anatomickou nebo funkční asplenií nebo terminálním deficitem složek komplementu. Další indikace: studenti prvního ročníku vysokých škol žijící na kolejích; mikrobiologové, kteří jsou běžně vystaveni izolátům Neisseria meningitidis; vojenští rekruti; a osoby, které cestují nebo pobývají v zemích, kde je meningokokové onemocnění hyperendemické nebo epidemické (např. „pásmo meningitidy“ v subsaharské Africe v období sucha), zejména pokud bude kontakt s místním obyvatelstvem dlouhodobý. Vláda Saúdské Arábie vyžaduje očkování pro všechny cestující do Mekky během každoroční pouti hadždž. Meningokoková konjugovaná vakcína se upřednostňuje u dospělých splňujících některou z výše uvedených indikací, kteří jsou ve věku <55 let, i když meningokoková polysacharidová vakcína (MPSV4) je přijatelnou alternativou. Revakcinace po 5 letech může být indikována u dospělých, kteří byli dříve očkováni vakcínou MPSV4 a u kterých přetrvává vysoké riziko infekce (např. u osob žijících v oblastech, kde se onemocnění vyskytuje epidemicky).
10. Vybrané stavy, u kterých lze použít vakcínu proti Haemophilus influenzae typu b (Hib). Konjugované Hib vakcíny jsou registrovány pro děti ve věku 6–71 měsíců. Nejsou k dispozici žádné údaje o účinnosti, na jejichž základě by bylo možné vydat doporučení týkající se použití Hib vakcíny u starších dětí a dospělých s chronickými onemocněními spojenými se zvýšeným rizikem onemocnění Hib. Studie však naznačují dobrou imunogenicitu u pacientů, kteří mají srpkovitou anémii, leukémii nebo infekci HIV nebo kteří prodělali splenektomii; podání vakcíny těmto pacientům není kontraindikováno.
Doporučený očkovací kalendář pro dospělé byl schválen Poradním výborem pro očkovací praxi, Americkou akademií porodníků a gynekologů a Americkou akademií rodinných lékařů. Standardní formát poznámek pod čarou MMWR byl pro účely zveřejnění tohoto plánu upraven.
Navržená citace: Centers for Disease Control and Prevention. Doporučený očkovací kalendář pro dospělé—Spojené státy, říjen 2005-září 2006. MMWR 2005;54:Q1–Q4.
Tento rozpis uvádí doporučené věkové skupiny a lékařské indikace pro rutinní aplikaci v současnosti licencovaných vakcín pro osoby ve věku >19 let. Licencované kombinované vakcíny lze použít vždy, když je některá ze složek kombinace indikována a když ostatní složky vakcíny nejsou kontraindikovány. Podrobná doporučení naleznete v příbalových letácích výrobců a v kompletních vyjádřeních ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Všechny klinicky významné reakce po očkování nahlaste do systému hlášení nežádoucích účinků vakcín (VAERS). Formuláře pro hlášení a pokyny k podání hlášení VAERS jsou k dispozici na telefonním čísle 800-822-7967 nebo na webových stránkách VAERS na adrese http://www.vaers.hhs.gov.
Informace o tom, jak podat žádost o odškodnění v rámci Programu odškodnění za poškození způsobená očkováním, jsou k dispozici na adrese http://www.hrsa.gov/osp/vicp nebo na telefonním čísle 800-338-2382. Chcete-li podat žádost o odškodnění za poškození způsobené očkováním, obraťte se na U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, telefon 202-357-6400.
Další informace o výše uvedených vakcínách a kontraindikacích očkování jsou k dispozici také na adrese http://www.cdc.gov/nip nebo v kontaktním centru CDC-INFO na čísle 800-CDC-INFO (232-4636) v angličtině a španělštině, 24 hodin denně, 7 dní v týdnu.
Použití obchodních názvů a komerčních zdrojů slouží pouze k identifikaci a neznamená schválení ze strany Ministerstva zdravotnictví a sociálních služeb USA. odkazy na internetové stránky, které nejsou součástí CDC, jsou poskytovány jako služba čtenářům MMWR a nepředstavují ani neznamenají schválení těchto organizací nebo jejich programů ze strany CDC nebo Ministerstva zdravotnictví a sociálních služeb USA. CDC neodpovídá za obsah stránek, které se na těchto stránkách nacházejí. Adresy URL uvedené v MMWR byly aktuální k datu zveřejnění.
Odmítnutí odpovědnosti Všechny HTML verze článků MMWR jsou elektronickou konverzí z textu ASCII do HTML. Při této konverzi mohlo dojít k překladu znaků nebo k chybám ve formátu verze HTML. Uživatelé by se neměli spoléhat na tento dokument HTML, ale jsou odkázáni na elektronickou verzi PDF a/nebo původní papírovou kopii MMWR, kde je uveden oficiální text, obrázky a tabulky. Originální papírovou kopii tohoto vydání lze získat na adrese Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371; telefon: (202) 512-1800. Pro aktuální ceny kontaktujte GPO.
**Dotazy nebo zprávy týkající se chyb ve formátování zasílejte na adresu [email protected].
Datum poslední revize: 10/13/2005
