Dostat molekuly léku do mozku znamená překonat obrannou hematoencefalickou bariéru. Anthony King zjišťuje, jak chemici pronikají do mozkové pevnosti
Originální činnosti, jako je cvičení nebo jídlo, mohou poměrně výrazně změnit složení naší krve. Může se například zvýšit obsah draslíku v krvi a může dojít k výrazným změnám v obsahu lipidů a aminokyselin. Do krevního oběhu se mohou dostat i metabolity toxické pro nervové buňky.
Krevně-mozková bariéra naštěstí brání tomu, aby se flotsam nebo jetsam v naší krvi dostal do mozku. To je zásadní, protože signalizace neuronů v mozku závisí na elektrických signálech a jemných chemických signálech, které vyžadují přesně regulované mikroprostředí, a to může být snadno narušeno molekulami přicházejícími z krve.
„Nechcete, aby vaše komunikační centrum bylo narušeno věcmi, které se mohou odehrávat v žaludku, střevech nebo jiné oblasti těla. Chcete, aby bylo stabilní a dokonale fungovalo, ať už spíte, nebo vás honí tygr,“ vysvětluje Lester Drewes z Minnesotské univerzity v americkém Duluthu. Hematoencefalickou bariéru neboli BBB tvoří endotelové buňky vystýlající cévy v mozku. Tyto pevnostní buňky jsou k sobě velmi pevně přilepeny a na rozdíl od jiných orgánů a tkání mezi nimi nejsou žádné skuliny, kterými by látky přenášené krví mohly pronikat do mozkové tkáně.

Zdroj: © HAMISH KIDD
Krevní mozková bariéra chrání více než 400 mil kapilár a krevních cév v mozku
Tato obrana je skutečným bolehlavem při léčbě mozkových nádorů a dalších neurologických onemocnění. Léky, které BBB považuje za cizorodé molekuly, nemohou projít. Ve skutečnosti více než 95 % léků nevykazuje v mozku užitečnou aktivitu a mnohé z nich vykazují špatný průnik BBB. Vysoký podíl velkomolekulárních léčiv neprochází, což zahrnuje všechny produkty biotechnologií: rekombinantní proteiny, monoklonální protilátky a RNA interferenční léčiva.
William Pardridge, ředitel Laboratoře pro výzkum hematoencefalické bariéry na Kalifornské univerzitě v Los Angeles (USA), se domnívá, že mise vývoje léků proti Alzheimerově chorobě a dalším mozkovým poruchám utrpěla tím, že se soustředila na objevování léků pro centrální nervový systém, zatímco se zavíraly oči před jejich dodáváním. Říká, že žádná velká farmaceutická společnost na světě dnes nemá program zaměřený na léky pro BBB.
Slizcí zákazníci
Dřívější strategií pro překonání bariéry bylo učinit léky lépe rozpustnými v lipidech; to jim umožnilo proniknout do endotelových buněk v mozku, které lipidy milují. Většina zneužívaných drog, jako je alkohol, kokain a heroin, je lipofilní. Má to však i svou stinnou stránku: „Pokud z něčeho uděláte lipofilní látku, pronikne do každého orgánu a buňky v těle, a proto je třeba použít velké množství. Pokud to může mít špatný vedlejší účinek na jiný orgán nebo tkáň, objeví se,“ říká Drewes.
Některé malé léky – jako například L-DOPA používaný k léčbě Parkinsonovy choroby – lze dopravovat pomocí přirozených „transportních systémů živin“, ale tento přístup má komplikace při hledání správného dávkovacího režimu, protože transportéry pacientů mají různou účinnost. Ačkoli se léky rozpustné v tucích mohou dostat do membrány mozkových endoteliálních buněk, mohou být stejně rychle vyvrženy efluxními transportéry.
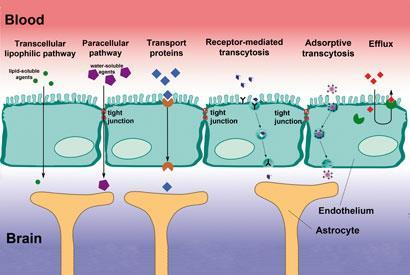
Zdroj: © PŘEPRAVENO Z ARMIN K?BELBECK
Existuje několik mechanismů, jak mohou životně důležité molekuly překonat bariéru, některé z nich mohou být využity léky
„Biologie je skutečně proti dodávání léků do mozku, takže je třeba chytrých strategií,“ říká Joan Abbottová, neuroložka z King’s College London ve Velké Británii. „V minulosti si velké farmaceutické společnosti zjednodušovaly práci tím, že se držely malých molekul, které měly správné chemické složení a vyhýbaly se efluxním transportérům. Jedním z důležitých nedávných poznatků je, že zvýšená rozpustnost v lipidech nemusí být nutně lepší; pro většinu léků je důležitá „volná nevázaná“ koncentrace v mozku, zatímco lipofilní léky mají tendenci ulpívat na jiných strukturách uvnitř mozku, včetně lipidových membrán. „Firemní lékárníci to nyní berou na vědomí,“ dodává Abbott.
V dnešní době si však společnosti uvědomují, že potřebují mnohem inteligentnější léky, aby byly specifičtější a měly méně vedlejších účinků. ‚Proto se snaží zkoumat nové chemické látky, nové nosiče a dokonce i techniky pro krátké otevření BBB a její opětovné uzavření po vstupu léčiva,‘ říká Abbott.
Dočasné portály
Nádory, které začínají v mozku, patří mezi nejagresivnější a nejsmrtelnější druhy rakoviny, avšak možnosti léčby jsou omezeny BBB. Loni v létě vědci z Tchaj-wanu oznámili úspěšné narušení této bariéry pomocí fokusovaného ultrazvuku (viz Chemický svět, září 2010, str. 24). Skupina pod vedením Kuo-Chen Weie z Chang Gung University vstřikovala krysám magnetické nanočástice potažené chemoterapeutikem. Použili ultrazvuk k otevření malé oblasti BBB a magnetické pole k navedení částic na přesné místo v mozku.1
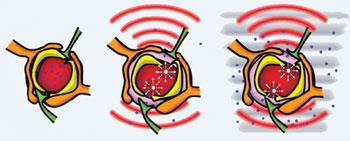
Zdroj: © PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, USA
Ultrazvuk může narušit bariéru a umožnit tak průchod magnetickým částicím
Ultrazvuk by mohl pomoci i při onemocněních, jako je Alzheimerova a Parkinsonova choroba, říká Kullervo Hynynen z lékařské fakulty Torontské univerzity v Kanadě, který provedl podobnou práci s ultrazvukem a mikrobublinami. Podotýká, že přesný fyzikální a biologický mechanismus působení ultrazvuku není znám. ‚Víme, že bubliny se s ultrazvukovou vlnou rozpínají a smršťují, a některé experimenty s rychlou mikroskopií ukázaly, že malé cévy se – alespoň in vitro – s bublinou rozpínají a smršťují. Endotelové buňky se tedy roztahují.‘
Elektronová mikroskopie tuto myšlenku fyzikálního natahování bariérových buněk podpořila, ačkoli je vyvolán i určitý aktivní transport vakuol přes endoteliální buňky, poznamenává Hynynen. Potenciální riziko všech metod narušování BBB spočívá v tom, že se necháte vyvést z míry. Molekuly se při narušení dostanou do mozku, ale toto riziko je malé, protože je vystavena pouze vymezená oblast mozku. Potíže s ultrazvukem souvisejí s nedostatkem znalostí o mechanismu, jakým funguje, spolu s faktory týkajícími se bezpečnosti, účinnosti a časového rozmezí (například jak dlouho je bariéra otevřená).
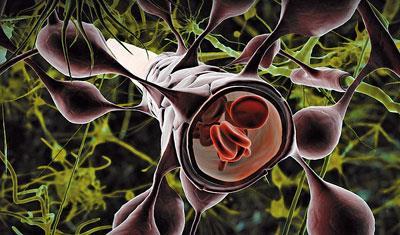
Zdroj: © BEN BRAHIM MOHAMMED
Endotelové buňky těsně obepínají cévy, aby vyloučily
Jiným rušivým přístupem je vstříknutí hyperosmotického roztoku (takového, který má vyšší koncentraci rozpuštěných látek než okolní buňky) do krčních tepen, aby se BBB na určitou dobu otevřela. Tuto metodu již několik let prosazuje Edward Neuwelt z Oregon Health and Science University v americkém Portlandu. „Tekutina proudící cévami je hyperosmotická, a tak odčerpává vodu z endoteliálních buněk, což způsobuje jejich smršťování,“ vysvětluje Drewes. „Tím se rozrušují těsné spoje a vznikají mezery a prostory. Pokud podáte protinádorový lék do krevního oběhu, může difundovat do mozku a do nádoru. Buňky postupně nabobtnají do své obvyklé velikosti, takže účinek je přechodný.
Nádory, které vznikají v mozku, jsou poměrně vzácné; desetkrát více lidí onemocní nádorem mozku z nádorů, které začínají jinde v těle. BBB brzdí moderní léčbu rakoviny, která působí jinde v těle. Američtí vědci však nedávno tuto oblast oživili pomocí léků na erektilní dysfunkci. Julia Ljubimova z Cedars-Sinai Medical Centre v Los Angeles a její kolegové zjistili, že Viagra (sildenafil) a
Levitra (vardenafil), které inhibují enzym zvaný fosfodiesteráza 5 (PDE5), zvyšují propustnost hematoencefalické bariéry. Na myším modelu prokázali, že tyto léky mohou zvýšit množství Herceptinu, velké monoklonální protilátky používané k léčbě rakoviny plic a prsu, procházející přes BBB a zvýšit její protinádorový účinek v mozku.2
Piggy-backing on the BBB
Beverly Davidsonová, neuroložka z University of Iowa v USA, hledala terapii pro děti, které trpí lysozomálním střádáním, způsobeným absencí určitého mozkového enzymu . ‚Víme, že nemůžeme jednoduše dodat enzym do krve, aby se dostal do mozku, a proto se snažíme vymyslet metody, jak tento problém překonat,‘ vysvětluje. Její skupina vzala bariérové endotelové buňky a upravila je tak, aby produkovaly chybějící enzym a vylučovaly ho do samotného mozku.3 „V podstatě děláme z BBB našeho přítele a ne nepřítele.
Rekombinantní DNA, která produkuje enzym, byla do endoteliálních buněk dodána pomocí virového vektoru, který vědci upravili tak, aby se dostal do nemocných mozkových endotelií. Davidson doufá, že nový genetický materiál zůstane v endoteliích po mnoho let. „Nemáme žádné důkazy o tom, že by se tyto buňky vůbec dělily, alespoň u hlodavců,“ vysvětluje, takže jedno kolo genové terapie by mohlo trvat desítky let. Léčba obnovila aktivitu enzymu v celém mozku myšího modelu; dalším krokem je přejít na velký zvířecí model onemocnění.
Kanadská společnost AngioChem vyvinula jiný způsob, jak propašovat terapii přes bariéru – využitím vlastních transportních receptorů. Tyto receptory, jako je protein příbuzný lipoproteinovým receptorům (LRP-1), normálně umožňují vstup základních látek, jako je glukóza, inzulín a růstové hormony, do mozku. „Zdá se, že se jim podařilo poprvé doručit něco, co zaútočí na nádor,“ říká Drewes. „Jsou z toho nadšeni a snaží se to rozvinout do obecnějšího systému podávání léků.
Doručovací prostředky a trojské koně
Další oblastí skutečného růstu jsou umělé konstrukce nebo upravené doručovací prostředky, říká Abbott: „V příštích 10 letech jich očekávám hodně. Nanočástice a různé polymery mohou být konstruovány tak, aby měly správné vlastnosti pro vazbu léčiv, ale také aby rozpoznaly receptory na mozkových endoteliálních buňkách, takže se dostanou přes bariéru. Jednou z výhod polymerů je, že je lze chemicky vyladit, poznamenává Martin Garnett z Centra pro výzkum dětských mozkových nádorů na Nottinghamské univerzitě ve Velké Británii, který začal pracovat na polymerních nanočásticích.
Ljubimova věří, že nanomedicína přinese velký skok v léčbě rakoviny a zlepší kvalitu života pacientů snížením toxicity léčby. ‚V klinických studiích je spousta věcí, které předpovídají velké zisky ‚za pět až deset let‘,‘ říká. Abbott však v souvislosti s takovými nosiči léků nabízí slovo opatrnosti. ‚Potíž je stejná jako u transportérů v BBB. Vypočítat, kolik léčiva se dostane do mozku prostřednictvím dopravních prostředků, je poměrně obtížné. Většina důkazů naznačuje, že množství, které dosáhne správného cíle, je poměrně malé, takže je třeba sáhnout po skutečně aktivních látkách.

Zdroj: © HAMISH KIDD
Molekulární trojský kůň dokáže propašovat léky jako GDNF přes bariéru
Metodu trojského koně, která spojuje terapeutické látky s molekulami, jež normálně procházejí bariérou, prosazuje Pardridge. Znovu vytvořil gliový neurotrofický faktor (GDNF) jako molekulárního trojského koně. GDNF je silný neurotrofin, který dokáže oživit poškozené nervy na zvířecích modelech Parkinsonovy choroby; je to také potenciální léčba mrtvice a drogové závislosti, ale přes BBB neprochází.
Pomocí implantovaných zásobníků s léčivem a komorových katétrů – oba postupy jsou invazivní – vědci zjistili, že GDNF, který dodávali, byl biologicky aktivní, ale postrádal klinickou účinnost. Problémem byla distribuce; bylo zapotřebí velmi přesné umístění katétrů, a toho se nepodařilo dosáhnout ve všech klinických studiích. Pardridgeův Trojan je monoklonální protilátka proti lidskému inzulinovému receptoru, která dokáže GDNF dopravit přes BBB.4 Ve studiích s opicemi rodu Rhesus nezaznamenal žádné nežádoucí účinky spojené s podáváním velkých dávek fúzního proteinu protilátky-GDNF.
Výstup z laboratoře
Abbott naznačuje, že jedním z důvodů pomalého pokroku v oblasti dodávání léků do BBB je nedostatek finančních prostředků a zájmu ze strany průmyslu. Vysvětluje, že velké farmaceutické firmy se do značné míry stáhly z aspektů chemie mozku a dodávání léků, protože vložily mnoho peněz do programů, které se ukázaly jako málo produktivní. Nyní jsou opatrnější, pesimističtější nebo se zaměřují na oblasti s větší šancí na úspěch. Některé společnosti mohou mít dokonce pocit, že nejsou kompetentní sledovat cíle v oblasti mozku, kde je BBB výzvou. Její složité chemické složení ztěžuje předvídatelnost.
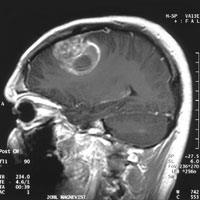
Zdroj: © JULIA LJUBINOV
Nádory v mozku představují zvláštní problém, protože většina běžných léků proti rakovině nemůže bariérou projít
Existují však pozitivní náznaky. V posledních několika letech byly zdokonaleny modely buněčných kultur in vitro pro tuto bariéru – potřebné pro testy propustnosti léčiv. Zobrazovací techniky, jako je pozitronová emisní tomografie (PET) a magnetická rezonance (MRI), pomáhají ukázat, co BBB dělá a které léky se v dostatečné koncentraci dostanou ke správným cílům.
To má zásadní význam, protože vědci si uvědomili, že bariéra není statická obranná struktura. Je to aktivní, regulované a regulační rozhraní; mění se například v místě a okolí poranění po mrtvici. Podle Neuwelta jsou mozkové nádory, epilepsie, Alzheimerova a Parkinsonova choroba spojeny s „poruchami normální BBB, které přispívají k jejich patologii. „5
Informace o stavu bariéry u konkrétního pacienta mohou být nezbytné pro navržení a zpřesnění vhodné terapie. Stále častěji se například u posttraumatických stresových poranění uznává, že je třeba vědět, co bariéra dělá, aby bylo možné upravit léčbu, říká Abbott. Může být nutné upravovat léčbu v průběhu měsíců nebo týdnů.
Garnett říká, že farmaceutické společnosti se dosud soustředily spíše na malé molekuly léků než na systémy jejich podávání, ale to se podle něj nyní mění. Na univerzitách a ve výzkumných ústavech navíc existuje aktivní výzkumná komunita, která se zabývá ultrazvukem, trojskými fúzními proteiny, polymerními konstrukcemi a dalšími prostředky, jak překonat bariéru a dostat léčbu tam, kde je jí třeba.
Abbott v závěru optimisticky hodnotí BBB a snahu dostat přes ni terapii: „Za posledních pět let došlo k velkému pokroku. Vidíme nejrůznější věci, které jsou nyní možné – takže pokud jde o základní porozumění, myslím, že věci vypadají opravdu dobře. Je ale asi pravda, že velká část inovací pochází od malých společností; některé z nich spolupracují s většími společnostmi nebo je převzaly. Tradiční velké farmaceutické firmy jsou stále poměrně opatrné při zkoušení nových způsobů, jak dostat věci do mozku, i když se to mění.
Anthony King je nezávislý vědecký spisovatel z irského Dublinu
.
