Neutrale, polære og elektrisk ladede partikler
På den mindste skala består hjernen, ligesom alle andre materielle objekter, af atomer, som igen består af positivt ladede atomkerner, der er omgivet af en skal med positivt ladede elektroner.
På jorden og i vores hjerner svæver atomerne sjældent rundt isoleret, men klynger sig ofte sammen til molekyler, hvor flere atomer deler nogle af deres elektroner for at danne en fælles, delt ydre skal. Kemikere kalder denne sammenkædning af atomer gennem en fælles elektronskal for en kovalent binding.
Normalt er antallet af positive ladninger i et atoms eller molekyls kerne lig med antallet af elektroner i dets skal, og molekylet siges da at være elektronisk neutralt. De elektrostatiske kræfter, der udgår fra den positivt ladede kerne, ophæves nøjagtigt af de modsatte kræfter fra de negativt ladede elektroner.
Der er imidlertid to måder, hvorpå atomer eller molekyler kan afvige fra en sådan tilstand af neutral balance mellem de elektriske kræfter: De kan enten blive polære, eller de kan blive ioniserede.
I polære molekyler er elektronerne ikke jævnt fordelt rundt om molekylets skal. Et meget almindeligt eksempel på et sådant molekyle, og faktisk det hyppigst forekommende molekyle i vores hjerne, er vand. Vand (H2O) består af et oxygenatom og to hydrogenatomer, der er forbundet med hinanden gennem deres fælles ydre elektronskal.
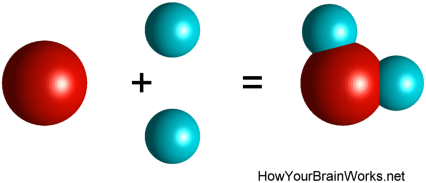
Men de elektroner, der danner den ydre skal, er tættere forbundet med oxygenkernen end med hydrogenkernerne. Den elektriske ladningsfordeling langs vandmolekylet er derfor ikke jævn, og iltatomet er lidt mere negativt ladet end de to brintatomer. Dette bidrager til vandmolekylers tilbøjelighed til at hænge sammen og danne dråber: Den positive H-ende af det ene vandmolekyle tiltrækkes elektrisk af O-enden af det næste molekyle.
Sommetider får atomer ekstra elektroner i deres skal, og bliver derved elektrisk … Ioniserede partikler … under opbygning
Der er to grundlæggende drivkræfter, der ligger til grund for al elektrisk aktivitet i hjernen: elektrostatiske kræfter mellem
