For at få lægemiddelmolekyler ind i hjernen skal man krydse den defensive blod-hjerne-barriere. Anthony King undersøger, hvordan kemikere infiltrerer hjernens fæstning
Ordinære aktiviteter som at motionere eller spise kan ændre vores blodsammensætning ret dramatisk. Blodets kaliumindhold kan f.eks. stige, og der kan ske betydelige ændringer i dets indhold af lipider og aminosyrer. Metabolitter, der er giftige for nerveceller, kan endda komme ind i blodbanen.
Blod-hjernebarrieren blokerer heldigvis for, at fly- og flydele i vores blod ikke kan trænge ind i vores hjerne. Dette er afgørende, fordi neuronernes signalering i hjernen er afhængig af elektriske signaler og fine kemiske signaler, som kræver et præcist reguleret mikromiljø, og dette kan let forstyrres af molekyler, der kommer ind fra blodet.
‘Man ønsker ikke, at ens kommunikationscenter bliver forstyrret af ting, der måske sker i maven, tarmen eller andre områder af kroppen. Det skal være stabilt og fungere perfekt, uanset om man sover eller bliver jagtet af en tiger,” forklarer Lester Drewes fra University of Minnesota i Duluth, USA. Blod-hjernebarrieren, eller BBB, består af de endothelceller, der beklæder blodkarrene i hjernen. Disse fæstningsceller er limet meget tæt sammen, og i modsætning til andre organer og væv er der ingen sprækker mellem dem, hvor blodbårne stoffer kan sive ind i hjernevævet.

Kilde: © HAMISH KIDD
Blod-hjerne-barrieren beskytter over 400 kilometer kapillærer og blodkar i hjernen
Dette forsvar er en sand hovedpine i forbindelse med behandling af hjernetumorer og andre neurologiske sygdomme. Lægemidler, der af BBB behandles som fremmede molekyler, er ikke i stand til at passere. Faktisk viser over 95 % af lægemidlerne ikke nogen nyttig aktivitet i hjernen, og mange af dem trænger dårligt ind i BBB. En stor del af de store molekylære lægemidler kan ikke passere, hvilket omfatter alle produkter fra bioteknologien: rekombinante proteiner, monoklonale antistoffer og RNA-interferensmedicin.
William Pardridge, direktør for Blood-Brain Barrier Research Laboratory ved University of California Los Angeles, USA, mener, at udviklingen af lægemidler mod Alzheimers sygdom og andre hjernesygdomme har lidt under, at man har fokuseret på opdagelse af lægemidler til centralnervesystemet, mens man har set gennem fingre med lægemiddeltilførslen. Han siger, at ingen af de store medicinalvirksomheder i verden i dag har et program, der er rettet mod BBB-lægemidler.
Slibrige kunder
En tidlig strategi for at krydse barrieren var at gøre lægemidler mere lipidopløselige; dette gjorde det muligt for dem at trænge ind i de lipidelskende endothelceller i hjernen. De fleste misbrugsstoffer, som f.eks. alkohol, kokain og heroin, er lipofile. Men der er en ulempe: “Hvis man gør noget lipofilt, vil det trænge ind i alle organer og celler i kroppen, og derfor skal man bruge store mængder. Hvis det kan have en dårlig bivirkning på et andet organ eller væv, så vil det ske,” siger Drewes.
Nogle små lægemidler – som f.eks. L-DOPA, der anvendes til behandling af Parkinsons – kan transporteres ind via naturlige “næringsstoftransportsystemer”, men denne fremgangsmåde har komplikationer med hensyn til at finde den rigtige doseringsordning, da patienternes transportsystemer har forskellig effektivitet. Selv om lipidopløselige lægemidler kan komme ind i hjernens endothelcellemembran, kan de også blive smidt ud lige så hurtigt af effluxtransportørerne.
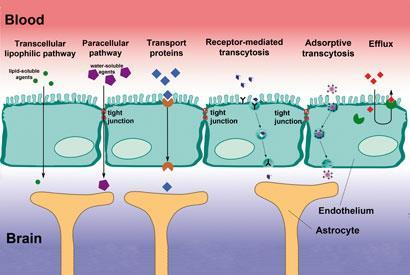
Kilde: © ADAPTERET FRA ARMIN K?BELBECK
Der findes flere mekanismer, hvormed livsvigtige molekyler kan krydse barrieren, og nogle af dem kan udnyttes af lægemidler
“Biologien er virkelig imod lægemiddeltilførsel til hjernen, så der er brug for smarte strategier”, siger Joan Abbott, der er neurovidenskabsmand ved King’s College i London, Storbritannien. “Tidligere har de store medicinalfirmaer forenklet tingene ved at holde sig til små molekyler, som havde den rette kemi og undgik effluxtransportørerne”. En vigtig nyere indsigt er, at øget lipidopløselighed ikke nødvendigvis er bedre; for de fleste lægemidler er det den “frie ubundne” koncentration i hjernen, der er vigtig, mens lipofile lægemidler har en tendens til at klæbe til andre strukturer i hjernen, herunder lipidmembraner. “Virksomhedernes lægemiddelkemikere er nu ved at tage dette til sig”, tilføjer Abbott.
Derimod er virksomhederne i dag klar over, at de har brug for langt mere intelligente lægemidler for at gøre dem mere specifikke med færre bivirkninger. “Det er derfor, de forsøger at udforske nye kemikilder, nye leveringsmidler og endda teknikker til kortvarigt at åbne BBB og derefter lukke den igen, efter at et lægemiddel er kommet ind”, siger Abbott.
Temporære portaler
Tumorer, der begynder i hjernen, er blandt de mest aggressive og dødbringende kræftformer, men behandlingsmulighederne er begrænset af BbB. Sidste sommer rapporterede forskere i Taiwan, at det var lykkedes dem at bryde barrieren ved hjælp af fokuseret ultralyd (se Chemistry World, september 2010, s. 24). Under ledelse af Kuo-Chen Wei fra Chang Gung University injicerede gruppen magnetiske nanopartikler, der var belagt med et kemoterapimiddel, i rotter. De brugte ultralyd til at åbne et lille område af BbB og et magnetfelt til at lede partiklerne til et præcist sted i hjernen.1
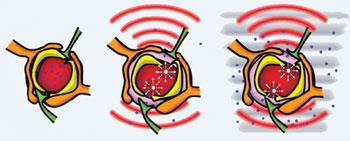
Kilde:
Ultralyd kan bryde barrieren, så magnetiske partikler kan ledes igennem
Ultralyd kunne også hjælpe ved sygdomme som Alzheimers og Parkinsons, siger Kullervo Hynynynen fra University of Toronto Medical School i Canada, som har udført lignende arbejde med ultralyd og mikrobobler. Den nøjagtige fysiske og biologiske mekanisme ved ultralyd er ikke kendt, påpeger han. “Vi ved, at boblerne udvider sig og trækker sig sammen med ultralydsbølgen, og nogle hurtige mikroskopiforsøg har vist, at de små blodkar – i det mindste in vitro – udvider sig og trækker sig sammen med boblen. Derfor bliver endothelcellerne strakt ud”.
Elektronmikroskopi har understøttet denne idé om fysisk strækning af barrierecellerne, selv om der også induceres en vis aktiv vacuoletransport på tværs af endothelcellerne, bemærker Hynynynen. Den potentielle risiko ved alle BBB-forstyrrelsesmetoder er, at man lader sin vagt falde. Molekyler vil trænge ind i hjernen under afbrydelsen, men denne risiko er lille, da kun et afgrænset område af hjernen udsættes. Vanskelighederne med ultralyd vedrører den manglende viden om den mekanisme, hvormed den virker, sammen med faktorer vedrørende sikkerhed, effektivitet og tidshorisont (f.eks. hvor længe barrieren er åben).
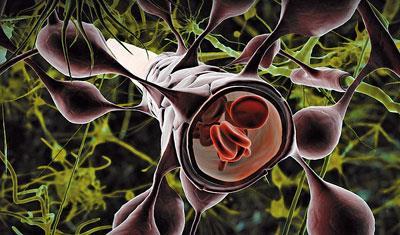
Kilde: © BEN BRAHIM MOHAMMED
Endothelcellerne omslutter blodkarrene tæt for at udelukke
En anden forstyrrende metode er at injicere en hyperosmotisk opløsning (en opløsning, der har en højere koncentration af opløste stoffer end de omkringliggende celler) i halspulsårerne for at åbne BBB for en tid. Denne metode har Edward Neuwelt fra Oregon Health and Science University i Portland, USA, været fortaler for i nogle år nu. “Den væske, der strømmer gennem blodkarrene, er hyperosmotisk og trækker derfor vand ud af endothelcellerne, hvilket får dem til at skrumpe”, forklarer Drewes. “Dette trækker de tætte forbindelser fra hinanden og danner huller og mellemrum. Hvis man indfører et antitumormedicin i blodstrømmen, kan det diffundere ind i hjernen og ind i tumoren”. Cellerne svulmer gradvist op til deres sædvanlige størrelse igen, så virkningen er forbigående.
Mens kræftformer, der udvikler sig i hjernen, er relativt sjældne; 10 gange så mange mennesker udvikler hjernetumorer fra kræftformer, der begynder andre steder i kroppen. BBB hæmmer moderne kræftbehandlinger, der virker andre steder i kroppen. Amerikanske forskere gav dog for nylig området et løft ved hjælp af lægemidler mod erektil dysfunktion. Julia Ljubimova fra Cedars-Sinai Medical Centre i Los Angeles og hendes kolleger fandt, at Viagra (sildenafil) og
Levitra (vardenafil), som hæmmer et enzym kaldet phosphodiesterase 5 (PDE5), øgede blod-hjerne-barrierens gennemtrængelighed. Ved hjælp af en musemodel viste de, at disse lægemidler kan øge mængden af Herceptin, et stort monoklonalt antistof, der anvendes til behandling af lunge- og brystkræft, der krydser BbB og øger dets anti-tumoreffekt i hjernen.2
Piggy-backing på BbB
Beverly Davidson, en neurolog ved University of Iowa, USA, har søgt efter en behandling til børn, der lider af lysosomal lagringssygdom, der skyldes fravær af et bestemt enzym i hjernen. “Vi ved, at vi ikke bare kan give enzymet til blodet og få det til hjernen, så vi forsøger at udvikle metoder til at overvinde dette problem”, forklarer hun. Hendes gruppe tog endothelceller i barrieren og manipulerede dem til at producere det manglende enzym og udskille det i selve hjernen.3 “I bund og grund gør vi BbB til vores ven i modsætning til vores fjende”.
Det rekombinante DNA, der producerer enzymet, blev leveret til endothelcellerne ved hjælp af en viral vektor, som forskerne havde modificeret til at finde hjem til de syge hjerneendotheler. Davidson håber, at det nye genetiske materiale vil forblive i endotheliaerne i mange år. “Vi har ingen tegn på, at disse celler deler sig overhovedet, i det mindste hos gnavere”, forklarer hun, så en enkelt runde genterapi kan vare i årtier. Behandlingen genskabte enzymaktiviteten i hele hjernen i en musemodel; det næste skridt er at gå over til en større dyremodel af sygdommen.
Den canadiske virksomhed AngioChem har udviklet en anden måde at smugle terapier over barrieren på – ved at udnytte sine egne transportreceptorer. Disse receptorer, som f.eks. lipoproteinreceptorrelateret protein (LRP-1), giver normalt vigtige stoffer som glukose, insulin og væksthormoner mulighed for at komme ind i hjernen. “Det ser ud til at være den første succes med at levere noget, der kan angribe en tumor”, siger Drewes. “Det er der en vis begejstring over, og de forsøger at udvikle det til et mere generelt lægemiddeltilførselssystem.
Leveringsmidler og trojanske heste
Et andet område med reel vækst er kunstige konstruktioner eller konstruerede leveringsmidler, siger Abbott: “I løbet af de næste 10 år forventer jeg, at der vil komme mange af dem. Nanopartikler og forskellige polymerer kan konstrueres til at have de rigtige egenskaber til at binde lægemidler, men også til at genkende receptorer på hjernens endothelceller, så de bliver ført over barrieren. En af fordelene ved polymerer er, at man kan indstille dem kemisk, bemærker Martin Garnett fra Children’s Brain Tumor Research Centre ved University of Nottingham i Det Forenede Kongerige, som har påbegyndt en del arbejde med polymernanopartikler.
Ljubimova mener, at nanomedicin vil give et stort spring fremad inden for kræftbehandling og forbedre patienternes livskvalitet ved at reducere giftigheden af behandlingerne. “Der er masser af ting i kliniske forsøg, som forudsiger store gevinster “om fem til ti år”,” siger hun. Abbott giver dog et ord af forsigtighed med hensyn til sådanne lægemiddelkøretøjer. “Problemet er det samme som med transportører i BBB. Det er ret svært at beregne, hvor meget af et lægemiddel der kommer ind i hjernen via transportmidler. De fleste beviser tyder på, at den mængde, der når det rigtige mål, er ret lille, så man er nødt til at gå efter virkelig aktive stoffer”.

Kilde: © HAMISH KIDD
En molekylær trojansk hest kan snige lægemidler som GDNF over barrieren
En trojansk hest-metode, som knytter terapeutiske midler til molekyler, der normalt passerer barrieren, er Pardridge forkæmper for. Han har genudviklet glial-derived neurotrophic factor (GDNF) som en molekylær trojansk hest. GDNF er en potent neurotrofin, der kan genoplive beskadigede nerver i dyremodeller af Parkinsons sygdom; det er også en potentiel terapi mod slagtilfælde og stofmisbrug, men det krydser ikke BBB.
Ved hjælp af implanterede lægemiddelreservoirer og ventrikelkatetre – begge invasive procedurer – opdagede forskerne, at det GDNF, de leverede, var biologisk aktivt, men manglede klinisk effekt. Problemet var fordelingen; det var nødvendigt med en meget præcis placering af katetrene, og dette blev ikke opnået i alle kliniske forsøg. Pardridge’s Trojan er et monoklonalt antistof mod den humane insulinreceptor, som kan levere GDNF på tværs af BBB.4 I forsøg med Rhesusaber har han ikke set nogen bivirkninger i forbindelse med indgivelse af store doser af antistof-GDNF-fusionsprotein.
Afgang fra laboratoriet
Abbott antyder, at en af grundene til, at fremskridtene med hensyn til tilgivelse af lægemidler til BBB har været langsomme, er mangel på finansiering og interesse fra industrien. Hun forklarer, at store medicinalvirksomheder stort set har trukket sig tilbage fra aspekter af hjernekemi og lægemiddeloverførsel, fordi de har investeret mange penge i programmer, som har vist sig ikke at være produktive. De er nu mere forsigtige, mere pessimistiske, eller de fokuserer på områder med større chancer for succes. Nogle virksomheder føler måske endda, at de ikke er kompetente til at forfølge mål i hjernen, hvor BBB er en udfordring. Dens komplekse kemi gør forudsigelighed vanskeligere.
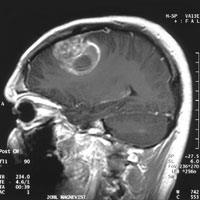
Kilde: © JULIA LJUBINOV
Tumorer i hjernen udgør et særligt problem, da de fleste almindelige kræftlægemidler ikke kan krydse barrieren
Der er dog positive tegn. In vitro cellekulturmodeller af barrieren – som er nødvendige for test af lægemidlers permeabilitet – er blevet forbedret i løbet af de sidste par år. Billeddannelsesteknikker som positronemissionstomografi (PET) og magnetisk resonansbilleddannelse (MRI) er med til at vise, hvad BBB gør, og hvilke lægemidler der når frem til de rigtige mål i tilstrækkelig koncentration.
Dette er afgørende, da forskerne er kommet til den erkendelse, at barrieren ikke er en statisk forsvarsstruktur. Det er en aktiv, reguleret og regulerende grænseflade; den ændres på og omkring skadestedet efter f.eks. et slagtilfælde. Ifølge Neuwelt er hjernetumorer, epilepsi, Alzheimers sygdom og Parkinsons sygdom alle forbundet med “forstyrrelser i den normale BBB, som bidrager til deres patologi. “5
Informationer om barrierens status hos en bestemt patient kan være nødvendige for at udtænke og forfine passende behandlinger. I stigende grad i forbindelse med f.eks. posttraumatiske stressskader anerkendes det, at man er nødt til at vide, hvad barrieren gør, for at tilpasse behandlingen, siger Abbott. Det kan være nødvendigt at justere behandlingen over en periode på flere måneder eller uger.
Garnett siger, at medicinalvirksomhederne indtil nu har koncentreret sig om små lægemiddelmolekyler snarere end om systemer til lægemiddeloverførsel, men han mener, at dette nu er ved at ændre sig. Desuden er der et aktivt forskningsmiljø inden for universiteter og forskningsinstitutter, der kigger på ultralyd, trojanske fusionsproteiner, polymerkonstruktioner og andre midler til at overvinde barrieren og få behandlingen frem til det sted, hvor der er behov for den.
Abbott slutter med en optimistisk vurdering af BBB og bestræbelserne på at få terapier over den: “Der er sket mange fremskridt i de sidste fem år. Vi ser alle mulige ting, som nu er mulige – så med hensyn til den grundlæggende forståelse synes jeg, at tingene ser rigtig godt ud. Men det er nok rigtigt at sige, at en stor del af innovationen kommer fra små virksomheder; nogle af dem indgår partnerskaber med eller er blevet overtaget af større virksomheder. De traditionelle store medicinalvirksomheder er stadig ret forsigtige med at prøve nye måder at få ting ind i hjernen på, men det er dog ved at ændre sig.
Anthony King er freelance videnskabsskribent med base i Dublin, Irland
