INDLEDNING
Grundlæggende og klinisk forskning udført i de seneste år har etableret en direkte, 2-vejs sammenhæng mellem kronisk nyresygdom og kardiovaskulær sygdom.1,2 I den daglige kliniske praksis anvendes serumkreatininkoncentrationer og den glomerulære filtrationshastighed estimeret med Cockcroft-Gault3 -formlen eller Modification of Diet in Renal Disease (MDRD)4-ligningen almindeligvis til at vurdere nyrefunktionen. Plasmakreatininkoncentrationer kan imidlertid påvirkes af en række faktorer, såsom patientens alder, køn, muskelmasse, fysisk aktivitet, kost og medicinering.5
Cystatin C er en proteininhibitor af cysteinprotease, som syntetiseres med en stabil hastighed af alle kerneceller. På grund af dets lave molekylvægt og høje isoelektriske punkt kan det næsten udelukkende elimineres ved glomerulær filtration. Cystatin C-koncentrationerne påvirkes ikke af alder, køn eller proteinindtagelse, og de er følsomme over for små ændringer i glomerulær filtration. På grund af disse egenskaber anses plasmakoncentrationen af cystatin C for at være en af de bedste markører for glomerulær filtreringsstatus.6-9 For nylig har flere undersøgelser rapporteret om en sammenhæng mellem forhøjede cystatin C-værdier og udvikling af kardiovaskulære komplikationer hos patienter med koronarsygdom. Det vides i øjeblikket ikke, om denne sammenhæng skyldes, at cystatin C er en bedre markør for nyrefunktionen end serumkreatinin, eller om der er andre faktorer end glomerulær filtration, som påvirker koncentrationen af dette protein og desuden er relateret til kardiovaskulær risiko10 .
Sigtet med denne undersøgelse var at vurdere den prognostiske værdi af plasma cystatin C-koncentrationen hos patienter indlagt for akut koronarsyndrom (ACS) med høj risiko, og at undersøge forholdet mellem cystatin C og andre markører for nyrefunktion og inflammation.
METODER
Dette er en prospektiv, observationel undersøgelse, der blev udført mellem maj 2006 og juli 2007. I alt 203 patienter over 18 år og konsekutivt indlagt på hjerteintensivafdelingen (ICU) i vores center med en diagnose af højrisiko-ACS blev inkluderet.
De diagnostiske kriterier for højrisiko-ACS omfattede mindst 2 af følgende faktorer: smerter med iskæmiske karakteristika, elektrokardiografiske ændringer, der er i overensstemmelse med iskæmi, og/eller forhøjede myokardienekrosemarkører. Den behandling, der blev givet, og de yderligere undersøgelser, der blev udført under patientens hospitalsophold, var baseret på den behandlende læges kliniske beslutninger. Hos de fleste patienter blev der anvendt en invasiv strategi, der omfattede akut koronarangiografi (ved myokardieinfarkt med ST-segmentforhøjelse eller venstre grenblok) eller tidlig planlagt koronarangiografi i løbet af de første 24 til 72 timer efter indlæggelsen.
Kliniske karakteristika
Følgende data blev registreret fra patienternes kliniske journaler: demografiske oplysninger, tilstedeværelse af klassiske kardiovaskulære risikofaktorer (diabetes mellitus, systemisk hypertension, dyslipidæmi og rygning) og historie med kendt vaskulær sygdom (iskæmisk hjertesygdom, cerebrovaskulær sygdom, perifer arteriel sygdom og tidligere myokardie-revaskulariseringsbehandling). De øvrige kliniske variabler, der blev analyseret, omfattede typen af ACS, Killip-klasse på tidspunktet for indlæggelsen, systoliske og diastoliske trykværdier, pulstryk (estimeret som forskellen mellem systolisk og diastolisk arterielt tryk) og hjertefrekvens.
Alle patienter gennemgik ekkokardiografi, hvor den venstre ventrikulære ejektionsfraktion blev estimeret med Simpson-metoden ved hjælp af en 4-kammers tilgang; gennemsnittet af 3 bestemmelser blev beregnet hos patienter med sinusrytme og gennemsnittet af 5 bestemmelser hos patienter med atrieflimmer.
I 95 % af patienterne blev der foretaget koronarangiografi, og sværhedsgraden af koronarlæsioner blev vurderet med en score baseret på antallet af berørte epikardiale koronararterier.
Analytiske data
Basisværdierne for hæmoglobin, hæmatokrit, leukocytter, glukose og kreatinin blev registreret i de første laboratorieanalyser, der blev udført på vores center på tidspunktet for indlæggelsen på hospitalet. Koncentrationerne af totalkolesterol, højdensitetslipoproteinkolesterol (HDL-C), lavdensitetslipoproteinkolesterol (LDL-C), glukose, højfølsomt C-reaktivt protein og cystatin C blev registreret i de første 24 timer sammen med det maksimale troponin I (TpI)-niveau.
Cystatin C blev målt med et automatiseret homogent immunoassay ved hjælp af et Dade-Behring BN ProSpec nefelometer. Reagenset til analysen bestod af polystyrenpartikler belagt med antistoffer mod proteinet, som agglutinerer, når de blandes med prøver, der indeholder cystatin C, og som spreder lys med en intensitet, der er proportional med koncentrationen af analysanden.
Referenceintervallet for serumkoncentrationen af cystatin C hos voksne med den anvendte nefelometriske metode er 0,51 til 0,95 mg/L. Koncentrationerne af højfølsomt C-reaktivt protein blev også bestemt ved hjælp af immunoassay. Den glomerulære filtrationshastighed blev vurderet ved hjælp af MDRD-ligningen.
Analyserede episoder
De kardiovaskulære komplikationer, der blev analyseret, omfattede dødelighed på hospitalet, dødelighed af alle årsager under opfølgningen, udvikling af et nyt myokardieinfarkt, defineret som brystsmerter eller tilsvarende anginøse smerter med EKG-forandringer eller forhøjede tumornekrosemarkører i løbet af de første 24 timer efter indlæggelse (patienter med forhøjede markører efter koronarinterventionelle procedurer blev udelukket), og udvikling af hjertesvigt under indlæggelse eller opfølgning.
Klinisk opfølgning
Den gennemsnitlige opfølgning var 186 (SD, 110; median, 156) dage, i hvilken periode alle patienternes kliniske hændelser blev registreret. Opfølgningen blev udført ved telefonisk kontakt, i ambulatorier og ved gennemgang af patienternes sygehusjournaler.
Statistisk analyse
Alle oplysninger blev prospektivt registreret i en database oprettet med Microsoft Office Access 2003 SP2. De statistiske analyser blev udført med SPSS (Statistical Package for the Social Sciences), version 12.0. De kategoriske eller dikotomiske variabler er udtrykt som absolutte værdier og procentdele og blev sammenlignet med Pearson χ2-testen. De kontinuerlige variabler med normal fordeling er beskrevet som middelværdi (SD), og Student t-testen blev anvendt til sammenligninger mellem grupperne. Variabler, der ikke udviste en gaussisk fordeling, blev sammenlignet med Mann-Whitney U-testen.
Spearmans korrelationskoefficient blev anvendt til at evaluere korrelationerne mellem cystatin C-koncentrationen og højfølsomt C-reaktivt protein og glomerulær filtrationshastighed. Der blev anvendt en logistisk regressionsanalyse til at vurdere den uafhængige rolle af kliniske og laboratoriefaktorer med hensyn til cystatin C for forudsigelse af udviklingen af kardiovaskulære komplikationer under indlæggelse, herunder de signifikante variabler i den univariate analyse. De justerede odds ratio’er og 95 % konfidensintervaller (CI) er præsenteret. Kaplan-Meier-overlevelseskurver under opfølgningen blev konstrueret og sammenlignet ved hjælp af long-rank-testen.
For at foretage en beskrivende analyse af den undersøgte population blev nogle kvantitative variabler kategoriseret i intervaller: den glomerulære filtrationshastighed (>90, 90-60, 55% og 0,95 og
En P-værdi på mindre end 0,05 blev anset for statistisk signifikant.
RESULTATER
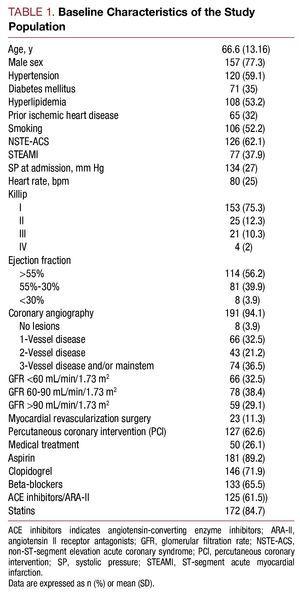
Fra maj 2006 til juli 2007 blev 203 patienter, der blev indlagt med en højrisiko-ACS-diagnose, inkluderet i undersøgelsen. Gennemsnitsalderen var 66,6 (13,16) år. Blandt de samlede patienter præsenterede 62,1 % af patienterne (n=126) ikke-ST-segment elevation ACS og 37,9 % (n=77), ST-segment elevation ACS. Undersøgelsespopulationens baselinekarakteristika er beskrevet i tabel 1.
Mediankoncentrationen af cystatin C var 1,01 (interval, 0,83-1,35) mg/L, plasmakreatinin ved den første udførte analyse var 1 (0.9-1,3) mg/L, glomerulær filtrationshastighed var 72,4 (49,12-93,73) mL/min/1,73 m2, og højfølsomt C-reaktivt protein var 1,37 (0,46-5,02) mg/L. Den glomerulære filtration på tidspunktet for indlæggelse var 2 hos 32,5 % af patienterne, og serumcystatin C var >0,95 mg/L hos 113 (55,7 %) patienter.
Patienter med højere cystatin C-værdier præsenterede en dårligere klinisk profil, var ældre, havde en høj prævalens af hypertension, dårligere Killip-klasse på indlæggelsestidspunktet, mere alvorlig koronar sygdom på koronarangiografi og højere plasmakreatinin- og C-reaktive proteinværdier (Tabel 2).
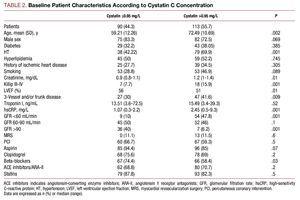
Der var ingen signifikante forskelle mellem de 2 cystatin C-grupper med hensyn til den udførte koronarintervention; det endelige angiografiske resultat gav en lignende succesrate og ingen signifikante komplikationer (3,27 % for patienter med cystatin C ≤0,95 og 4,09 % i den anden gruppe). Analysen af den farmakologiske behandling viste en væsentlig højere anvendelse af betablokkere og aspirin i gruppen med cystatin C ≤0,95 (tabel 2).
Serum cystatin C-værdier viste en højere korrelation med estimeret glomerulær filtrationshastighed (r=-0,655; P=,001) (figur 1) end med mikroalbuminuri (r=0,302, P=,01) og en lavere korrelation med C-reaktivt protein (r=0,29; P=,01).
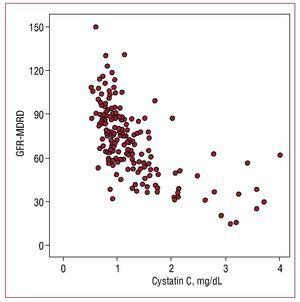
Figur 1. Korrelation mellem cystatin C-værdier og glomerulær filtrationshastighed estimeret med MDRD-formlen (GFR-MDRD).
I gruppen af patienter med cystatin C-værdier >0,95 havde 6,5 % normale glomerulære filtrationshastigheder og 46 % glomerulære filtrationshastigheder mellem 60 og 90 mL/min/1,73 m2. Desuden havde 10 % af de patienter, der havde nyrefunktionsforstyrrelser med en filtrationsrate på 2, cystatin C værdier
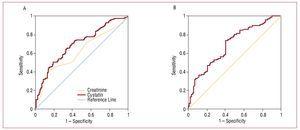
Figur 2. A, ROC’er for cystatin C og kreatinin i forhold til udvikling af kardiovaskulære komplikationer (hjertesvigt, infarkt og kardiovaskulær død). B, ROC-kurve for den glomerulære filtrationshastighed estimeret med MDRD i forhold til udvikling af kardiovaskulære komplikationer (hjertesvigt, infarkt og kardiovaskulær død).
Hospitalsopholdet varede i median 9 (6-19) dage. Fra indlæggelsestidspunktet til afslutningen af studiets opfølgning havde 56 (27,58 %) patienter fra den samlede stikprøve udviklet hjertesvigt, de fleste af dem i gruppen med forhøjede cystatin C-værdier (45 patienter). Mortaliteten på hospitalet var signifikant højere i gruppen med forhøjede cystatin C-værdier (17,6 % vs. 3,3 %; P=.001), og disse forskelle var vedvarende under opfølgningen (figur 3, tabel 4).
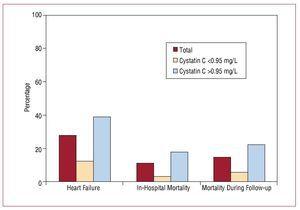
Figur 3. Sammenhæng mellem cystatin C 0,95 mg/L og udvikling af kardiovaskulære hændelser under indlæggelse på hospitalet.

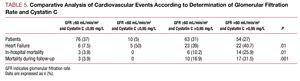
I den univariate analyse blev der ikke observeret nogen sammenhæng mellem kardiovaskulære komplikationer og typen af ACS, hyperlipidæmi eller peak TpI-koncentration, men der blev fundet en sammenhæng med de resterende kardiovaskulære risikofaktorer: antallet af berørte kar, ejektionsfraktion, nyrefunktionsmarkører, cystatin C og højfølsomt C-reaktivt protein. Da resultaterne fra patienter med en glomerulær filtrationshastighed på >60 mL/min/1,73 m2 blev analyseret, fandt vi, at patienter med cystatin C >0.95 mg/L præsenterede en signifikant højere rate af kardiovaskulære komplikationer end patienter med glomerulær filtration >60 og cystatin C 60 og cystatin C
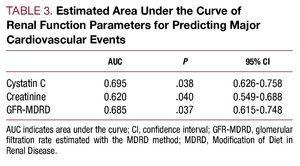
Et estimeret hændelsesfri overlevelse (dvs. ingen hjertesvigt, myokardieinfarkt eller død) efter en gennemsnitlig opfølgning på 186 dage var signifikant højere i gruppen af patienter med cystatinværdier ≤0.95 mg/L: 75 % mod 44 % (P=.02) (Figur 4).

Figur 4. Kaplan-Meier-kurver til estimering af sandsynligheden for overlevelse uden større kardiovaskulære hændelser i henhold til cystatin C-værdien.
Den multivariate analyse identificerede alder, ejektionsfraktion og cystatin C-koncentration som uafhængige prædiktive faktorer for kardiovaskulære komplikationer under indlæggelse (tabel 6).
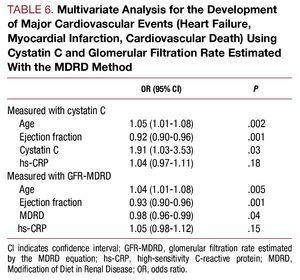
DISCUSSION
Resultaterne af den foreliggende undersøgelse viser, at forhøjede cystatin C-værdier forudsiger udviklingen af hjertesvigt, myokardieinfarkt og kardiovaskulær død under indlæggelse hos patienter med højrisiko-ACS uafhængigt af andre klassiske risikofaktorer. Desuden kan plasma cystatin C-værdien have en større evne til at stratificere patienter med høj risiko for kardiovaskulære komplikationer under indlæggelse end andre metoder til vurdering af nyrefunktionen. Vi fandt, at forhøjet cystatin C var forbundet med en dårligere kardiovaskulær prognose, selv i gruppen af patienter med normal glomerulær filtration. Så vidt vi ved, er dette den første rapport om denne sammenhæng, som vi mener kan have betydning for risikostratificering i denne patientpopulation.
I de seneste år har flere artikler beskrevet en tæt sammenhæng mellem nyrefunktionsforstyrrelser og kardiovaskulære komplikationer under opfølgning af patienter med akut og kronisk iskæmisk hjertesygdom samt andre kliniske præsentationer af kardiovaskulær sygdom, især hjertesvigt.1,10-12 En reduktion i glomerulær filtration under 60 mL/min er forbundet med en betydelig stigning i risikoen for død, myokardieinfarkt og slagtilfælde, både hos patienter med eller uden forudgående kardiovaskulær sygdom.13 Specifikt er denne sammenhæng beskrevet hos ACS-patienter med ST-segmentelevation og patienter uden.10,13-15 I VALIANT-undersøgelsen16 (patienter med ventrikeldysfunktion og hjertesvigt efter et myokardieinfarkt med ST-segmentelevation) var en forværring af nyrefunktionen (vurderet med den glomerulære filtrationshastighed) forbundet med en stigning i dødelighed og kardiovaskulære komplikationer under opfølgningen. Lignende resultater er blevet rapporteret for de patientpopulationer, der indgår i SAVE- (postinfarktventrikulær dysfunktion), HOPE- (patienter med høj kardiovaskulær risiko, de fleste med kronisk iskæmisk hjertesygdom) og PEACE- (patienter med kronisk iskæmisk hjertesygdom) undersøgelser. I disse undersøgelser blev forholdet mellem nyrefunktionsforstyrrelser og prognosen observeret for nedsat glomerulær filtrationshastighed og for urinalbuminudskillelse.16-19
Som nævnt ovenfor er der beskrevet et direkte 2-vejsforhold mellem nyrefunktionsforstyrrelser og hjerte-kar-sygdomme. Kronisk nyresvigt begunstiger udviklingen af hypertension og dyslipidæmi og fremmer aktivering af renin-angiotensinaldosteronsystemet. Disse faktorer synes sammen med stigningen i inflammatoriske mediatorer at bidrage til en højere produktion af frie radikaler, som griber ind i den aterosklerotiske proces og kardiovaskulære skader. Desuden begunstiger ændringer i mineralstofskiftet (stigning i promotorer og fald i inhibitorer af forkalkning) kalkaflejringer i kranspulsårerne.20,21 Endelig er der beskrevet en mindre intensiv anvendelse af terapeutiske interventioner med anerkendt klinisk og prognostisk fordel hos patienter med nyrefunktionsforstyrrelser. Specifikt hos dem med ACS kan mindre aggressiv behandling og længere forsinkelser i udførelsen af interventionelle koronarprocedurer samt lavere brug af IIb/IIIa, blokkere af reninangiotensin-aldosteron-aksen, betablokkere, statiner og trombocythæmmende midler bidrage til den dårligere prognose, der er beskrevet i denne patientpopulation22 .
I den daglige kliniske praksis er vurderingen af nyrefunktionen normalt baseret på serumkreatininbestemmelser og estimater af den glomerulære filtrationshastighed ved hjælp af Cockcroft-Gault- eller MDRD-formlerne. Begge disse metoder har flere begrænsninger, hvoraf mange er afledt af faktorer, der påvirker kreatininproduktionen, såsom alder, kvindelig køn, race-relaterede karakteristika, kost og forløbet af kroniske sygdomme.
Disse ligninger blev for nylig evalueret hos patienter med hjertesvigt og sammenlignet med NT-proBNP, der er en prognostisk markør. Den prognostiske information, som NT-proBNP giver, viste sig at være bedre end den prognostiske information om nyrefunktionen, der er estimeret ved hjælp af MDRD-formlen.23
Cystatin C har molekylære og metaboliske egenskaber, der gør plasmakoncentrationerne af dette protein til en god biologisk markør til estimering af nyrefunktionen; små funktionelle ændringer påvises med en højere sensitivitet end de konventionelle parametre, der anvendes til dette formål.24 Dette kan begrunde det forhold, at i gruppen af patienter med serumkoncentrationer af cystatin C over den øvre normalgrænse, havde 15 % en normal glomerulær filtrationshastighed; bestemmelse af statin C kan være nyttig til identifikation af patienter med en præklinisk tilstand af nyresygdom.6
De resultater, der er opnået i den foreliggende undersøgelse, er til en vis grad i overensstemmelse med de rapporterede resultater, der indikerer, at cystatin C er en uafhængig prædiktor for kardiovaskulære komplikationer hos patienter med koronar sygdom.25-27 Desuden kan vores data udvide dette koncept til at omfatte patienter med normal glomerulær filtrationshastighed. Jernberg et al26 analyserede forholdet mellem plasma cystatin C værdier og prognose i en gruppe patienter indlagt for ACS uden ST-segment-elevation og rapporterede en signifikant sammenhæng mellem cystatin C værdier og dødelighed. Det er også blevet beskrevet, at forhøjede cystatin C-koncentrationer er forbundet med en øget risiko for død, kardiovaskulære komplikationer og forekomsten af hjertesvigt hos ambulante patienter med kronisk koronarsygdom.24 Hos ældre personer uden manifest nyresygdom er cystatin C en risikomarkør for død, kardiovaskulær sygdom og kronisk nyresygdom.6 I den aktuelle undersøgelse fandt vi, at patienter med forhøjede cystatin C-niveauer havde en dårligere risikoprofil; dog var det relativt lave C-reaktive proteinniveau overraskende. Vi mener, at dette kan forklares ved proteinets kinetik, som har et specifikt, karakteriseret spektrum, hvor dets værdi afhænger af tidspunktet, hvor prøven udtages (toppen opstår 49 timer efter symptomdebut, og en mere forsinket top ses ved ST-segment-elevation akut myokardieinfarkt); i vores undersøgelse blev prøverne udtaget inden for de første 24 timer efter indlæggelse på hospitalet.28 De kardiovaskulære komplikationer, der ramte patienterne i vores undersøgelse, adskiller sig fra dem, der er offentliggjort i nyere registre29 , og dette kan skyldes, at der blev inkluderet patienter med meget høj risiko og med en højere forekomst af komplikationer. I det nyligt offentliggjorte MASCARA-register var kun 50 % af de inkluderede patienter oprindeligt blevet indlagt på en intensivafdeling eller hjerteintensivafdeling, hvorimod alle vores patienter kom fra en hjerteintensivafdeling, hvilket utvivlsomt indebærer en vis selektionsbias. Ikke desto mindre bestod patientgruppen med forhøjet cystatin C af en population med en betydelig højere risikoprofil og et betydeligt højere antal kardiovaskulære komplikationer end de resterende patienter. Den foreliggende undersøgelse bidrager til at etablere større præcision i disse sammenhænge ved at give den første rapport om, at forhøjede cystatin C-niveauer i de første timer af indlæggelse for højrisiko-ACS er en uafhængig prædiktor for kardiovaskulære komplikationer på hospitalet. Desuden er sammenhængen mellem cystatin C og en risiko for kardiovaskulære komplikationer højere end for andre almindeligt anvendte parametre til vurdering af nyrefunktionen og opretholdes selv i gruppen af patienter med normal glomerulær filtration. På nuværende tidspunkt vides det ikke præcist, om evnen til at forudsige en højere risiko for komplikationer skyldes, at cystatin C er en bedre markør for nyrefunktionen end andre almindelige parametre (serumkreatinin og glomerulær filtrationshastighed), eller om der er andre faktorer ud over glomerulær filtration, som påvirker cystatin C-koncentrationen og kan være direkte relateret til den kardiovaskulære risiko. I denne linje er der beskrevet en positiv korrelation mellem plasmaværdierne for C-reaktivt protein og fibrinogen med forhøjede cystatin C-koncentrationer og tilstedeværelsen af kardiovaskulær sygdom.30 I PRIME-undersøgelsen (Prospective Epidemiological Study of Myocardial Infarction) blev sammenhængen mellem cystatin C og udvikling af akut myokardieinfarkt hjertedød og angina pectoris undersøgt hos patienter uden koronar sygdom. Efter justering for de almindelige kardiovaskulære risikofaktorer var plasmacystatin C-niveauet signifikant forbundet med udvikling af den første koronarkomplikation af iskæmisk oprindelse. Forfatterne mente ikke, at den nedsatte glomerulære filtrationshastighed kunne retfærdiggøre de højere cystatin C-værdier, som tilfældene havde i forhold til kontrollerne, og de foreslog, at inflammation kunne være årsag til forholdet mellem cystatin C og risikoen for hjerte-kar-sygdomme31,32 . I overensstemmelse med disse data viste vores resultater en positiv korrelation mellem cystatin C og højfølsomt C-reaktivt protein (r=0,2), som også er en uafhængig prædiktor for kardiovaskulære komplikationer, og giver yderligere beviser for at retfærdiggøre tilstedeværelsen af direkte relationer mellem nyresygdom, inflammation og kardiovaskulær sygdom.
Men blandt de vigtigste begrænsninger i den præsenterede undersøgelse bør vi påpege, at resultaterne kun henviser til patienter med højrisiko-ACS indlagt på en hjerteintensivafdeling, hvoraf størstedelen blev aggressivt behandlet med tidlig koronarangiografi. På den anden side bør disse karakteristika fremhæves, fordi der kun findes få oplysninger om denne specifikke population, hos hvem cystatin C blev målt ved indlæggelsen på hospitalet. I næsten alle de offentliggjorte undersøgelser er tidspunktet for bestemmelserne ikke angivet, og i det mindste hos patienter med ACS kan plasmakoncentrationerne af cystatin C påvirkes af den tid, der er gået siden hændelsen, og af de diagnostiske og terapeutiske indgreb, der er foretaget. Begrænsningen med en kort opfølgning forhindrer en udvidelse af vores observationer til mellemlang eller lang sigt. Ikke desto mindre giver vores resultater mulighed for at forbedre risikostratificeringen hos patienter, der er indlagt for højrisiko-ACS, hvilket vil være nyttigt for beslutning om terapi såvel som for at fastslå diagnosen.
KONKLUSIONER
Cystatin C-bestemmelse på tidspunktet for indlæggelse på hospitalet hos patienter med højrisiko-ACS kan være et godt klinisk værktøj til stratificering af kardiovaskulær risiko. Bestemmelse af dette protein vil supplere de oplysninger, som andre metoder til vurdering af nyrefunktionen giver, og ud over de diagnostiske implikationer kan det være nyttigt til identifikation af gruppen med den højeste risiko. Det kan være nødvendigt at være særlig opmærksom på at opfylde anbefalingerne i retningslinjerne for klinisk praksis i denne population. Desuden kan cystatin C bidrage med vigtige oplysninger til stratificering af patienter med højrisiko-ACS og bevaret nyrefunktion. Der kan være behov for yderligere undersøgelser med en længere opfølgning for at definere cystatin C’s rolle i forbindelse med ACS med større præcision.
ABKORVIATIONER
ACS: akut koronarsyndrom
MDRD: Modification of Diet in Renal Disease
TpI: troponin I
