Indledning
Divertikulær sygdom i tyktarmen er den mest almindelige sygdom, der rammer tyktarmen i den vestlige verden. Prævalensen af divertikulær sygdom er steget i løbet af det sidste århundrede i hele verden, sandsynligvis på grund af ændringer i livsstilen, såsom rygning, overvægt og generelt fysisk inaktivitet og fiberfattig kost. Prævalensen stiger med alderen og varierer fra ca. 5 % hos voksne under 40 år til 50-70 % hos personer på 80 år eller derover. 80 % af de patienter, der får divertikulitis, er 50 år eller ældre. Divertikler kan forekomme i antal fra enkeltstående til hundreder, de er typisk 5-10 mm i diameter, men kan overstige 2 cm i størrelse. Divertikulose forekommer primært i sigmoideum og descendens colon hos mere end 90 % af patienterne, men kan være udbredt i varierende grad i resten af colon.1
Der er flere divertikulær-relaterede termer, som vil blive anvendt i denne gennemgang. Tilstedeværelsen af divertikler i colon i fravær af åbenlys inflammation kaldes divertikulose eller ukompliceret divertikelsygdom (UDD). Den kan være symptomatisk eller asymptomatisk. Udtrykket “akut divertikulitis i tyktarmen” (ACD) anvendes til at beskrive betændelse i divertiklerne, som kan udvikle sig til komplikationer (kompliceret ACD). Der findes også kronisk divertikulitis på grund af tilbagevendende divertikulitis eller på grund af udvikling af en segmental colitis i forbindelse med divertiklerne. Sammenfattende er det kliniske spektrum af divertikelsygdomme bredt.
Studier om sygdommens naturlige historie påpeger, at et stort flertal af patienterne med divertikler (ca. 80 %) forbliver asymptomatiske hele livet igennem. Af de 15-20 %, der udvikler symptomer, vil ca. 1/4 i sidste ende få en episode af symptomatisk smertefuld divertikelsygdom uden inflammation, og op til 10-25 % vil få en episode af ACD. Ca. 1-2 % vil kræve hospitalsindlæggelse og 0,5 % operation. Divertikler er ansvarlige for størstedelen (24-42%) af episoderne af nedre gastrointestinale blødninger.2-4
Fysiopatologi og symptomudvikling
Et divertikel i colon er en herniation af mucosa og submucosa, svarende til et svagt punkt, hvor vasa recti trænger ind i tunica muscularis. De patogenetiske mekanismer for divertikulær sygdom er stadig dårligt forstået, men det er generelt anerkendt, at de sandsynligvis er relateret til komplekse interaktioner mellem kost, koloniens mikrobiota, genetiske faktorer, koloniens motilitet og struktur, som resulterer i deres dannelse af koloniens divertikler over tid.5 Se fig. 1. I 1971 offentliggjorde Painter og Burkitt deres berømte hypotese om, at divertikelsygdomme skyldes overtryk i tyktarmen som følge af segmentering baseret på utilstrækkelig indtagelse af kostfibre. Som reaktion på det øgede intraluminale tryk kan der udvikles outpouchings, som kan stige frem på områder med potentiel svaghed.6 Stase eller obstruktion i det snævre divertikel kan føre til bakteriel overvækst og lokal vævsiskæmi, som i sidste ende fører til perforation.7 Siden da har talrige observationsundersøgelser forsøgt at påvise den mulige effekt af fibre på forebyggelse af divertikelsygdom. De fleste af dem konkluderede, at risikoen for UDD var omvendt forbundet med indtagelse af kostfibre.8-10 På baggrund af disse beviser anbefales en kost med højt fiberindhold til forebyggelse af divertikelsygdom i de fleste aktuelle retningslinjer og positionspapirer.11-15 Denne hypotese er imidlertid for nylig blevet udfordret, da: (1) den omvendte sammenhæng mellem fiberindtagelse og divertikulose er blevet draget i tvivl i nogle nyere epidemiologiske undersøgelser16,17 og (2) nye patogene hypoteser, såsom den neuropatiske og myopatiske hypotese, er ved at opstå.18-22 Andre faktorer, der er blevet forbundet med en øget risiko for divertikelsygdom, omfatter fysisk inaktivitet, forstoppelse, fedme og rygning23 .-27
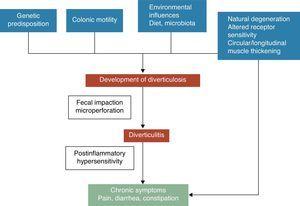
Symptomudvikling ved divertikulær sygdom er sandsynligvis relateret til komplekse interaktioner mellem genetiske træk, kolonstruktur, intestinal motilitet lav grad af inflammation og postinflammatorisk overfølsomhed.
Sammenhængen mellem ukompliceret divertikelsygdom (UDD) og symptomer er usikker. Der er noget, der tyder på, at smertefuld divertikulær sygdom kan være en tilstand, der er relateret til inflammation og dens virkninger på den neuromuskulære funktion i tyktarmen.22-28 Tilstedeværelsen af en kronisk, lavgradig tarminflammation ville inducere en sensorisk-motorisk dysfunktion, der fører til udvikling og/eller vedholdenhed af symptomer. Ændringer i tarmens mikroflora kunne være en af de formodede mekanismer, der er ansvarlige for lavgradsbetændelse. Bakteriel overvækst hjulpet af fækal stase inde i divertiklerne kunne bidrage til kronisk lavgradsinflammation, som sensibiliserer både intrinsiske primære efferente og extrinsiske primære afferente neuroner. Disse ændringer kan føre til hypertrofi af glatte muskler og øget følsomhed over for abdominal distension og endelig til udvikling af symptomer.3,22 Se fig. 1.
Som vi nævnte ovenfor, forbliver de fleste personer med divertikulose i tyktarmen asymptomatiske, men kan i sidste ende udvikle komplikationer som ACD eller divertikelblødning. I denne artikel fokuserer vi på ACD. Den kliniske manifestation af denne hændelse vil afhænge af en række faktorer, herunder perforationens størrelse, graden af ekstrakolonisk forurening og kroppens evne til at inddæmme denne forurening.29,30
Håndtering af divertikulær sygdomHåndtering af ukompliceret divertikulær sygdom (UDD)
Hos patienter med asymptomatisk UDD2 kan en fiberrig kost anbefales på grund af dens mulige profylaktiske fordel med hensyn til at forebygge symptomatisk UDD og komplikationer. Der er ingen dokumentation for, at andre lægemidler er nyttige hos disse patienter.
Der er mere dokumentation for fordelene ved behandling ved symptomatisk UDD. Det hyppigste symptom er mavesmerter, som kan forværres ved spisning og lindres ved defækation eller passage af flatus. Andre symptomer er kvalme, diarré, forstoppelse og oppustethed. Over 61 % af patienter med symptomatisk UDD, som ikke tager nogen terapeutisk foranstaltning for at forhindre gentagelse af symptomer, vil blive symptomatiske inden for 1 år, og ca. 4 % vil udvikle komplikationer.31
Fem midler er blevet foreslået til behandling (se fig. 2):

Behandling af ukompliceret divertikulær sygdom. Virkningsmekanismer.
A) Fiberrig kost eller bulking agents
Flere randomiserede kontrollerede forsøg (RCT) og andre interventionsstudier evaluerer effekten af fibre i symptomatisk UDD, men med inkonsistente resultater.32-37 Under alle omstændigheder anbefales fibre i forebyggelse og behandling af symptomatisk UDD samt i forebyggelse af ACD i de fleste af de nuværende retningslinjer og positionspapirer.11-15
B) Antibiotikabehandling
Rationalet for brugen af antibiotika ved symptomatisk UDD er ikke klart fastlagt. Nyere undersøgelser tyder på, at ændringer i tarmens mikrobiota (intestinal bakteriel overvækst) kan bidrage til udvikling af symptomer på grund af overdreven produktion af tarmgas gennem kulhydratfermentering. For at undgå systematiske virkninger synes dårligt absorberede antimikrobielle stoffer, der virker mod enteriske patogener, men som har minimal risiko for systematisk toksicitet eller bivirkninger, at være de mest hensigtsmæssige antibiotika. Rifaximin er blevet foreslået.
Rifaximin
Rifaximin er en ikke-systematisk rifamycinanalog med et bredt spektrum af aktivitet in vitro. Rifaximin kan nedsætte tarmfloraens metaboliske aktivitet, hvilket øger den fækale masse, og det kan også udrydde bakteriel overvækst. Dette antibiotikum har en høj sikkerheds- og tolerabilitetsprofil.33,38 Plasmaniveauet af rifaximin er minimalt, hvorfor ikke-enteriske patogener ikke udsættes for et selektivt pres, og risikoen for bakteriel resistens er lav.39 Tre åbne og to dobbeltblinde RCT’er40-44 har undersøgt effektiviteten af cyklisk administration af rifaximin og fibre i forhold til reduktion af symptomer sammenlignet med fibre alene. En systematisk gennemgang og to metaanalyser har analyseret disse forsøg.44-46 De konkluderede, at kombineret behandling er effektiv med hensyn til at opnå symptomlindring efter 1 år hos patienter med UDD. 35 % af de patienter, der blev behandlet med fibre alene, var asymptomatiske sammenlignet med 64 % i grupper med kombineret behandling. Det nødvendige antal behandlinger var tre for rifaximin vs. placebo for at lindre symptomlindring og ni for at undgå komplikationer. Sammenfattende har man opnået de bedste resultater ved at anvende en kombination af opløselige fibre, såsom glucomannan, og rifaximin 1 uge hver måned.
C) Probiotika
Probiotika er levende mikroorganismer, der kan genoprette den kommensale tarmflora, som kan være blevet ændret ved divertikelsygdom på grund af stase og nedsat kolontransittid.47 Desværre findes der kun få data om brugen heraf ved symptomatisk UDD, og de fleste af undersøgelserne er små og ukontrollerede. De fleste af dem viser symptomforbedring.48-50
Probiotika er også blevet undersøgt i kombination med 5-aminosalicylat (5-ASA). Tursi og kolleger har gennemført tre RCT’er, der sammenlignede 5-ASA alene, probiotika alene eller kombinationsbehandling.51-53 Både 5-ASA og probiotika syntes at være effektive til forebyggelse af symptomatisk UDD, men deres kombination var bedre. Et nyligt dobbeltbindet RCT offentliggjort af samme videnskabelige gruppe konkluderede, at både cyklisk mesalazin og Lactobacillus casei subsp DG, især i kombination, synes at være bedre end placebo til at opretholde remission af symptomatisk UDD.54 Men sammenfattende kan man sige, at de dårlige undersøgelsesdesigns og deres lille størrelse ikke tillader definitive konklusioner.
D) 5-ASA: mesalazin
Mesalazin har antiinflammatoriske og antioxidante virkninger. I 2010 offentliggjorde Gatta et al,55 en systematisk Cochrane-undersøgelse, der evaluerede 5-ASA’s rolle hos patienter med divertikelsygdom. Forfatterne konkluderede, at 5-ASA kan være effektiv i behandlingen af denne sygdom, og at daglig mesalazin var bedre end cyklisk administration til at forebygge tilbagefald. Der er behov for veltilrettelagte RCT’er af høj kvalitet for at bekræfte deres observationer. Faktisk viste det første placebokontrollerede dobbeltblindede forsøg, at mesalazin var effektivt til at opnå smertelindring hos patienter med akut UDD.56 Der er også to interessante RCT’er, der viste en fordel for mesalazin sammenlignet med rifaximin med hensyn til forebyggelse af symptomatisk recidiv og lignende succes med hensyn til at opretholde langvarig remission sammenlignet med det probiotiske Lactobacillus casei.53,57
E) Antikolinergiske/antispasmodiske midler
Den hipermotilitet i colon ved divertikulose tyder på, at antispasmodiske midler som dicyclomin og hyoscyamin kan forbedre symptomerne ved at mindske muskelsammentrækningen. Men der er ingen RCT’er, der bekræfter denne fordel.
F) Undgå NSAID-behandling
Flere kontrollerede undersøgelser har vist, at NSAID’er er en risikofaktor for udvikling af symptomer, ACD, perforation og blødning.7,58-60 NSAID-brugere har større risiko for at udvikle symptomatiske divertikelsygdomme end ikke-brugere (RR: 1,5, CI 95%: 1,1-2,1).58 Og hos patienter med komplicerede divertikelsygdomme var der et større forbrug af NSAID’er sammenlignet med kontroller uden sygdom. Det blev postuleret, at denne øgede risiko skyldtes slimhindebeskadigelse, der resulterede i nedsat barrierefunktion i colonslimhinden, hvilket muliggjorde translokation af bakterier, som fremkalder inflammation.
G) Niveauer af D-vitamin
Det ser ud til, at forekomsten af ACD har været forbundet med geografisk og sæsonbestemt variation. På grund af dette gennemførte Maguire et al. to interessante observationsstudier, der viste, at lavere niveauer af D-vitamin og lav UV-lyseksponering (UV-eksponering bestemmer D-vitaminstatus) er forbundet med en signifikant højere risiko for ACD. Der er behov for flere undersøgelser af høj kvalitet, før der kan gives en anbefaling.61,62
Behandling af akut divertikulitis i colonien (ACD)
Selv om de fleste personer med divertikulose forbliver asymptomatiske, anslås det, at ca. 10-25 % af dem vil udvikle en episode af venstre ACD.63 Generelt er den kliniske diagnose ikke tilstrækkelig præcis, og radiologiske teknikker er indiceret. Hos patienter med milde symptomer (de fleste) og uden tegn på kompliceret ACD kan kombinationen af smerter i venstre underliv, fravær af opkastning og et C-reaktivt protein >50mg/l være tilstrækkelig til at stille diagnosen.64,65 Hvis billeddannelse er indiceret, kan en betinget strategi med ultralyd som førstevalgsteknik og efterfulgt af computertomografi (CT), hvis ultralyd ikke er entydig eller tvivlsom, sandsynligvis repræsentere den mest effektive tilgang. Antallet af CT-undersøgelser kan reduceres med 50 %. I 1978 foreslog Hinchey et al. en klassifikation af ACD, som senere blev ændret.66,67 Der skelnes mellem fem stadier af ACD; stadie 0, klinisk mild divertikulitis, stadie I (a: perikolisk inflammation og b: abces
cm i nærheden af den primære inflammation), stadie II, intraabdominal, bækken- eller retroperitoneal abces eller abces fjernt fra den primære inflammation, stadie III, generaliseret purulent peritonitis og stadie IV, fækal peritonitis. Se fig. 3.

Algoritme til behandling af akut divertikulitis i colonien.
Behandling af ukompliceret ACD (Hinchey-stadie 0 eller Ia)
De fleste ukomplicerede ACD kan sikkert behandles konservativt med en succesrate på mellem 70 % og 100 %.14 Ambulant behandling kan give mulighed for betydelige omkostningsbesparelser for sundhedssystemerne. I tilfælde af ukompliceret ACD er kriterierne for stationær behandling betydelig inflammation (herunder tilstedeværelse af feber eller peritonitis), intolerance over for oral væske, alder over 80-85 år, immunosuppression eller alvorlige komorbiditeter. I de fleste tilfælde vil et kort hospitalsophold være tilstrækkeligt. Der er ingen dokumentation for, at diætrestriktioner har påvirket behandlingsresultaterne, selv om de fleste læger normalt anbefaler klar flydende kost.
En af de største nylige ændringer i behandlingen af ukompliceret ACD er den faldende brug af antibiotika. En nyere Cochrane-undersøgelse, der kun er baseret på en kvalitativ tilgang (uden metaanalyse), viste, at de bedste tilgængelige data ikke støtter rutinemæssig brug af antibiotika.68 Antibiotika hverken fremskynder helbredelsen eller forhindrer komplikationer eller tilbagefald. Derfor er brugen af antibiotika i dette tilfælde tvivlsom. Sandsynligvis ville de være hensigtsmæssige hos patienter med tegn på generaliseret infektion, tegn på septikæmi eller bakteriæmi og hos patienter med nedsat immunforsvar. Anbefalede behandlinger er baseret på klinisk konsensus. Der kan anvendes forskellige antibiotika, lige fra ampicilin til tredje generations cefalosporiner, så længe det er effektivt mod grampositive, gramnegative og anaerobe bakterier. Kombinationen af ciprofloxacin og metronidazol er sandsynligvis den mest ordinerede orale behandling. Hvis denne kombination tolereres dårligt, kan ampicilin-sulphabactam være et godt valg. På den anden side har nyere data vist, at der ikke er nogen fordele ved intravenøs frem for oral antibiotika og ved intravenøs 4 dages behandling frem for 7 dages behandling.69-71 Normalt observeres der klinisk forbedring inden for 3-4 dage efter behandlingen. Endelig anbefales indlæggelse på hospital med intravenøs antibiotika, når patienten ikke er i stand til at indtage føde oralt, er påvirket af alvorlig komorbiditet eller ikke forbedres ved ambulant behandling.
Behandling af kompliceret ACD (Hinchey-stadie Ib til IV)ACD Hinchey Ib eller II: abces
Omkring 15 % af patienterne med ACD vil udvikle en absces.67 Der er ingen evidens af høj kvalitet om den mest optimale behandling af ACD med abscesdannelse. Indlæggelse på hospital er indiceret. Størrelsen er en vigtig determinant for en vellykket behandling. Ved mindre abscesser (
cm) anbefales konservativ behandling med bredspektret antibiotika. Den vil være vellykket i op til 70 %.72 Når konservativ behandling mislykkes eller ved større abscesser bør der foretages perkutan drænage. Det lykkes i op til 80 %.73 Kirurgi vil være en redningsbehandling, når de tidligere nævnte behandlinger ikke virker.ACD Hinchey III eller IV: purulent eller fækal peritonitis
Peritonitis er den alvorligste komplikation med en dødelighed på 14 %. Selv om der ikke foreligger dokumentation, anses tidlig operation for at være standardbehandling for disse patienter. Valget af operation påvirkes af patientens forhold, operative fund og kirurgens erfaring. Hos kritisk syge patienter med hæmodynamisk ustabilitet anbefales Hartmann’s procedure. Hos hæmodynamisk stabile patienter må primær anastomose med eller uden proximal fækal afledning dog anses for at være at foretrække.14,74
Traditionelt anbefaler internationale retningslinjer, at der anvendes endoskopi efter en episode af ACD for at udelukke colorectal cancer. Denne anbefaling er kun baseret på ekspertudtalelser. Nylige retrospektive undersøgelser og en systematisk gennemgang75-80 viser, at kræftfrekvensen hos disse patienter er ret lav. På baggrund af denne nylige dokumentation kan den mest effektive strategi være at henvise til koloskopi kun de patienter med vedvarende symptomer eller patienter med mistænkelige CT-fund. Men der er behov for flere undersøgelser for at kunne give en fast anbefaling.
Håndtering efter en episode af ACDPrævention af tilbagevendende ACD
Efter en episode af ACD vil omkring en tredjedel få en anden ACD, og efter en anden episode vil yderligere en tredjedel få et nyt anfald.73,74 Men der er kun få beviser for at definere den optimale behandling efter en ACD-episode med henblik på at forebygge en ny episode.
A) Fiberrig kost
Når den akutte episode er overstået, anbefales almindeligvis en fiberrig kost for at reducere tilbagevendende episoder. Men RCT’er om fiberrige diæter hos patienter med ACD har haft inkonsistente resultater. En nyligt offentliggjort systematisk gennemgang af fiberrig kost kunne ikke omfatte nogen undersøgelse, der undersøger fibrenes rolle i forebyggelsen af tilbagevendende ACD.26,81 Nogle fødevarer (frø, popcorn og nødder) undgås klassisk set, fordi de teoretisk set kan trænge ind i, blokere eller irritere divertiklerne. Men Strate et al. fandt i deres store, prospektive undersøgelse ingen sammenhæng med en øget risiko for ACD. Derfor bør udelukkelse af disse fødevarer fra kosten ikke anbefales.82 Også vægtreduktion og rygestop kan have en gunstig indflydelse på forebyggelse af ACD.9,83
B) Antibiotika
Der er tre nyere systematiske oversigter, som har vurderet den rolle, som cyklisk rifaximin spiller i forebyggelsen af recidiv af ACD, men som ikke viste en klar fordel.46,84,85 Ud fra et patofysiologisk synspunkt kunne en plausibel forklaring på rifaximins ineffektivitet med hensyn til at forebygge recidiv være, at en cyklisk behandling muligvis ikke kontrollerer koloniens bakteriepopulation i en hel måned, fordi koloniens bakteriepopulation genopstår inden for 7-14 dage efter rifaximins ophør. Et nyligt spansk åbent RCT har imidlertid vist, at cyklisk rifaximin kan forbedre symptomerne og opretholde perioder med remission efter ACD.86 Der opstod recidiv hos 10,4 % af de patienter, der fik rifaximin plus fibre, sammenlignet med 19,3 % af de patienter, der fik fibre alene. Desuden havde patienter, der blev diagnosticeret første gang siden ≥1 år, en højere risiko for eksacerbation (OR 3,34, 95 % CI: 0,01-12,18). Men der er behov for yderligere undersøgelser, da der på nuværende tidspunkt ikke kan gives nogen anbefalinger. Der er ingen evidens for at støtte brugen af andre antibiotika i denne sammenhæng.
C) Probiotika
I nogle åbne undersøgelser er det undersøgt, hvilken rolle probiotika spiller i forebyggelsen af recidiv af ACD. Giaccari et al. evaluerede for mere end 20 år siden Lactobacillus sp. efter rifaximin hos 79 patienter med kolonstenose efter divertikulitis for 79 patienter. 88 % af patienterne forblev asymptomatiske i en periode på 12 måneder.87 Denne observationsundersøgelse var den første, der antydede en mulig rolle for probiotika i denne sammenhæng. En nyere undersøgelse evaluerede en kombineret behandling; balsalazid og VSL#3 (en probiotisk blanding af otte arter). Efter 12 måneder var 73 % af de personer, der fik kombinationsbehandling, asymptomatiske sammenlignet med 53 %, der fik probiotisk monoterapi (p>0,05).52 Sammenfattende synes probiotika at være effektive til at forebygge tilbagefald af ACD, men der mangler veltilrettelagte undersøgelser.
D) 5-ASA
Flere dobbeltblindede og åbne RCT’er har vurderet mesalazins rolle i forebyggelsen af tilbagefald af ACD. Desværre har de fleste af dem ikke fundet en fordel af mesalazin i forhold til placebo med hensyn til at forebygge tilbagefald.88-90 Raskin et al. har for nylig offentliggjort to interessante og identiske fase 3-dobbeltblindede, placebo-RCT’er (PREVENT1 og PREVENT2), der også viser, at mesalazin ikke er bedre end placebo med hensyn til at forebygge tilbagefald af ACD.91 Også den kombinerede behandling, 5-ASA plus rifaximin, er blevet evalueret i flere undersøgelser. Trivedi og Das gennemgik data fra fem RCT og en åben undersøgelse, der tilsammen omfattede over 600 patienter, og konkluderede, at kombinationen synes at være bedre end rifaximin alene til forebyggelse af recidiverende ACD.92
E) Kirurgi
Indtil for få år siden blev elektiv kirurgi anbefalet efter to anfald af ukompliceret ACD eller et anfald af kompliceret ACD for at reducere morbiditet og mortalitet ved recidiv. Men elektiv kirurgi indebærer også en øget risiko for morbi-mortalitet.93 Derfor er det vigtigt at afveje morbiditet og mortalitet som følge af kirurgi mod risikoen for komplicerede recidiv og symptomernes sværhedsgrad.
Nyere data viser, at naturhistorien for ACD er meget mere godartet, end man tidligere har troet.73,94 Den langsigtede risiko for tilbagefald er mere lavere end tidligere antaget, og de langsigtede risici for efterfølgende akut kirurgi (3-7 %), død (95 viste, at 16 % af tilfældene med første ACD blev akut opereret sammenlignet med kun 6 % i tilbagefaldstilfælde, og at 30-dages mortaliteten for første episode også var højere sammenlignet med tilbagefaldstilfælde (3 % vs. 0 %). Faktisk har størstedelen af de patienter, der præsenteres for kompliceret ACD, ingen sygdomshistorie.96 Det foreslås også, at tilbagevendende ACD kan beskytte mod perforation, muligvis på grund af adhæsionsdannelse forårsaget af inflammation.95 Derfor mindsker en politik med elektiv kirurgi efter ACD ikke sandsynligheden for yderligere operation (op til 3 %) og beskytter ikke fuldt ud mod tilbagefald. På den anden side har forbedret diagnostik og behandlingsmetoder reduceret morbi-mortaliteten ved kompliceret ACD. På grund af disse nye data anbefaler American Society of Colon and Rectum Surgeons i sin seneste retningslinje, at elektiv sigmoidresektion efter helbredelse af ACD bør foretages fra sag til sag14 og mener, at antallet af tidligere episoder ikke er en god indikator for udvælgelsen af kandidater til elektiv kirurgi. Lægerne bør tage hensyn til patientens helbredstilstand og alder, hyppigheden og sværhedsgraden af anfaldet/anfaldene og tilstedeværelsen af vedvarende symptomer efter den akutte episode.14
Det er meget vanskeligt at forudse, hvilke tilfælde af ACD der vil få tilbagefald. CT-gradueret sværhedsgrad af første episode af ACD synes at være en prædiktor for en ugunstig naturhistorie. ACD i venstre side, >5 cm af colon involveret og en retroperitoneal absces var prædiktorer for recidiv og skal tages i betragtning.97 Der er ikke enighed om, hvorvidt ung alder (82 Ifølge den nuværende evidens bør alder ikke betragtes som en indikation for elektiv kirurgi, da den ikke synes at være relateret til et alvorligt sygdomsforløb efter en medicinsk behandlet ACD. Men i betragtning af, at der er en øget forekomst af ACD hos yngre patienter, er det nødvendigt med yderligere undersøgelser for at afklare dette specifikke spørgsmål.
Særlige tilfælde er de immunsupprimerede personer. Kohortestudier viser, at disse patienter havde en høj risiko for kompliceret recidiverende ACD (en 5 gange større risiko for perforation) og en høj risiko for akut kirurgi.98 Derfor kan en lavere tærskel for elektiv kirurgi være til gavn for dem.14 Men Biondo et al. viser i deres nylige undersøgelse, at immunsupprimerede patienter havde en signifikant højere dødelighed, men kun i den første episode. Derfor er kontroversen til stede.99
Behandling af følgesygdommeA) Fistel
En fistel opstår, når en divertikulær flegma eller absces brister ind i et tilstødende organ. En fistel forekommer hos mindre end 5 % af patienterne med ACD. De hyppigste er kolovesikale og kolovaginale fistler. Formentlig vil en operativ resektion i en enkelt fase med lukning af fistlen og primær anastomose kunne udføres hos de fleste patienter. Andre fistler som koloenteriske eller coluterine fistler er sjældne.100,101
B) Obstruktion
Fremkaldende episoder af ACD, som kan være subkliniske, kan medføre kronisk forsnævring af colon uden igangværende inflammation. Der kan forekomme en høj grad eller fuldstændig obstruktion. Først og fremmest er det nødvendigt at behandle obstruktion for at udelukke en malign ætiologi. Når neoplasme er tilstrækkeligt udelukket, og der ikke er nogen ACD, kan endoskopisk dilatation eller midlertidig dekompression med metalstent være terapeutiske muligheder.102 Senere kan en efterfølgende enkeltfaset resektion uden diversion realiseres.
Behandling af segmental colitis associeret med divertikulose
Det defineres som en kronisk inflammation af interdivertikulær mucosa i et colonsegment involverer. Rektum og det højre colon er skånet. Det er blevet i en særskilt klinisk og patologisk lidelse og præsenterer sig ofte med blodig afføring. Patogenesen er ukendt. Spektret af histologiske forandringer spænder fra mild uspecifik inflammation til inflammatoriske tarmsygdomslignende forandringer. Derfor er differentialdiagnosen ofte vanskelig. De fleste patienter kommer sig fuldstændigt i løbet af få uger eller måneder. Nogle af dem behandles i første omgang med oral 5-ASA, men sandsynligvis er disse lægemidler ikke nødvendige, da de fleste tilfælde spontant forsvinder.103
Konklusioner
I symptomatisk UDD er formålet med behandlingen at forebygge komplikationer og reducere symptomerne. Ifølge den nuværende dokumentation synes fiber plus cyklisk rifaximin eller mesalazin plus probiotika at være de mest effektive behandlinger. I ACD synes antibiotika fortsat at være hovedhjørnestenen i behandlingen, og en ambulant behandling anses for at være den optimale tilgang for langt de fleste patienter med ukompliceret ACD. Indlæggelsesbehandling og intravenøs antibiotika er dog nødvendig ved kompliceret ACD. Akutkirurgiens rolle er i øjeblikket under forandring. De fleste diverticulitis-associerede abscesser kan behandles med intravenøs antibiotika og/eller perkutan drænage, og akut kirurgi vil kun blive betragtet som standardbehandling hos patienter med peritonitis. Endelig bør elektiv kirurgi efter helbredelse af ACD foretages fra sag til sag.
Autors bidrag
Gargallo CJ, Sopeña F og Lanas A bidrog ligeligt til udformningen, redigeringen, udarbejdelsen og gennemgangen af denne artikel.
Interessekonflikter
Dr. Carla J. Gargallo og Dr. Federico Sopeña rapporterer ikke interessekonflikter. Dr. Angel Lanas har været rådgiver for AlfaWasserman.
