Ioniske, kovalente (simple molekylære og kæmpestore atomare) og metalliske forbindelser har alle forskellige egenskaber. Derfor skal der for at klassificere et stof som en af disse forbindelser udføres en række forsøg/eksperimenter for at finde ud af, hvilke egenskaber det har. Se følgende tabel:
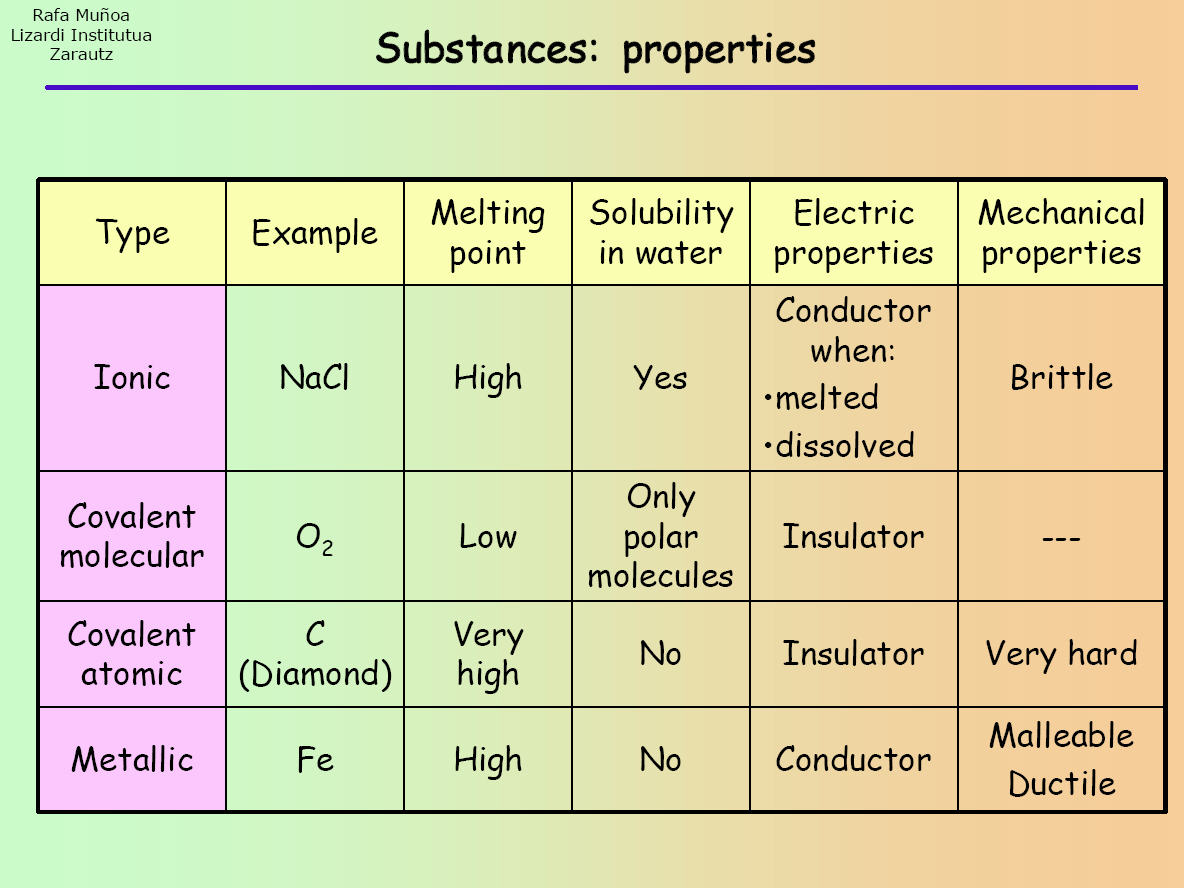
Når forsøget er udført, kan de resultater, du opnår, sammenlignes med dem i tabellen for at finde ud af, hvilken slags forbindelse stoffet er.
Først kan en prøve af det ukendte stof anbringes i et reagensglas og sættes over en flamme. Dette gøres for at bestemme smeltepunktet. Hvis stoffet smelter, er der sandsynligvis tale om et kovalent simpelt molekylært stof (som vist i tabellen). Hvis der derimod ikke sker nogen smeltning, kan stoffet enten være ionisk, kovalent kæmpestor atomart stof eller metallisk.
Det er egentlig derfor, at vi skal udføre mere end én test på det ukendte stof, fordi nogle kategorier af forbindelser har lignende egenskaber (f.eks. har ioniske forbindelser og kovalente forbindelser begge et højt smeltepunkt).
Næst kan du prøve at opløse noget af stoffet i vand (eller et andet polært opløsningsmiddel). Hvis det opløses, kan det være enten en ionisk eller en kovalent simpel molekylær forbindelse. Dine resultater fra det foregående og det næste forsøg vil hjælpe dig med at indsnævre dine resultater til kun én type forbindelse.
Næst kan du tilslutte prøven til et kredsløb som det nedenfor viste for at se, om den leder en elektrisk strøm.
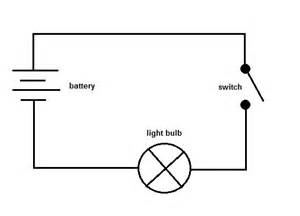
Du kan udskifte kontakten med prøven. Hvis pæren lyser, så er det en leder, og hvis ikke, så er det en ikke-leder.
Så hvis prøven ved slutningen af dette forsøg for eksempel ikke er smeltet, er opløst i vand og leder en elektrisk strøm, så er det en ionisk forbindelse.
Alle disse observationer kan forklares yderligere ved at undersøge de bindinger og intermolekylære tiltrækningskræfter, der holder komponenterne i en forbindelse sammen.
