- Methodologi
- Figur1:Imaging pathway
- Diagnostisk tilgang og indledende behandling
- Urincytologi
- Initial imaging in low-risk patients
- Figur2:Transitional-cell-carcinoma-of-the-bladder-(US)
- Figur3:Renalt overgangscellekarcinom (US og RPUG)
- Initial imaging in high-risk patients
- Figur4:Blære-og-nyre-TCC (CTU)
- Figur5:Blære-TCC (MRI)
- Figur6:Ureterisk TCC (CTU)
- Figur7:Blæretumor (cystoskopi)
- Andre billeddiagnostiske undersøgelser
- Klinisk opfølgning
- Tabel2: Indikationer for henvisning
Methodologi
En elektronisk søgning fra august-september 2015 i MEDLINE gennem PubMed og Cochrane Database of Systematic reviews identificerede relevante originale artikler, systematiske oversigter og evidensbaserede retningslinjer fra perioden 2008-september 2015, som blev inkluderet. Følgende termer blev anvendt i kombination under litteraturgennemgangen for at udarbejde listen over de gennemgåede artikler: “painless”, “macroscopic”, “visible” OG “haematuria”, “kidneys”, “ureters”, “urinary bladder”, “bladder cancer”, “urinary tract”, “cytology”, “diagnostic imaging”, “radiography”, “ultrasonography”, “ultrasonography”, “ultra sound”, “pyelography”, “tomografi, røntgenkomputeret” OG “urografi”, “magnetisk resonans” OG “urografi”, “intravenøs” ELLER “ekskretorisk” OG “urografi”, “urologi” ELLER “nefrologi” OG “henvisning” ELLER “konsultation”, “cystoskopi”, “retningslinjer”.
Der blev også foretaget en manuel søgning for at identificere andre relevante publikationer fra de fremkomne undersøgelser i forbindelse med gennemgangen. I alt 84 artikler i fuldtekst blev shortlistet og vurderet med henblik på støtteberettigelse. Artikler, der beskrev originale undersøgelser, evidensbaserede retningslinjer eller systematiske oversigter, blev inkluderet, mens pædiatriske undersøgelser og dyreforsøg blev udelukket. Artikler, der ikke var på engelsk, eller som havde begrænset tekst, blev også udelukket, hvorefter 59 endelige artikler blev inkluderet og klassificeret i henhold til Oxford Centre for Evidence-Based Medicine Levels of Evidence . De evidensbaserede vejledninger blev udarbejdet og gennemgået af DIP-redaktionens ekspertpanelmedlemmer (Diagnostic Imaging Pathways (DIP)) i overensstemmelse med de sædvanlige DIP-processer (http://www.imagingpathways.health.wa.gov.au/index.php/production/processes-for-creating-and-managing-content), i samråd med redaktøren, en urolog og en nefrolog. Den endelige algoritme (figur 1), som også er tilgængelig på Imaging Pathways (Online clinical decision-making tool: Dulku G. Painless Macroscopic Haematuria. Diagnostic Imaging Pathways; september 2015), giver vejledning og billeddannelsesanbefalinger for voksne patienter med uforklarlig, smertefri, synlig hæmaturi.
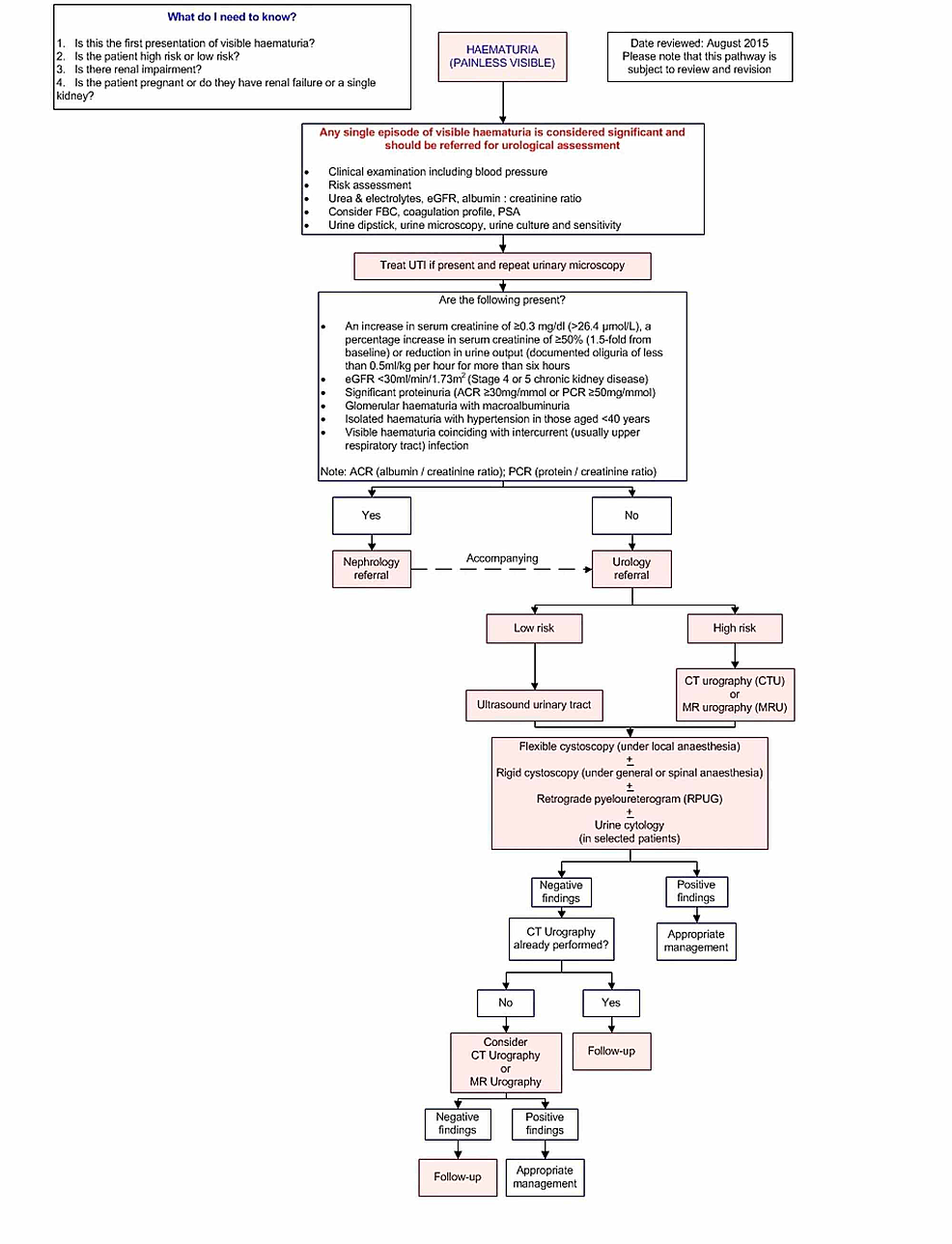
Figur1:Imaging pathway
Denne pathway giver vejledning om billeddannelse af voksne patienter med uforklarlig smertefri synlig hæmaturi.
eGFR: Estimeret glomerulær filtrationsrate; FBC: FBC: Fuldt blodbillede; PSA: Prostataspecifikt antigen; ACR: Albumin/kreatinin-forhold; PCR: PCR: UTI: Urinvejsinfektion.
Vores gennemgang omfattede ikke en analyse af billeddannelsesvejledning til påvisning af urinvejskalk som årsag til hæmaturi, da dette typisk er forbundet med smerter. Vores fokus var primært på den billeddannende vejledning og den understøttende litteratur for smertefri synlig hæmaturi med urologiske maligniteter som en mulig årsag.
Diagnostisk tilgang og indledende behandling
Konsensus fra British Association of Urological Surgeons (BAUS) og Interregional Chiefs of Urology Service (IRCUS), Kaiser Permanente, Amerika foreslog, at enhver enkelt episode af VH betragtes som signifikant og bør henvises til urologisk vurdering, som i næsten alle tilfælde vil omfatte cystoskopi .
I mellemtiden kan der foretages undersøgelser for at identificere forbigående, behandlelige årsager og sørge for primær billeddannelse. Patienter med VH og påvist urinvejsinfektion (UTI) bør stadig undersøges for samtidig malignitet, da malignitet ofte sameksisterer med eller fungerer som nidus for en infektion til at sprede sig fra . Urinvejsinfektion bør behandles før cystoskopi, da der er risiko for uro-sepsis, hvis cystoskopi udføres i tilstedeværelse af aktiv UTI.
Forekomsten af VH bør heller ikke tilskrives antikoagulerende eller trombocythæmmende behandling, og disse patienter bør også evalueres uanset disse medikamenter, da rapporter om underliggende malignitet blev fundet hos 24 % og 7 % af patienterne i to separate serier .
Derfor er billeddannelsens primære rolle at identificere de patienter med en malign årsag til hæmaturi. Valget af billeddannelsesmodalitet afhænger imidlertid af forskellige individuelle patientfaktorer (f.eks. alder, risikofaktorer for malignitet, nyrefunktion og graviditet) og andre faktorer, såsom lokal politik og praksis, omkostningseffektivitet og tilgængelighed af ressourcer .
Traditionelt har førstelinjeundersøgelser omfattet konventionel radiografi, renal ultralyd (US) og/eller intravenøst pyelogram (IVP) i kombination med cystoskopi .
Traditionelt har førstelinjeundersøgelser omfattet konventionel radiografi, renal ultralyd (US) og/eller intravenøst pyelogram (IVP) i kombination med cystoskopi. Sidstnævnte er vigtigt, da mange blødende urinvejslæsioner opstår i urinblæren, og det er endnu ikke endeligt bevist, at billeddannelsesprocedurer er lige så følsomme som cystoskopi til at diagnosticere de fleste af dem .
Second-line undersøgelser har omfattet multi-detector computed tomography urogram (MDCTU) og magnetisk resonans urografi (MRU), der ofte kun udføres, hvis de førstelinjede undersøgelser afslører en abnormitet.
IRCUS har anbefalet, at der udføres en modificeret CTU eller IVP med samtidig renal US til patienter med betydelig hæmaturi. Der er ikke behov for nyretomografi ved intravenøs urografi (IVU), hvis der udføres en samtidig renal US. Denne fremgangsmåde vil reducere eksponeringen for ioniserende stråling .
Ved anbefaling af billeddannelse til evaluering af VH havde Cowan foreslået, at den anvendte type billeddannelsesmodalitet skulle baseres på en risikoscore, hvor patienter >40 år skulle gennemgå CT-urografi, mens patienter <40 år skulle gennemgå ultralyd som den første billeddannelsesmodalitet . European Society of Urogenital Radiology (ESUR) har foreslået, at udredning af lavrisikopatienter kræver ultralyd og cystoskopi, mens højrisikopatienter kræver CTU og cystoskopi med henblik på grundig billeddannelse af nyrer og urinveje .
Urincytologi
Urincytologi er, selv om det er kontroversielt, afgørende for vurderingen af urothelialcellekarcinom i de øvre urinveje (UUT-UCC), og retningslinjerne fra European Association of Urology (EAU) anbefaler, at urincytologi bør udføres som en del af den diagnostiske standardundersøgelse . Urincytologi har en sensitivitet på 25 %, en specificitet på 91 %, en høj positiv prædiktiv værdi, men en lav negativ prædiktiv værdi .
Urincytologi har imidlertid en høj falsk negativ rate for påvisning af malignitet, og en negativ cytologi kan aldrig helt udelukke tilstedeværelsen af en blæretumor, cystoskopi er berettiget i alle tilfælde.
Numre kommercielt tilgængelige urinprøver for urinbårne biomarkører omfatter BTA TRAK, ImmunoCyt/uCyt+, CxBladder, Nuclear Matrix Protein 22 (NMP-22) og UroVysion (FISH), selv om disse kan gå glip af en betydelig andel af patienter med blærekræft, især når dens nøjagtighed er dårlig for lavstadie- og lavgrads-tumorer . Af disse grunde blev der ikke opnået konsensus om den rolle, som urincytologi og/eller blæretumormarkører spiller i vurderingen af patienter med hæmaturi .
Initial imaging in low-risk patients
ESUR havde foreslået, at undersøgelsen af lavrisikopatienter kræver US og cystoskopi, og højrisikopatienter kræver CTU og cystoskopi for grundig nyre- og urinvejsvurdering . US’s følsomhed er imidlertid ikke tilstrækkelig til at overflødiggøre behovet for cystoskopi på grund af dens manglende følsomhed i forbindelse med påvisning af små blæretumorer, især dem, der er mindre end 0,5 cm i diameter .
Ultrasound (US) er vigtig i den indledende vurdering af hæmaturi, og ud over at være let tilgængelig og billig, indebærer den ingen eksponering for ioniserende stråling og er især nyttig i strålefølsomme befolkningsgrupper, såsom børn og gravide eller kvinder i den fødedygtige alder. Ultralyd giver også mulighed for ubegrænsede scanningsniveauer, hvilket giver en god visualisering af nyrerne og urinblæren. Desuden kan Dopplerundersøgelser give yderligere oplysninger om massernes vaskularitet (figur 2A, 2B) .
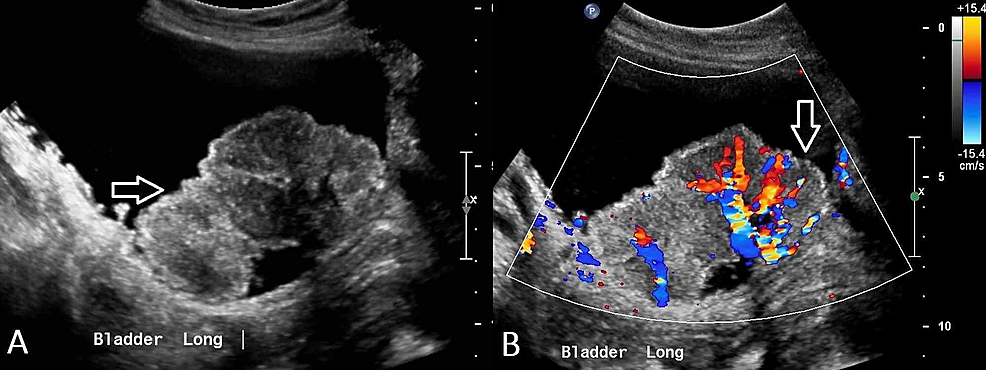
Figur2:Transitional-cell-carcinoma-of-the-bladder-(US)
(A) Ultralydsbassin viser en uregelmæssig, heterogen inden for urinblæren med flere mindre polypoide læsioner set ved siden af, hvilket tyder på urinblærekræft. (B) Vaskularitet påvises inden for denne masse.
Ved påvisning af UUT-tumorer har US en varierende sensitivitet ved påvisning af urothelkarcinomer, med moderat sensitivitet (82 %) for påvisning af nyrecellekarcinom og lav sensitivitet (12 %) for påvisning af urothelkarcinom i urinlederen . Men sammenlignet med IVP til påvisning af abnormiteter i UUT hos patienter med hæmaturi er US mere følsomt til påvisning af nyre- og blæretumorer , med en højere sensitivitet (96 % mod 25 %) og en højere negativ prædiktiv værdi (98 % mod 91 %) .
Dertil kommer, at US også er nyttig til påvisning af hydronefrose og/eller hydroureter, som kan være en følge af blæretumorer, der obstruerer vesicoureterisk junktion (figur 3). Ikke desto mindre har US sammenlignet med tværsnitsbilleder som MDCTU eller MRU en lavere sensitivitet til påvisning af urinvejsanormaliteter.
Ultrasound er fremragende til at afgøre, om en masse er cystisk eller ej, og om en cystisk læsion er en simpel cyste eller minimalt kompliceret eller kompliceret. Læsioner, der ikke er simple cyster, kræver yderligere udredning med CT eller MRI. Kontrastforstærket US (CEUS) er et lovende alternativ til den indledende undersøgelse af nyremasser. De rapporterede resultater af CEUS ved vurdering af formodede solide eller komplekse cystiske masser tyder på en tilsvarende værdi af CEUS sammenlignet med CT. CEUS har fordele som manglende nefrotoksicitet, ingen ioniserende stråling og mulighed for at evaluere forstærkningsmønsteret i realtid – og dette kan gøres ved den indledende US-undersøgelse af patienten. Der er dog behov for yderligere afklaring af CEUS’ plads i den diagnostiske algoritme.
Det synes derfor berettiget at anvende US som en billeddannelsesmodalitet i første linje ved vurdering af hæmaturi . I betragtning af at ultralyd alene potentielt kan overse ureter- og urothellæsioner, er yderligere evaluering med cystoskopi nødvendig, mens retrograd pyelo-ureterografi er et nyttigt supplement (Figur 3) .
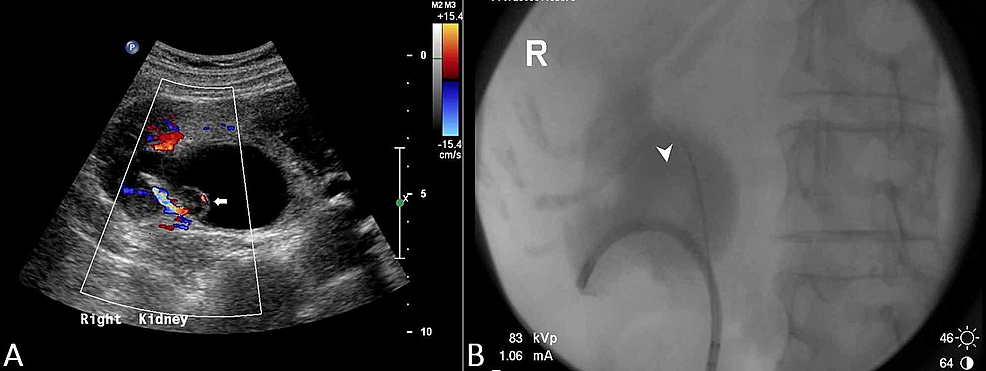
Figur3:Renalt overgangscellekarcinom (US og RPUG)
(A) Ultralydsbassin viser en diffust fortykket proximal højre ureter med en papillær læsion (pil) set inden for det højre nyrebækken og deraf følgende højre hydronefrose. (B) Dette svarer til de retrograde pyelo-ureterogrammer (RPUG) (pilespids), som tyder på et obstruerende højre øvre urinvejs overgangscellekarcinom i de øvre urinveje.
Initial imaging in high-risk patients
CT Urography
CT urography (også kaldet CT IVP selvom CTU er den foretrukne betegnelse) udkonkurrerer US, IVU, og radiografi ved vurdering af nyreparenkym-masser og urinvejskalk med en sensitivitet og specificitet for maligniteter i de øvre urinveje på henholdsvis 67-100 % og 93-99 % .
Den optimale diagnostiske strategi til udredning af patienter med høj risiko efter udelukkelse af UTI er en kombineret strategi med CTU og fleksibel cystoskopi . Patienter’ med læsioner, der er forenelige med blærekræft på CTU, bør henvises direkte til rigid cystoskopi og dermed undgå fleksibel cystoskopi med en fordel på en 17 % reduktion i antallet af udførte fleksible cystoskopier .
For alle andre patientkategorier, herunder yngre patienter og patienter med mere benigne indikationer og lavere sandsynlighed for kræft før test, er US den billeddannende modalitet i første række . CT-urografiundersøgelsesteknikmodifikationer, der består af begrænsede protokoller og scanningsfasekombinationer, kan anvendes alternativt eller som supplement til de andre billeddannende undersøgelser .
Scanningsprotokollen bør omfatte: ikke-kontrastscanning, nefrografisk (90-100 sekunder efter kontrastbolus) og ekskretionsfase (eller pyelografisk fase) (5-15 minutter efter kontrasttilførsel) . En kortiko-medullær fase er nyttig i udvalgte tilfælde, f.eks. hvis der er mistanke om pseudoaneurysme eller pseudotumor. Rutinemæssig registrering i denne fase kan ikke nødvendigvis være berettiget . De ikke-kontrastfyldte billeder er nyttige til påvisning af renal calculus. Den nefrografiske fase har den højeste følsomhed ved påvisning af nyremasser, og der kræves korrelation med uforstærkede billeder for at påvise entydig forstærkning. Den pyelografiske/ekskretoriske fase anvendes til at vurdere det opsamlende system, urinlederne og blæren med anvendelse af ureterdistensionsteknikker som f.eks. kompression, intravenøs saltvandsbolus og diuretika, der alle giver varierende resultater. CT-urografi kan også påvise ekstraurinær sygdom .
I modsætning til urotheliale tumorer forbliver mange patienter med renal malignitet asymptomatiske indtil sene stadier af sygdommen, da langt de fleste nyrekræftformer er små og opdages tilfældigt. Desuden invaderer nyremasser sjældent ind i det opsamlende system. Derfor forekommer den klassiske triade af flankesmerter, hæmaturi og en palperbar abdominal nyremasse ved nyrecellecarcinom (RCC) højst hos 6-9 % af patienterne, og når den er til stede, tyder den stærkt på lokalt fremskreden sygdom og dårlig prognose. Her anbefales CT og MRT hver især til udredning og betragtes som ligeværdige til stadieinddeling og diagnose (figur 4 og 5) . Der afventes dog sammenlignende undersøgelser mellem CT og højfelt-MRI. I mellemtiden kan MRI anvendes i udvalgte tilfælde til problemløsning. Diffusionsvægtet MRI (DWI) kan også være nyttig til påvisning og karakterisering af læsioner, men systematiske undersøgelser viser kun en moderat nøjagtighed .
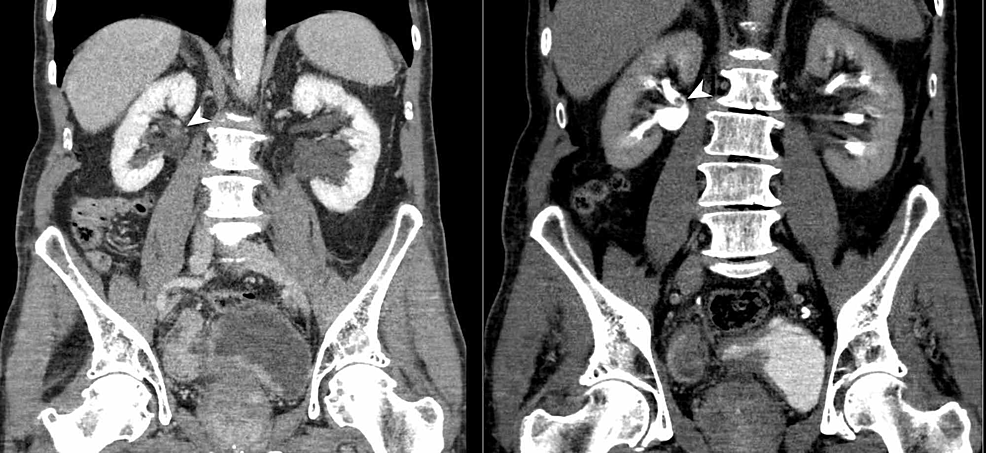
Figur4:Blære-og-nyre-TCC (CTU)
CT-urografi (koronal reformat) viser uregelmæssig fortykkelse af urinblærevæggen og også en sessil polypoid fyldningsdefekt i det bageste aspekt af det højre nyrebækken (pilhoveder). Resultaterne tyder på multifokalt urinvejsovergangscellekarcinom (TCC).
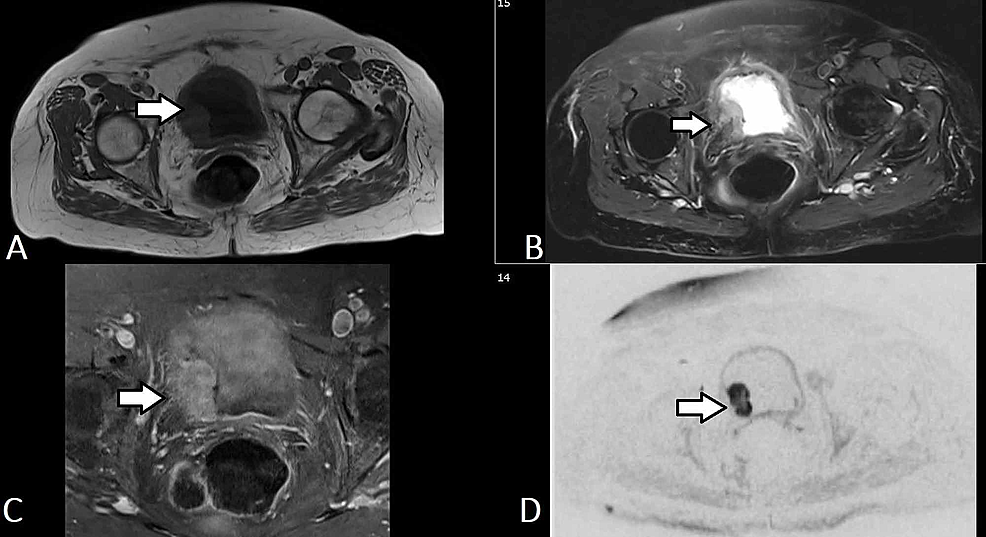
Figur5:Blære-TCC (MRI)
(A-D) Udvalgte aksiale MR-urografibilleder af samme patient viser en lobulær masse (pil), der udgår fra urinblærens højre laterale væg, som strækker sig til trigonen og invaderer ind i urinblærevæggen for at involvere det ydre lag uden udvidelse ind i det perivesikale fedt. Massen har lav T1-signalintensitet og høj T2-signalintensitet. Massen udviser en relativt homogen, diffus kontrastforstærkning og en markant diffusionsbegrænsning (b50/400/800). Konstellationen af fund afspejler en blæretumor, der sandsynligvis klassificeres som T2b No Mx.
TCC: Transitional Cell Carcinoma
Bosniak-klassifikationen af cystiske nyremasser er baseret på billeddannende karakteristika på kontrastforstærket CT, og den er nyttig til at forudsige risikoen for malignitet og til at give vejledning i behandlingen. Risikoen for malignitet for Bosniak 1, 2, 2F, 3 og 4 cystiske læsioner er henholdsvis 0 %, 0 %, 25 %, 54 % og 100 % .
CT-urografi kan også være effektiv ved diagnosticering af blæretumorer. Resultaterne kan dog variere afhængigt af den specifikke population, der undersøges. I højrisikogruppen var utvetydige CTU-resultater 93 % følsomme og 99 % specifikke for påvisning af blærekræft med en samlet negativ prædiktiv værdi (NPV) på 95 %. Den høje NPV af CTU kan overflødiggøre cystoskopi hos disse udvalgte patienter, selv om cystoskopi fortsat er den gyldne standard til påvisning af tumorer i de nedre urinveje, herunder urotheliale tumorer i blæren, da hverken IVP eller MDCTU konsekvent har en sensitivitet, der er signifikant nok til at udelukke blæreslimhindeanomalier .
Stråledoserne er et problem ved MDCTU, og dette kan reduceres ved at begrænse antallet af billeddannelsesfaser ved hjælp af dual-energy CT (DECT) eller split-bolus-teknik . Desuden (25) resulterer udeladelse af den ikke-forbedrede erhvervelse i en reduktion af stråleeksponeringen med næsten 50 % .
DECT giver oplysninger om, hvordan stoffer opfører sig ved forskellige energier, mulighed for at generere virtuelle ikke-forbedrede datasæt og forbedret påvisning af jodholdige stoffer på lav-energibilleder . Andre fordele ved DECT omfatter god tidsmæssig og rumlig registrering og god spektral adskillelse mellem høj- og lavenergiskanninger let at udligne dosis og støj . En prospektiv undersøgelse viste, at DECT-urografi i en enkelt fase med synkron nefrografisk ekretionsfaseforstærkning udgør en præcis “alt-i-en”-tilgang med en strålingsdosisbesparelse på op til 45 % sammenlignet med en standardprotokol med to faser med god opakificering i 86 .9 % af tilfældene og fremragende eller gode virtuelle uforstærkede (VUE) billeder i 83,3 % af tilfældene .
På den anden side giver split-bolus MDCTU mindst 50 % opakificering af de fleste UUT-segmenter med en høj følsomhed (88.9-100%), specificitet (99-99,5%) og nøjagtighed (98,5-99,5%) til påvisning af tumorer i de øvre urinveje (Figur 6) .
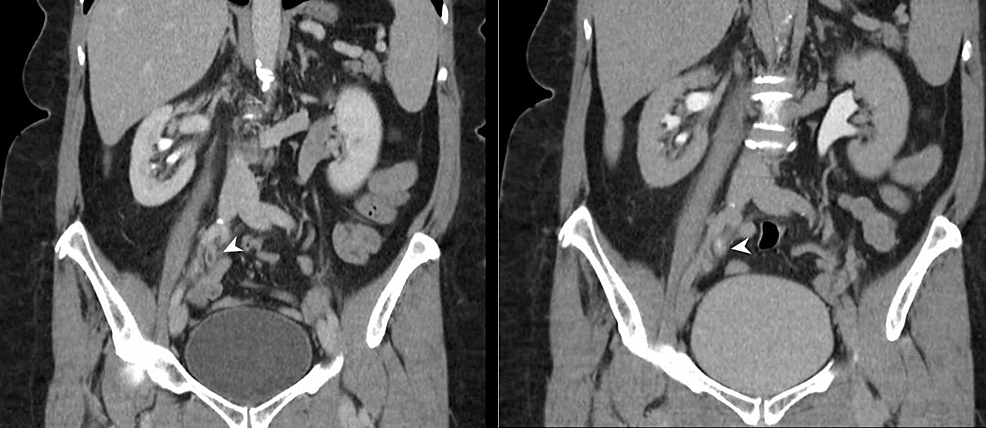
Figur6:Ureterisk TCC (CTU)
CT-urografi (koronale reformater) viser et 4 cm segment med cirkumferentiel urothelfortykkelse ved krydset mellem den midterste og distale højre ureter (pilhoveder) med unormal urothelforstærkning. Der er sekundær obstruktion af det højre opsamlingssystem med overgangspunktet på niveauet af den unormale urotheliale fortykkelse, hvilket er yderst mistænkeligt for en højresidig urothelial TCC.
TCC: Transitional Cell Carcinoma
Magnetisk Resonans Urografi
Magnetisk resonansbilleddannelse er nyttig ved diagnosticering og stadieinddeling af maligniteter i nyrer, blære og prostata og ved vurdering af nyrefunktionen. Det er en alternativ billeddannelsesteknik for strålefølsomme personer, herunder børn og gravide, personer, der har brug for gentagne undersøgelser af urinvejene, og personer med kontraindikation for jodholdige kontrastmidler.
En komplet MRU-protokol kan anvendes til billeddannelse af alle komponenter i nyrerne og urinopsamlingssystemet i en enkelt billeddannelsessession. MR-urografi udføres ved hjælp af to hovedmetoder: statisk-væskeurografi med ultrahurtige T2-vægtede sekvenser, svarende til den, der anvendes til magnetisk resonans-kolangiopancreatografi (MRCP), og T1-vægtede sekvenser af udskillelsesurografi efter IV-gadoliniumkontrastadministration .
Statisk-fluid MRU foretrækkes frem for ekskretorisk MRU ved billeddannelse af patienter med nedsat nyrefunktion, gravide patienter og patienter med ureterobstruktion, især når der er en rimelig risiko for nefrogen systemisk fibrose . Da de T2-vægtede sekvenser imidlertid udføres uden IV-kontrasttilførsel, er det ofte nødvendigt at foretage billeddannelsesmodifikationer for at optimere ureterisk billeddannelse.
Ureterisk billeddannelse kan også forbedres, især ved excretorisk MRU, efter indgivelse af IV-kontrastmateriale, saltopløsning og et diuretikum for at opnå en mere ensartet kontrastfordeling . Selv om beviserne viser, at DWI kun udviser moderat nøjagtighed med hensyn til forudsigelse af renal malignitet, er dens ydeevne som en uafhængig test stadig ikke testet . Tilføjelse af DWI til T1- og T2-vægtet billeddannelse øger følsomheden ved identifikation af UUT-kræft med fremragende overensstemmelse mellem observatørerne. Især kombinationen af T2WI+DWI viser følsomheder på mellem 92-98 % for diagnosticering af blæretumorer (figur 5).
Ulemperne ved MRU omfatter omkostninger, tilgængelighed, længere anskaffelsestid, billedforringelse på grund af bevægelsesartefakter, lavere rumlig opløsning og diagnostisk sikkerhed i forbindelse med påvisning af urothelial malignitet sammenlignet med CTU. Udviklingen af hurtigere sekvenser og optimering af 3-T MRI-protokoller forventes dog at løse disse problemer .
Cystoskopi
Cystoskopi er stadig den foretrukne metode til evaluering af urinblæren og bør ikke erstattes af nogen ekskretorisk billeddannelsesteknik . De seneste EAU-retningslinjer anbefaler også, at cystoskopi bør udføres for at udelukke en sideløbende blæretumor (figur 7), når UUT-kræft er diagnosticeret, især når forfattere har påvist bemærkelsesværdige falsk-positive og falsk-negative resultater ved CTU og MRU i forbindelse med påvisning af blæretumorer sammenlignet med histopatologi hos patienter med synlig hæmaturi . Der bør foretages en cystoskopi på stort set alle patienter med smertefri synlig hæmaturi .
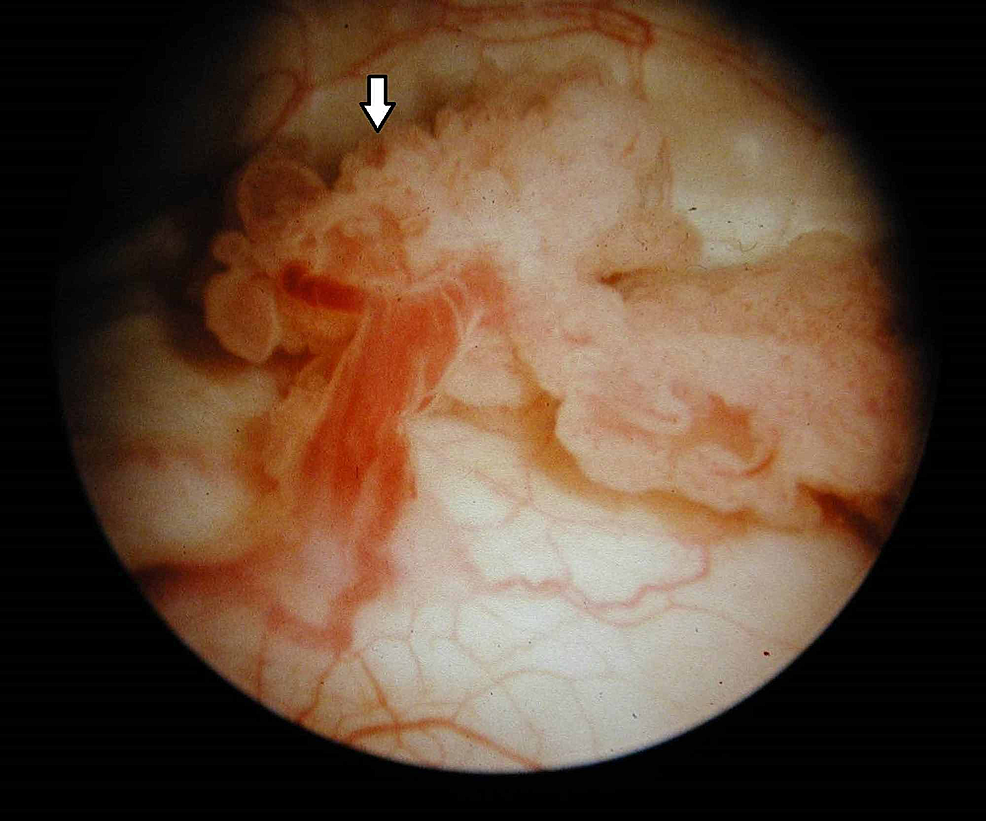
Figur7:Blæretumor (cystoskopi)
Cystoskopi afslører en exophytisk, blomkålslignende vækst med sarte blade og områder med ulceration i overensstemmelse med en malignitet i urinblæren (pil).
Fleksibel cystoskopi er en enkel, hurtig og sikker procedure, der udføres under lokalbedøvelse som et dagtilfælde med pålidelig beroligelse og giver mulighed for, at operative patienter kan diagnosticeres og forberedes til deres operation i samme besøg .
På den anden side udføres rigid cystoskopi under generel eller rygmarvsbedøvelse, især når der forventes mere komplekse yderligere procedurer. Et retrograd pyelo-ureterogram (RPUG) kan udføres på tidspunktet for rigid cystoskopi for at afbilde de øvre kanaler, hvis CTU ikke allerede er blevet udført .
Andre billeddiagnostiske undersøgelser
Retrograd pyelo-ureterografi
CT urogram har vist sig at have en større diagnostisk nøjagtighed end RPUG til påvisning af urothellæsioner . Derfor er det berettiget, at CTU bør anvendes før RP, som en enkelt, ikke-invasiv og omfattende test, der muliggør samtidig diagnose og/eller stadieinddeling.
Retrograd pyelografi kan stadig anvendes som en second-line undersøgelse for yderligere at karakterisere fyldningsdefekter, der er påvist på andre modaliteter, ikke-diagnostisk CTU, eller hos patienter med nyresvigt eller tilfælde af kontrastmiddelallergi. Retrograd pyelo-ureterografi kan kun vise ureterens lumen og kan ikke direkte afbilde extrinsiske abnormiteter (Figur 3) .
Plain Radiography of the Kidneys, Ureters and Urinary Bladder (Plain X-ray KUB)
Plain X-ray KUB er i øjeblikket af ringe værdi i udredning af patienter med smertefri hæmaturi og anvendes ikke som første linje billedmodalitet .
Excretory Urography/Intravenous Urography (IVU)
Intravenous urography er et godt valg til vurdering af urothelial og intraluminal sygdom, men er ikke tilstrækkeligt følsom til at påvise nyremasser <2-3 cm i størrelse og er nu blevet erstattet af CTU til billeddannelse af UUT . Undersøgelse af hæmaturi hos højrisikopatienter med IVU alene anbefales ikke længere .
Den største fordel er, at IVU afbilder hele UUT med en høj grad af rumlig opløsning og også giver strukturelle oplysninger samt begrænsede funktionelle data. Det er ofte den mest omkostningseffektive test i mange centre .
Hvorimod ulemperne ved IVU omfatter lang anskaffelsestid, potentielle farlige kontrastreaktioner, der kræver tarmforberedelse og eksponering for en mærkbar strålingsbelastning. Dens relative unøjagtighed er dens største mangel og vil snart være forældet .
Klinisk opfølgning
Der er en risiko for, at 1-3% af patienterne med en negativ udredning udvikler malignitet inden for tre år, hvis de ikke kontrolleres . American Urological Association (AUA) best policy panel anbefaler, at læger i primærsektoren kontrollerer for VH, nye urinsymptomer og positiv cytologi hver sjette måned i tre år, og hvis resultaterne er konsekvent negative på det tidspunkt, kan opfølgningen ophøre . BAUS anbefaler, at det er nødvendigt at genhenvise til urologi, hvis der udvikles VH eller symptomatisk ikke-synlig hæmaturi (NVH) i løbet af den primære opfølgning, hvis varighed ikke er klart defineret . Best Practice Advocacy Centre New Zealand har anbefalet årlig overvågning af nefrologiske årsager med urinprøve, blodtryk, eGFR og urinalbumin/kreatinin-forholdet/protein/kreatinin-forholdet (ACR/PCR), så længe der fortsat er hæmaturi, og årligt i to år for urologiske årsager med urinprøve, eGFR, urin-ACR/PCR og cytologi. Dette initiativ gør det muligt at foretage en opfølgning i primærsektoren for at berolige patienter, der er bekymrede over vedvarende hæmaturi, som kan være intermitterende, men vedvarende på trods af en negativ undersøgelse. Indikationen for henvisning til nefrologi og urologi er opsummeret i tabel 2 .
Reference til nefrologi
En stigning i serumkreatinin på ≥0.3 mg/dl (>26,4 µmol/L), en procentvis stigning i serumkreatinin på ≥50 % (1,5 gange fra baseline) eller nedsættelse af urinproduktionen (dokumenteret oliguri på mindre end 0.5 ml/kg pr. time i mere end seks timer
Signifikant proteinuri (ACR ≥30 mg/mmol eller PCR ≥50 mg/mmol) i tillæg til hæmaturi giver mistanke om intrinsisk nyresygdom
Glomerulær hæmaturi med makroalbuminuri
Isoleret hæmaturi (dvs, i fravær af signifikant proteinuri) med hypertension hos personer i alderen <40 år
Synlig hæmaturi sammenfaldende med interkurrent (sædvanligvis øvre luftveje) infektion
Urologisk henvisning
Synlig hæmaturi hos alle patienter (uanset alder)
Patienter med enhver symptomatisk ikkesynlig hæmaturi i fravær af urinvejsinfektion eller andre forbigående årsager (uanset alder)
Mandlige patienter med asymptomatisk ikke-synlig hæmaturi
Alle patienter med asymptomatisk ikke-synlig hæmaturi og andre risikofaktorer
Tabel2: Indikationer for henvisning
† Tilstedeværelsen af dysmorfiske røde blodlegemer, proteinuri, cellulære afstøbninger og/eller nyreinsufficiens eller enhver anden klinisk indikator, der er mistænkelig for nyreparenkym-sygdom, berettiger samtidig nefrologisk udredning, men udelukker ikke behovet for urologisk vurdering.
‡ Kvinder med asymptomatisk ikke-synlig hæmaturi i alderen <40 år kræver ikke henvisning til urologi.
