Uteruscirkulationen er yderst følsom over for østrogenstimulering og reagerer med en grad af vasodilatation, som intet andet organ i kroppen kan sammenligne med nogen anden stimulus.2 Under ovariecyklussen forekommer gentagne mønstre af UBF, der afspejler effekten af østrogenudskillelse og de modulerende virkninger af progesteron. Disse cykliske mønstre viser sig mest dramatisk hos dyr med korte præovulatoriske cyklusfaser, såsom koen, soen og moderfåret, og er illustreret i figur 1 med perifere niveauer af østrogen og progesteron.3, 4, 5 Efter befrugtningen hos disse arter ligner UBF-mønstrene dem hos ikke-graviditetsdyr, indtil der 17 til 28 dage senere sker en interdigitering af moder- og fostervævet; derefter sker der en definitiv og progressiv stigning i UBF, der fortsætter indtil terminaldræning. Da erosion af endometrium af føtal trophoblast sker meget tidligere efter undfangelsen hos primater, er det rimeligt at formode, at UBF stiger tidligere hos disse arter, selv om sådanne reaktioner aldrig er blevet observeret. De overordnede mønstre for den samlede UBF, UBF pr. vægtenhed af uterus og dets indhold, den del af UBF, der forsyner placentaen, og fostervægten i løbet af hele fåredrætsforløbet er illustreret i figur 2. Perioden mellem 17 og 70 dage af drægtigheden er forbundet med de hurtigste ændringer i UBF og PBF og svarer til tidspunktet for den endelige placentation hos denne art. Ved hjælp af mekanismer, der er ufuldstændigt forstået, udvides de blodkar, der forsyner placentaen, gradvist i denne periode, hvilket samtidig forårsager en absolut stigning i den samlede UBF og en shunting af dette blod fra ikke-placentale til placentavæv.* Med den efterfølgende placentamodning øges den del af UBF, der forsyner placentaen, og den absolutte mængde PBF, men med hastigheder, der mere ligner væksten af fosteret; i den sidste halvdel af drægtigheden er UBF pr. vægtenhed af uterus og dets indhold således stort set konstant. I samme periode er den mængde ilt, der udvindes fra hver milliliter blod, konstant, og derfor er den mængde ilt, der leveres pr. given vægt af gravid uterus, også konstant.6 Korrelative undersøgelser hos kvinder viser lignende homøostatiske mønstre fra 10 til 40 uger af graviditeten og et lignende iltforbrug (ca. 10 ml/kg).7 Da kvinder leverer den samme mængde ilt ved lavere UBF-hastigheder end moderfår (~150 mod ~270 ml/kg), følger det heraf, at den menneskelige placenta er mere effektiv i denne henseende. For fostre med samme vægt kræves der således mindre absolut UBF, og graviditetsbelastningen på hjertet mindskes.
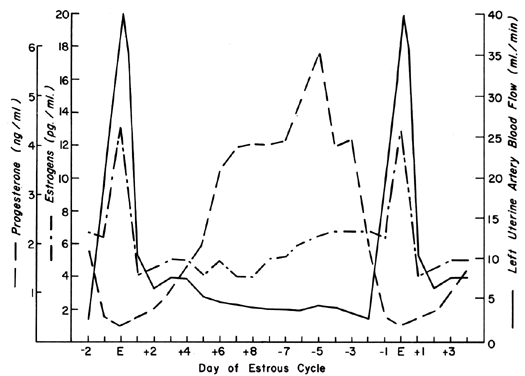 Fig. 1. Unilateralt uterin blodgennemstrømningsmønster i løbet af fårenes østruscyklus vist med rapporterede serumniveauer af østrogener og progesteron (Tilpasset fra Greiss FC, Jr, Anderson SG: Am J Obstet Gynecol 103:629, 1969; Yuthasastrakosol P et al: J Reprod Fertil 43:57, 1975.)
Fig. 1. Unilateralt uterin blodgennemstrømningsmønster i løbet af fårenes østruscyklus vist med rapporterede serumniveauer af østrogener og progesteron (Tilpasset fra Greiss FC, Jr, Anderson SG: Am J Obstet Gynecol 103:629, 1969; Yuthasastrakosol P et al: J Reprod Fertil 43:57, 1975.)
 Figur 2. Longitudinelle mønstre af uterin blodgennemstrømning og dens fordeling i løbet af en ægge-drætstid.
Figur 2. Longitudinelle mønstre af uterin blodgennemstrømning og dens fordeling i løbet af en ægge-drætstid.
Ændringer i PBF opnås ved en stadigt stigende vasodilatation af de blodkar, der forsyner placentaen, i løbet af drægtigheden. På et hvilket som helst tidspunkt i andet og tredje trimester kan der imidlertid stort set ikke ske yderligere akut vasodilatation af disse kar. For at opretholde en konstant ilttilførsel under episoder med nedsat PBF må der derfor ske en øget iltekstraktion (fig. 3). På grundlag af de rapporterede data ser det ud til, at grænsen for øget ekstraktion er todelt. PBF skal således reduceres med mere end 50 %, før ilttilførslen mindskes. Disse overvejelser forudsætter, at den homøostatiske PBF-hastighed var optimal før flowreduktionen. Vi ved imidlertid, at de homøostatiske niveauer kan være suboptimale, enten subakut, som ved toxæmi, eller kronisk, som ved nefropatier. I sådanne tilfælde er sikkerhedsfaktoren, dvs. den procentdel af PBF, der kan reduceres, før ilttilførslen er kompromitteret, nedsat. Dette skal altid tages i betragtning, når man vurderer effekten af en akut stimulus på fosteret.
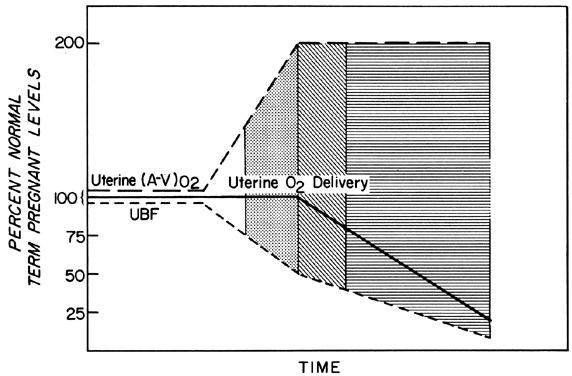 Fig. 3. Ændringer i uterin arteriovenøs iltudtrækning – (A-V)02 – som reaktion på reduktioner i uterin blodgennemstrømning i anden halvdel af den uterine drægtighed hos får. Da (A-V)02 kan fordobles, vil den uterine 02-levering blive opretholdt på et homøostatisk niveau, indtil den uterine blodgennemstrømning reduceres med mere end 50 %. De tydelige, stiplede og linierede områder angiver hypotetiske grader af fosterreserve, når de defineres som en funktion af optimal placentablodgennemstrømning, og de anvendes til at angive lignende niveauer af fosterreserve i efterfølgende illustrationer. (Tilpasset fra Huckabee WE, Metcalfe J, Prystowsky H et al: Blood flow and oxygen consumption of the pregnant uterus. Physiol 200:274, 1961.)
Fig. 3. Ændringer i uterin arteriovenøs iltudtrækning – (A-V)02 – som reaktion på reduktioner i uterin blodgennemstrømning i anden halvdel af den uterine drægtighed hos får. Da (A-V)02 kan fordobles, vil den uterine 02-levering blive opretholdt på et homøostatisk niveau, indtil den uterine blodgennemstrømning reduceres med mere end 50 %. De tydelige, stiplede og linierede områder angiver hypotetiske grader af fosterreserve, når de defineres som en funktion af optimal placentablodgennemstrømning, og de anvendes til at angive lignende niveauer af fosterreserve i efterfølgende illustrationer. (Tilpasset fra Huckabee WE, Metcalfe J, Prystowsky H et al: Blood flow and oxygen consumption of the pregnant uterus. Physiol 200:274, 1961.)
**I mennesket og hos undermenneskelige primater mister de spiralarterioler, der skal forsyne det intervilløse rum (ca. én pr. placentakotyledon), deres kapillærforbindelser og udvider sig ca. ti gange som følge af erstatning af karvæggene med trophoblast. Denne proces kan strække sig til eller under den myoendometriale overgang, hvilket bogstaveligt talt forvandler spiralarteriolerne til spiralarterier. Blod, der strømmer gennem disse modificerede blodkar ind i det intervilløse rum, udgør PBF.
I fårene er der i ikke-gravid tilstand flere diskrete områder af endometrium, kaldet karunkel, til stede. Under drægtigheden sker der en sammenvoksning af foster- og modervæv i disse karunkler, som udvider sig og bliver til individuelle placentakotyledoner. Det blod, der strømmer til disse områder, udgør tilsammen PBF. Selv om de cotyledonære arterielle blodkar udvider sig betydeligt, indeholder de ingen trophoblastiske elementer, overførsel mellem moder og foster sker via en kapillær-kapillær grænseflade, og der er ikke noget intervilløst rum til stede.
Dynamiske reaktioner i det uterine kredsløb
Blodkarrene i den ikke-gravide livmoder reagerer på samme måde som blodkarrene i ethvert andet muskelorgan med undtagelse af deres unikke reaktivitet over for østrogene stimulering, deres reaktion på lokalanæstetiske midler og muligvis deres reaktion på prostaglandiner (Tabel 1). I løbet af graviditeten udvider de blodkar, der forsyner placentaen, sig gradvist og opnår en tilstand, hvor der kun kan ske minimal eller ingen yderligere akut dilatation.24 Derfor er stimuli, der fremkalder vasodilatation i den ikke-gravide uterus, ineffektive, efter at der er sket en endelig placentation. De placentale kar bevarer dog deres evne til at vasokonstriktion som i den ikke-gravide tilstand. Da PBF udgør ca. 80-90 % af den samlede UBF ved terminsgraviditet, vil de samlede uterine vaskulære reaktioner fremstå som de placentale karres reaktioner. Dette punkt bliver ofte fejlfortolket, og man skal huske, at responserne fra de ikke-placentale kar er de samme, uanset om der er graviditet eller ej.
TABEL 1. Reaktioner i det ikke-gravide uterine karkarsystem*
|
Vasokonstriktion |
Vasodilatation |
|
|
α-Adrenergisk stimulering |
β-Adrenergisk stimulering |
|
|
(dopamin, epinephrin, |
(isoproterenol, epinephrin)8,9,16 |
|
|
norepinephrin)8,9,16 |
||
|
norepinephrin)8,9,10 |
Acetylcholin og parasympathomimetiske midler23 |
|
|
Sympathomimetiske midler11 |
Adenosiner17 |
|
|
(vasopressormidler) |
Bradykinin17,18 |
|
|
Hypoxæmi(alvorlig)12 |
Cyanid19 |
|
|
Lokalbedøvende midler |
Estrogener |
|
|
(intraarteriel administration)13,14 |
(forsinket men langvarig virkning)2 |
|
|
Nicotin |
Glucosamin |
|
|
(α-adrenerge mediering)15 |
(? osmotisk virkning)21 |
|
|
Hypoxæmi (mild)12 |
||
|
Iskæmi19 |
||
|
Nitroglycerin19 |
||
|
Prostaglandiner E1, E2 og I18,22 |
||
|
Vasoaktivt intestinal polypeptid20 |
** Den markante dilatation af de blodkar, der forsyner placenta, og den præponderante fordeling af uterinblodstrømmen til placenta udvisker de graviditetsrelaterede reaktioner; Derfor er virkningerne af vasodilaterende stimuli under graviditet kontroversielle. Når de testes, svarer de ikke-placentale vaskulære reaktioner til de ikke-gravide reaktioner.
Den menneskelige placentas hæmokoriale struktur tilføjer en unik faktor til dem, der normalt kontrollerer blodgennemstrømningen i andre vaskulære senge. Det vil sige, at blodet krydser spiralarterierne for at komme ind i det sumplignende intervilløse rum, perfunderer de føtale villi og vender derefter tilbage til den generelle cirkulation gennem mange opsamlingsvener i basalpladen. Blodet forlader således de normale vaskulære kanaler for at cirkulere i et nyt ekstravaskulært rum, der er podet ind i livmoderen under hele graviditeten. Da det intervilløse rum ligger inden for livmoderhulen, og da placenta er en fleksibel struktur, vil det tryk, der genereres af det kontraherende myometrium, blive overført ligeligt til fosterhulen og det intervilløse rum. Således kan en faktor, der er uden for den sædvanlige vaskulære kontrol, nemlig myometrial aktivitet, ændre trykket i det intervilløse rum og påvirke PBF gennem dens virkninger på perfusionstrykket. En skematisk fremstilling af blodgennemstrømningen til de ikke-placentale væv og til en enkelt kimblade er vist i figur 4 sammen med de formler, der er relevante for kontrollen af hver af dem. Det skal bemærkes, at disse formler kun er anvendelser af Ohm’s lov på disse individuelle kardiovaskulære situationer.
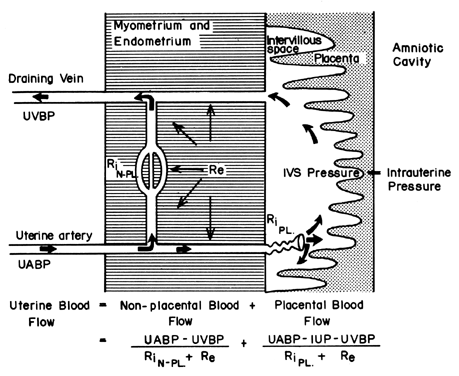 Figur 4. Ikke-placentale og placentale cirkulationer og de faktorer, der påvirker hver af dem i primatens uterus. Sammenhængen mellem disse faktorer og den distributive blodgennemstrømning er defineret i den ledsagende ligning. UABP, uterint arterielt blodtryk; UVBP, uterint venøst blodtryk; Re, ekstrinsisk vaskulær modstand; RiN-PL og RiPL, intrinsisk vaskulær modstand forårsaget af reaktiviteten af henholdsvis de ikke-placentale og placentale arterioler.(Fra Greiss FC, Jr: MCV/Q, 8:52, 1972.)
Figur 4. Ikke-placentale og placentale cirkulationer og de faktorer, der påvirker hver af dem i primatens uterus. Sammenhængen mellem disse faktorer og den distributive blodgennemstrømning er defineret i den ledsagende ligning. UABP, uterint arterielt blodtryk; UVBP, uterint venøst blodtryk; Re, ekstrinsisk vaskulær modstand; RiN-PL og RiPL, intrinsisk vaskulær modstand forårsaget af reaktiviteten af henholdsvis de ikke-placentale og placentale arterioler.(Fra Greiss FC, Jr: MCV/Q, 8:52, 1972.)
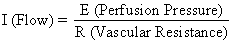
Det perfusionstryk, der leverer blod til ikke-placentale væv, er forskellen mellem det uterine arterielle og venøse blodtryk. Perfusionstrykket, der leverer blod til det intervilløse rum, er imidlertid forskellen mellem det uterine arterielle blodtryk og trykket i det intervilløse rum. Sidstnævnte tilnærmes bedst ved hjælp af fostervæsketrykket (IUP). I et muskulært organ vil modstandsfaktorerne omfatte modstand fra reaktivitet i den glatte vaskulære muskulatur, eller intrinsisk modstand (Ri), og det pres, der påføres blodkarrene, når de passerer gennem det kontraherende myometrium, eller extrinsisk modstand (Re). Det burde derfor være indlysende, at uterinkontraktioner kan påvirke PBF ved to mekanismer: ved at øge Re og ved at reducere det placentale perfusionstryk.
I klinisk praksis er tre hovedkarakteristika ved placenta-vaskulær kontrol vigtige. Disse omfatter forholdet mellem perfusionstryk og flow, spiralarteriernes respons på vasoaktive stimuli og virkningerne af myometriale sammentrækninger. Desuden skal man være opmærksom på de unikke virkninger af lokalanæstetiske midler.
Tryk-flow-forholdet
Når man observerer ændringer i UBF sekundært til reduktioner i perfusionstryk under myometrial quiescens, kan man udvikle et retlinet forhold med en hældning på 1 (Fig. 5). Dette afspejler den bredt dilaterede karakter af det placentale vaskulatur og indikerer, at PBF vil falde næsten i identisk forhold til faldet i perfusionstrykket. Da det uterine venøse tryk er ret konstant under de fleste omstændigheder, kan ændringer i det systemiske blodtryk (MBP) anvendes til at tilnærme sig PBF-ændringer. Det vil sige, at et fald på 25 % i det gennemsnitlige arterielle tryk forventes at medføre et fald på 25 % i PBF. Sådanne målinger bør imidlertid foretages i lateral decubitus-stilling, da det har vist sig, at den gravide uterus’ tryk på aorta alene sænker blodtrykket i bækkenområdet til under det, der observeres i brachialarterien.
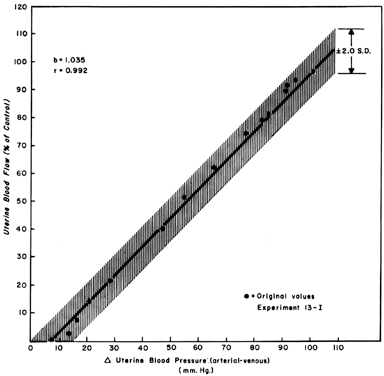 Figur 5. Tryk-flow-regressionslinje bestemt ud fra puljede proportionelle data hos terminsdygtige moderfår. Da sammenhængen er lineær, vil den uterine blodgennemstrømning variere med og i forhold til enhver ændring i perfusionstrykket (Fra Greiss FC, Jr: Am J Obstet Gynecol 96:41, 1966.)
Figur 5. Tryk-flow-regressionslinje bestemt ud fra puljede proportionelle data hos terminsdygtige moderfår. Da sammenhængen er lineær, vil den uterine blodgennemstrømning variere med og i forhold til enhver ændring i perfusionstrykket (Fra Greiss FC, Jr: Am J Obstet Gynecol 96:41, 1966.)
Reaktioner på vasoaktive stimuli
Da spiralarterierne nærmer sig maksimal dilatation i hviletilstand, har vasodilaterende midler eller stimuli ringe eller ingen virkning, selv om der er receptorer for sådanne midler til stede. Den glatte muskulatur i disse kar er imidlertid yderst følsom over for vasokonstriktoriske midler eller stimuli, mere end i de fleste andre perifere vaskulære senge (fig. 6). Dette betyder, at selv om MPB kan stige som reaktion på stimulering med et perifert virkende vasopressormiddel som f.eks. phenylephrin, er den forholdsmæssige stigning i placenta-vaskulær modstand (Ri) SÅ meget større, at nettoeffekten er et markant fald i PBF. Sådanne forskelle i vasokonstriktorfølsomhed skal tages i betragtning, når et vasopressormiddel er indiceret. Anvendelse af et mere centralt virkende lægemiddel som f.eks. efedrin vil, selv om det forårsager en lille mængde placental vasokonstriktion, resultere i en forholdsmæssigt større forbedring af MBP med en absolut stigning i PBF.
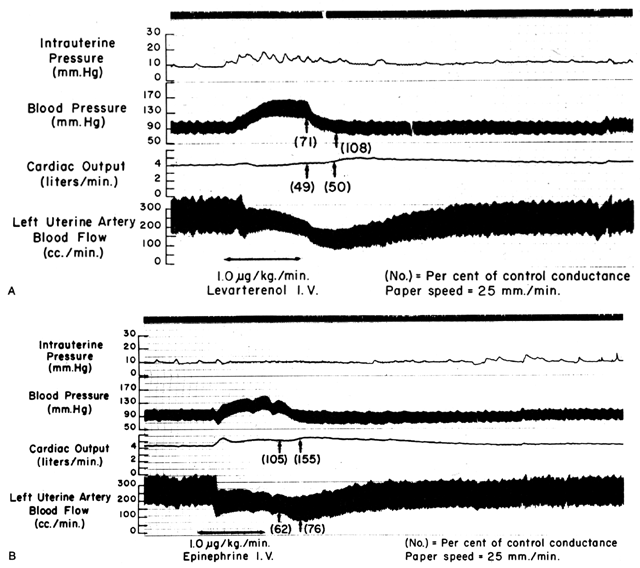 Fig. 6. Originale optagelser, der viser virkningerne af intravenøs ( A) levarterenol (noradrenalin) og ( B) epinephrin på moderens blodtryk, hjertevolumen og uterinblodgennemstrømning ved terminsfrugt hos får. Proportionelle ændringer i forhold til kontrolniveauerne af systemisk og uterin konduktans (det reciprokke af modstand) er indsat i parentes. Bemærk, at faldet i uterinkonduktans (stigning i modstand) er større end faldet i systemisk konduktans med andre midler. (Fra Greiss FC, Jr: Obstet Gynecol 21:295, 1963. Courtesy of Harper & Row, Publishers.)
Fig. 6. Originale optagelser, der viser virkningerne af intravenøs ( A) levarterenol (noradrenalin) og ( B) epinephrin på moderens blodtryk, hjertevolumen og uterinblodgennemstrømning ved terminsfrugt hos får. Proportionelle ændringer i forhold til kontrolniveauerne af systemisk og uterin konduktans (det reciprokke af modstand) er indsat i parentes. Bemærk, at faldet i uterinkonduktans (stigning i modstand) er større end faldet i systemisk konduktans med andre midler. (Fra Greiss FC, Jr: Obstet Gynecol 21:295, 1963. Courtesy of Harper & Row, Publishers.)
Myometrial Contractions
Ved hjælp af de to mekanismer, der er diskuteret ovenfor, nemlig forøgelse af Re og nedsættelse af perfusionstrykket, nedsætter myometrial kontraktioner PBF i direkte forhold til intensiteten og varigheden af hver kontraktion. Sammenhængen er så præcis, at en sporing af det intrauterine tryk næsten er et nøjagtigt omvendt billede af PBF (fig. 7). En forøgelse af kontraktionsfrekvensen mindsker PBF i en given tidsenhed ved at mindske varigheden af myometrial diastole, det tidsrum, hvor PBF er på et homøostatisk niveau. Hvis interkontraktionstonus forhøjes, som det er tilfældet ved en placentaabruption, vil PBF mellem kontraktionerne desuden blive reduceret proportionelt. Radioangiografiske undersøgelser hos undermenneskelige primater og kvinder viser, at PBF ophører under højdepunktet af myometriale kontraktioner af gennemsnitlig intensitet.25 Det er derfor indlysende, at fødslen i sagens natur er stressende for fosteret, da den gennemsnitlige mængde PBF, der perfunderer fostervillerne pr. givet tidsrum, falder gradvist, efterhånden som hyppigheden og intensiteten af uteruskontraktioner stiger.
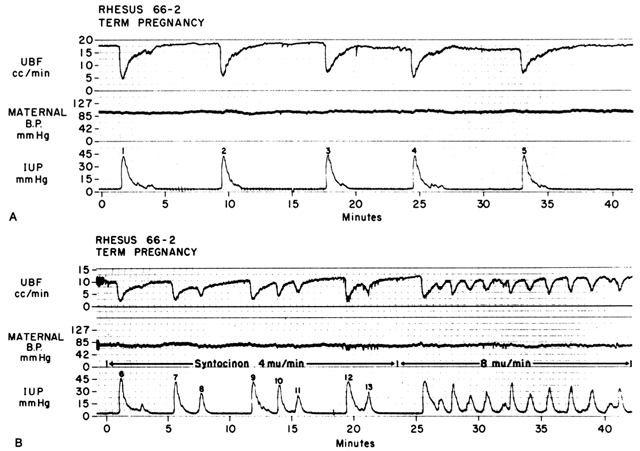 Fig. 7. A. Forholdet mellem uterin blodgennemstrømning (UBF) og uterinkontraktioner under spontane veer hos en rhesusabe. Bemærk den omvendte billedrelation, kraftige fald i UBF ved kontraktionernes begyndelse og langsommere genopretning af UBF af basalniveauet. UBF genvandt kun basalniveauet under “normal” tonus. B. Virkningen af øget kontraktionsfrekvens på UBF produceret af oxytocinstimulering af den spontane fødsel vist i A. Bemærk, at varigheden af faserne med normal tonus er nedsat. Den UBF-hastighed, der opnås mellem kontraktioner, er afhængig af intensiteten af den foregående kontraktion og varigheden af fasen med normal tonus. Efter veerne 7 og 12 var flowgenoprettelsen ufuldstændig, fordi den efterfølgende ve fandt sted uden en normal tonusfase (fra Greiss FC, Jr, Anderson SG: Clin Obstet Gynecol 11:96, 1968). Courtesy of Harper & Row, Publishers.)
Fig. 7. A. Forholdet mellem uterin blodgennemstrømning (UBF) og uterinkontraktioner under spontane veer hos en rhesusabe. Bemærk den omvendte billedrelation, kraftige fald i UBF ved kontraktionernes begyndelse og langsommere genopretning af UBF af basalniveauet. UBF genvandt kun basalniveauet under “normal” tonus. B. Virkningen af øget kontraktionsfrekvens på UBF produceret af oxytocinstimulering af den spontane fødsel vist i A. Bemærk, at varigheden af faserne med normal tonus er nedsat. Den UBF-hastighed, der opnås mellem kontraktioner, er afhængig af intensiteten af den foregående kontraktion og varigheden af fasen med normal tonus. Efter veerne 7 og 12 var flowgenoprettelsen ufuldstændig, fordi den efterfølgende ve fandt sted uden en normal tonusfase (fra Greiss FC, Jr, Anderson SG: Clin Obstet Gynecol 11:96, 1968). Courtesy of Harper & Row, Publishers.)
Lokalbedøvende midler
Disse lægemidler kan udøve virkninger på et karbed direkte, som efter utilsigtet intravaskulær injektion, og indirekte, som følge af lammelse af autonome nerver, der opretholder normal vaskulær tonus. I de fleste organer har intravaskulære injektioner ingen væsentlige virkninger på den vaskulære modstand. De uterine og placentale vaskulaturer reagerer imidlertid på sådanne stimuli med en betydelig vasokonstriktion. Desuden stimuleres myometriet på varierende vis af sådanne lægemidler (fig. 8). Hver for sig eller sammen nedsætter disse reaktioner PBF. Efter paracervikal blokanæstesi, der gives under fødslen, kan der forekomme en forsinket føtal bradykardi. Den bedste hypotese til at forklare den føtale reaktion er, at lokalanæstetiske midler injiceres tæt på uterusarterierne, og at de på grund af deres fremragende penetrering krydser arterievæggene for at forårsage deres uterine virkninger, der nedsætter PBF og forårsager føtal hypoxi.
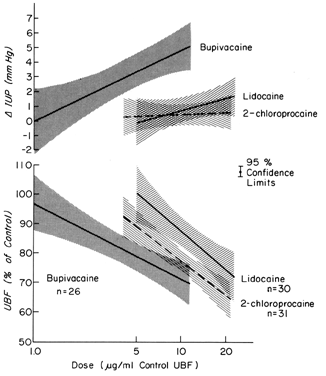 Figur 8. Dosis-respons-forhold mellem lokalbedøvende midler, der administreres direkte i uterusarterien, og uterin vaskulær konduktans og intrauterintryk i uterus under en æglægning. Effektive dosisniveauer ligger inden for de intervaller, der er observeret hos fostre under bradykardi efter paracervikal blokanæstesi (Fra Fishburne JI, Jr et al: Responses of the gravidine uterine vasculature to arterial levels of local anesthetic agents. Am J Obstet Gynecol 133:753, 1979. Med venlig høflighed af The C. V. Mosby Company.)
Figur 8. Dosis-respons-forhold mellem lokalbedøvende midler, der administreres direkte i uterusarterien, og uterin vaskulær konduktans og intrauterintryk i uterus under en æglægning. Effektive dosisniveauer ligger inden for de intervaller, der er observeret hos fostre under bradykardi efter paracervikal blokanæstesi (Fra Fishburne JI, Jr et al: Responses of the gravidine uterine vasculature to arterial levels of local anesthetic agents. Am J Obstet Gynecol 133:753, 1979. Med venlig høflighed af The C. V. Mosby Company.)
