EINLEITUNG
Grundlegende und klinische Forschungen der letzten Jahre haben eine direkte, wechselseitige Beziehung zwischen chronischen Nierenerkrankungen und Herz-Kreislauf-Erkrankungen nachgewiesen.1,2 In der täglichen klinischen Praxis werden die Serumkreatininkonzentration und die glomeruläre Filtrationsrate, die mit der Cockcroft-Gault-Formel3 oder der Modification of Diet in Renal Disease (MDRD)4 -Gleichung geschätzt wird, üblicherweise zur Einschätzung der Nierenfunktion verwendet. Die Plasmakreatininkonzentration kann jedoch durch eine Reihe von Faktoren wie Alter, Geschlecht, Muskelmasse, körperliche Aktivität, Ernährung und Medikamente beeinflusst werden.5
Cystatin C ist ein Proteininhibitor der Cysteinprotease, der von allen kernhaltigen Zellen in gleichbleibender Menge synthetisiert wird. Aufgrund seines geringen Molekulargewichts und seines hohen isoelektrischen Punkts kann es fast ausschließlich durch glomeruläre Filtration eliminiert werden. Die Cystatin-C-Konzentration wird durch Alter, Geschlecht oder Eiweißzufuhr nicht beeinflusst und reagiert empfindlich auf kleine Veränderungen der glomerulären Filtration. Aufgrund dieser Eigenschaften gilt die Cystatin-C-Konzentration im Plasma als einer der besten Marker für den glomerulären Filtrationsstatus.6-9 In jüngster Zeit haben mehrere Studien über einen Zusammenhang zwischen erhöhten Cystatin-C-Werten und der Entwicklung kardiovaskulärer Komplikationen bei Patienten mit koronarer Herzkrankheit berichtet. Derzeit ist nicht bekannt, ob dieser Zusammenhang darauf zurückzuführen ist, dass Cystatin C ein besserer Marker für die Nierenfunktion ist als das Serumkreatinin, oder ob es neben der glomerulären Filtration weitere Faktoren gibt, die die Konzentration dieses Proteins beeinflussen und zusätzlich mit dem kardiovaskulären Risiko zusammenhängen.10
Ziel dieser Studie war es, den prognostischen Wert der Cystatin-C-Konzentration im Plasma bei Patienten zu bewerten, die wegen eines akuten Koronarsyndroms (ACS) mit hohem Risiko hospitalisiert wurden, und die Beziehung zwischen Cystatin C und anderen Markern für Nierenfunktion und Entzündung zu untersuchen.
METHODEN
Es handelt sich um eine prospektive Beobachtungsstudie, die zwischen Mai 2006 und Juli 2007 durchgeführt wurde. Insgesamt wurden 203 Patienten, die älter als 18 Jahre waren und konsekutiv auf der kardiologischen Intensivstation (ICU) unseres Zentrums mit der Diagnose eines Hochrisiko-ACS hospitalisiert wurden, eingeschlossen.
Die Diagnosekriterien für ein Hochrisiko-ACS umfassten mindestens zwei der folgenden Faktoren: Schmerzen mit ischämischen Merkmalen, elektrokardiografische Veränderungen, die auf eine Ischämie hindeuten, und/oder erhöhte Myokardnekrose-Marker. Die Behandlung und die zusätzlichen Untersuchungen, die während des Krankenhausaufenthalts des Patienten durchgeführt wurden, beruhten auf den klinischen Entscheidungen des behandelnden Arztes. Bei den meisten Patienten wurde eine invasive Strategie angewandt, die eine dringende Koronarangiographie (bei Myokardinfarkt mit ST-Strecken-Hebung oder Linksschenkelblock) oder eine frühzeitige geplante Koronarangiographie innerhalb der ersten 24 bis 72 Stunden nach der Krankenhausaufnahme vorsah.
Klinische Merkmale
Die folgenden Daten wurden aus den klinischen Aufzeichnungen der Patienten erfasst: demografische Informationen, Vorhandensein klassischer kardiovaskulärer Risikofaktoren (Diabetes mellitus, systemische Hypertonie, Dyslipidämie und Rauchen) und bekannte Gefäßerkrankungen in der Vorgeschichte (ischämische Herzkrankheit, zerebrovaskuläre Erkrankung, periphere arterielle Verschlusskrankheit und frühere myokardiale Revaskularisationsbehandlung). Zu den anderen klinischen Variablen, die analysiert wurden, gehörten die Art des ACS, die Killip-Klasse zum Zeitpunkt des Krankenhausaufenthalts, die systolischen und diastolischen Druckwerte, der Pulsdruck (geschätzt als Differenz zwischen systolischem und diastolischem arteriellem Druck) und die Herzfrequenz.
Alle Patienten unterzogen sich einer Echokardiographie, bei der die linksventrikuläre Auswurffraktion mit der Simpson-Methode unter Verwendung eines 4-Kammer-Ansatzes geschätzt wurde; bei Patienten mit Sinusrhythmus wurde der Mittelwert von 3 Bestimmungen berechnet, bei denen mit Vorhofflimmern der Mittelwert von 5 Bestimmungen.
Bei 95 % der Patienten wurde eine Koronarangiographie durchgeführt, und der Schweregrad der Koronarläsionen wurde anhand eines Scores bewertet, der auf der Anzahl der betroffenen epikardialen Koronararterien basierte.
Analytische Daten
Baseline-Werte für Hämoglobin, Hämatokrit, Leukozyten, Glukose und Kreatinin wurden in den ersten Laboranalysen erfasst, die in unserem Zentrum zum Zeitpunkt des Krankenhausaufenthalts durchgeführt wurden. Die Konzentrationen von Gesamtcholesterin, High-Density-Lipoprotein-Cholesterin (HDL-C), Low-Density-Lipoprotein-Cholesterin (LDL-C), Glukose, hochsensitivem C-reaktivem Protein und Cystatin C wurden in den ersten 24 Stunden zusammen mit dem Spitzenwert von Troponin I (TpI) erfasst.
Cystatin C wurde mit einem automatisierten homogenen Immunoassay unter Verwendung eines Dade-Behring BN ProSpec Nephelometers gemessen. Das Reagenz für die Analyse bestand aus Polystyrolpartikeln, die mit Antikörpern gegen das Protein beschichtet waren. Diese Partikel agglutinieren, wenn sie mit Cystatin C-haltigen Proben gemischt werden, und streuen Licht mit einer Intensität, die proportional zur Konzentration des Analyten ist.
Das Referenzintervall für die Serum-Cystatin-C-Konzentration bei Erwachsenen mit der verwendeten nephelometrischen Methode beträgt 0,51 bis 0,95 mg/L. Die Konzentrationen des hochsensitiven C-reaktiven Proteins wurden ebenfalls mittels Immunoassay bestimmt. Die glomeruläre Filtrationsrate wurde mit der MDRD-Gleichung geschätzt.
Analysierte Episoden
Zu den analysierten kardiovaskulären Komplikationen gehörten die Sterblichkeit im Krankenhaus, die Gesamtmortalität während der Nachbeobachtung, die Entwicklung eines neuen Myokardinfarkts, definiert als Brustschmerzen oder äquivalente Angina pectoris mit EKG-Veränderungen, oder erhöhte Tumornekrose-Marker während der ersten 24 Stunden nach dem Krankenhausaufenthalt (Patienten mit erhöhten Markern nach koronaren Interventionsverfahren wurden ausgeschlossen) und die Entwicklung einer Herzinsuffizienz während des Krankenhausaufenthalts oder der Nachbeobachtung.
Klinische Nachbeobachtung
Die durchschnittliche Nachbeobachtungszeit betrug 186 (SD, 110; Median, 156) Tage, in denen alle klinischen Ereignisse der Patienten erfasst wurden. Die Nachbeobachtung erfolgte durch telefonischen Kontakt, in Ambulanzen und durch Einsichtnahme in die Krankenakte der Patienten.
Statistische Analyse
Alle Informationen wurden prospektiv in einer mit Microsoft Office Access 2003 SP2 erstellten Datenbank erfasst. Die statistischen Analysen wurden mit SPSS (Statistical Package for the Social Sciences), Version 12.0, durchgeführt. Die kategorialen oder dichotomen Variablen werden als absolute Werte und Prozentsätze ausgedrückt und wurden mit dem Pearson χ2-Test verglichen. Die kontinuierlichen Variablen mit einer Normalverteilung werden als Mittelwert (SD) angegeben, und der Student t-Test wurde für die Vergleiche zwischen den Gruppen verwendet. Variablen, die keine Gaußsche Verteilung aufwiesen, wurden mit dem Mann-Whitney-U-Test verglichen.
Der Spearman-Korrelationskoeffizient wurde verwendet, um die Korrelationen der Cystatin-C-Konzentration mit dem hochsensitiven C-reaktiven Protein und der glomerulären Filtrationsrate zu bewerten. Mit Hilfe einer logistischen Regressionsanalyse wurde die unabhängige Rolle der klinischen und Laborfaktoren in Bezug auf Cystatin C für die Vorhersage der Entwicklung kardiovaskulärer Komplikationen während des Krankenhausaufenthalts bewertet, einschließlich der signifikanten Variablen der univariaten Analyse. Es werden die bereinigten Odds Ratios und 95%-Konfidenzintervalle (CI) dargestellt. Es wurden Kaplan-Meier-Überlebenskurven während der Nachbeobachtung erstellt und mit dem Long-Rank-Test verglichen.
Um eine deskriptive Analyse der untersuchten Population durchzuführen, wurden einige quantitative Variablen in Intervalle eingeteilt: die glomeruläre Filtrationsrate (>90, 90-60, 55% und 0,95 und
Ein P-Wert von weniger als .05 wurde als statistisch signifikant angesehen.
ERGEBNISSE
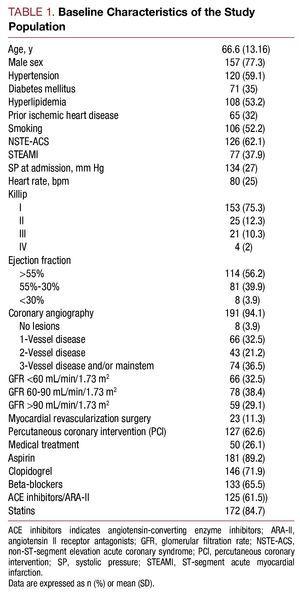
Von Mai 2006 bis Juli 2007 wurden 203 Patienten, die mit der Diagnose eines Hochrisiko-ACS ins Krankenhaus eingeliefert wurden, in die Studie aufgenommen. Das Durchschnittsalter betrug 66,6 (13,16) Jahre. Bei 62,1 % der Patienten (n=126) handelte es sich um ein ACS ohne ST-Strecken-Hebung und bei 37,9 % (n=77) um ein ACS mit ST-Strecken-Hebung. Die Ausgangsmerkmale der Studienpopulation sind in Tabelle 1 beschrieben.
Die mediane Cystatin-C-Konzentration betrug 1,01 (Bereich, 0,83-1,35) mg/L, das Plasmakreatinin bei der ersten durchgeführten Analyse 1 (0.9-1,3) mg/L, die glomeruläre Filtrationsrate lag bei 72,4 (49,12-93,73) ml/min/1,73 m2 und das hochempfindliche C-reaktive Protein bei 1,37 (0,46-5,02) mg/L. Die glomeruläre Filtrationsrate zum Zeitpunkt des Krankenhausaufenthalts lag bei 32,5 % der Patienten bei 2, und der Serum-Cystatin-C-Wert betrug bei 113 (55,7 %) Patienten >0,95 mg/L.
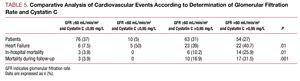
Patienten mit höheren Cystatin-C-Werten wiesen ein schlechteres klinisches Profil auf, waren älter, hatten eine hohe Prävalenz von Bluthochdruck, eine schlechtere Killip-Klasse zum Zeitpunkt des Krankenhausaufenthalts, eine schwerere Koronarerkrankung bei der Koronarangiographie und höhere Plasmakreatinin- und C-reaktive Proteinwerte (Tabelle 2).
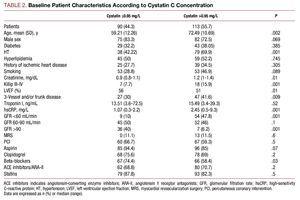
Es gab keine signifikanten Unterschiede zwischen den beiden Cystatin-C-Gruppen hinsichtlich der durchgeführten Koronarintervention; das angiographische Endergebnis ergab eine ähnliche Erfolgsrate und keine signifikanten Komplikationen (3,27 % bei Patienten mit Cystatin C ≤0,95 und 4,09 % in der anderen Gruppe). Die Analyse der pharmakologischen Behandlung zeigte einen wesentlich höheren Einsatz von Betablockern und Aspirin in der Gruppe mit Cystatin C ≤0,95 (Tabelle 2).
Die Serum-Cystatin-C-Werte zeigten eine höhere Korrelation mit der geschätzten glomerulären Filtrationsrate (r=-0,655; P=,001) (Abbildung 1) als mit der Mikroalbuminurie (r=0,302, P=,01) und eine geringere Korrelation mit dem C-reaktiven Protein (r=0,29; P=,01).
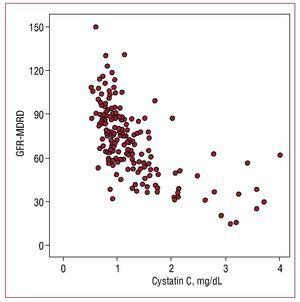
Abbildung 1. Korrelation zwischen Cystatin-C-Werten und der mit der MDRD-Formel (GFR-MDRD) geschätzten glomerulären Filtrationsrate.
In der Gruppe der Patienten mit Cystatin-C-Werten >0,95 wiesen 6,5 % normale glomeruläre Filtrationsraten und 46 % glomeruläre Filtrationsraten zwischen 60 und 90 ml/min/1,73 m2 auf. Darüber hinaus hatten 10 % der Patienten, die eine Nierenfunktionsstörung mit einer Filtrationsrate von 2 hatten, Cystatin-C-Werte
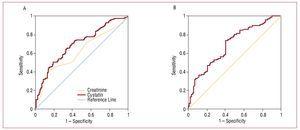
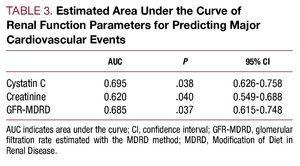
Abbildung 2. A, ROC-Kurven von Cystatin C und Kreatinin in Bezug auf die Entwicklung von kardiovaskulären Komplikationen (Herzinsuffizienz, Infarkt und kardiovaskulärer Tod). B, ROC-Kurve der mit der MDRD geschätzten glomerulären Filtrationsrate in Bezug auf die Entwicklung kardiovaskulärer Komplikationen (Herzversagen, Infarkt und kardiovaskulärer Tod).
Der Krankenhausaufenthalt dauerte im Median 9 (6-19) Tage. Vom Zeitpunkt der Aufnahme bis zum Abschluss der Nachbeobachtung entwickelten 56 (27,58 %) Patienten aus der Gesamtstichprobe eine Herzinsuffizienz, die meisten von ihnen in der Gruppe mit erhöhten Cystatin-C-Werten (45 Patienten). Die In-Hospital-Mortalität war in der Gruppe mit erhöhten Cystatin-C-Werten signifikant höher (17,6 % gegenüber 3,3 %; P=.001), und diese Unterschiede blieben während der Nachbeobachtung bestehen (Abbildung 3, Tabelle 4).
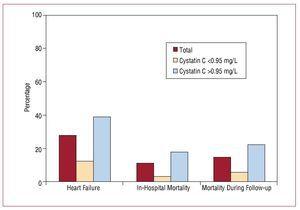
Abbildung 3. Zusammenhang zwischen Cystatin C 0,95 mg/L und der Entwicklung von kardiovaskulären Ereignissen im Krankenhaus.

In der univariaten Analyse wurde kein Zusammenhang zwischen kardiovaskulären Komplikationen und der Art des ACS, der Hyperlipidämie oder der TpI-Spitzenkonzentration festgestellt, wohl aber ein Zusammenhang mit den übrigen kardiovaskulären Risikofaktoren: Anzahl der betroffenen Gefäße, Ejektionsfraktion, Nierenfunktionsmarker, Cystatin C und hochempfindliches C-reaktives Protein. Bei der Analyse der Ergebnisse von Patienten mit einer glomerulären Filtrationsrate von >60 mL/min/1,73 m2 wurde festgestellt, dass Patienten mit Cystatin C >0.95 mg/L eine signifikant höhere Rate an kardiovaskulären Komplikationen aufwiesen als Patienten mit einer glomerulären Filtrationsrate >60 und Cystatin C 60 und Cystatin C
Das geschätzte ereignisfreie Überleben (d. h. keine Herzinsuffizienz, kein Myokardinfarkt oder Tod) nach einer mittleren Nachbeobachtungszeit von 186 Tagen war in der Gruppe der Patienten mit Cystatin-Werten ≤0.95 mg/L: 75 % gegenüber 44 % (P=.02) (Abbildung 4).

Abbildung 4. Kaplan-Meier-Kurven zur Schätzung der Überlebenswahrscheinlichkeit ohne größere kardiovaskuläre Ereignisse in Abhängigkeit vom Cystatin-C-Wert.
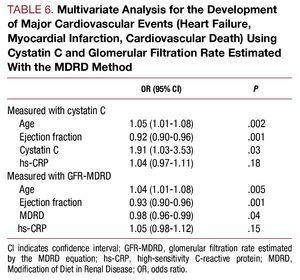
Die multivariate Analyse identifizierte Alter, Ejektionsfraktion und Cystatin-C-Konzentration als unabhängige prädiktive Faktoren für kardiovaskuläre Komplikationen während des Krankenhausaufenthalts (Tabelle 6).
DISKUSSION
Die Ergebnisse der vorliegenden Studie deuten darauf hin, dass erhöhte Cystatin-C-Werte bei Patienten mit Hochrisiko-ACS unabhängig von anderen klassischen Risikofaktoren die Entwicklung von Herzinsuffizienz, Myokardinfarkt und kardiovaskulärem Tod im Krankenhaus vorhersagen. Darüber hinaus ist der Cystatin-C-Plasmawert möglicherweise besser geeignet, Patienten mit einem hohen Risiko für kardiovaskuläre Komplikationen während des Krankenhausaufenthalts zu stratifizieren als andere Methoden zur Beurteilung der Nierenfunktion. Wir fanden heraus, dass ein erhöhter Cystatin C-Wert auch in der Gruppe der Patienten mit normaler glomerulärer Filtration mit einer schlechteren kardiovaskulären Prognose verbunden war. Unseres Wissens ist dies der erste Bericht über diesen Zusammenhang, der unseres Erachtens Auswirkungen auf die Risikostratifizierung in dieser Patientengruppe haben könnte.
In den letzten Jahren wurde in mehreren Artikeln ein enger Zusammenhang zwischen Nierenfunktionsstörungen und kardiovaskulären Komplikationen bei der Nachbeobachtung von Patienten mit akuter und chronischer ischämischer Herzerkrankung sowie anderen klinischen Erscheinungsformen kardiovaskulärer Erkrankungen, insbesondere Herzinsuffizienz, beschrieben.1,10-12 Eine Verringerung der glomerulären Filtrationsrate unter 60 ml/min ist mit einem deutlich erhöhten Risiko für Tod, Herzinfarkt und Schlaganfall verbunden, und zwar sowohl bei Patienten mit als auch ohne vorherige kardiovaskuläre Erkrankung.13 Dieser Zusammenhang wurde insbesondere bei ACS-Patienten mit ST-Strecken-Hebung und bei Patienten ohne ST-Strecken-Hebung beschrieben.10,13-15 In der VALIANT-Studie16 (Patienten mit ventrikulärer Dysfunktion und Herzinsuffizienz nach ST-Strecken-Hebung-Myokardinfarkt) war eine Verschlechterung der Nierenfunktion (bewertet anhand der glomerulären Filtrationsrate) mit einem Anstieg der Sterblichkeit und kardiovaskulärer Komplikationen während der Nachbeobachtung verbunden. Ähnliche Ergebnisse wurden für die Patientengruppen in den Studien SAVE (ventrikuläre Postinfarktdysfunktion), HOPE (Patienten mit hohem kardiovaskulärem Risiko, mehrheitlich mit chronischer ischämischer Herzerkrankung) und PEACE (Patienten mit chronischer ischämischer Herzerkrankung) berichtet. In diesen Studien wurde der Zusammenhang zwischen der Nierenfunktionsstörung und der Prognose sowohl für die verringerte glomeruläre Filtrationsrate als auch für die Albuminausscheidung im Urin beobachtet.16-19
Wie bereits erwähnt, wurde eine direkte wechselseitige Beziehung zwischen Nierenfunktionsstörung und Herz-Kreislauf-Erkrankungen beschrieben. Chronisches Nierenversagen begünstigt die Entwicklung von Bluthochdruck und Dyslipidämie und fördert die Aktivierung des Renin-Angiotensin-Dosteron-Systems. Diese Faktoren scheinen zusammen mit dem Anstieg der Entzündungsmediatoren zu einer erhöhten Produktion freier Radikale beizutragen, die in den atherosklerotischen Prozess und die kardiovaskulären Schäden eingreifen. Darüber hinaus begünstigen Veränderungen des Mineralstoffwechsels (Zunahme der Promotoren und Abnahme der Inhibitoren der Kalzifizierung) Kalziumablagerungen in den Herzkranzgefäßen.20,21 Schließlich wurde bei Patienten mit Nierenfunktionsstörungen ein weniger intensiver Einsatz von therapeutischen Maßnahmen mit anerkanntem klinischem und prognostischem Nutzen beschrieben. Insbesondere bei ACS-Patienten können eine weniger aggressive Behandlung und längere Verzögerungen bei der Durchführung interventioneller Koronarverfahren sowie ein geringerer Einsatz von IIb/IIIa, Blockern der Renin-Angiotensin-Aldosteron-Achse, Betablockern, Statinen und Thrombozytenaggregationshemmern zu der beschriebenen schlechteren Prognose in dieser Patientengruppe beitragen.22
In der täglichen klinischen Praxis basiert die Beurteilung der Nierenfunktion in der Regel auf der Bestimmung des Serumkreatinins und der Schätzung der glomerulären Filtrationsrate anhand der Cockcroft-Gault- oder der MDRD-Formel. Diese beiden Methoden weisen mehrere Einschränkungen auf, von denen viele auf Faktoren zurückzuführen sind, die die Kreatininproduktion beeinflussen, wie z. B. das Alter, das weibliche Geschlecht, rassenspezifische Merkmale, die Ernährung und der Verlauf von chronischen Krankheiten.
Diese Gleichungen wurden kürzlich bei Patienten mit Herzinsuffizienz bewertet und mit NT-proBNP, einem prognostischen Marker, verglichen. Die prognostische Aussagekraft von NT-proBNP erwies sich als besser als die der mit der MDRD-Formel geschätzten Nierenfunktion.23
Cystatin C besitzt molekulare und metabolische Eigenschaften, die die Plasmakonzentrationen dieses Proteins zu einem guten biologischen Marker für die Schätzung der Nierenfunktion machen; kleine funktionelle Veränderungen werden mit einer höheren Sensitivität erkannt als die zu diesem Zweck verwendeten herkömmlichen Parameter.24 Dies könnte die Tatsache rechtfertigen, dass in der Gruppe der Patienten mit Serum-Cystatin-C-Konzentrationen oberhalb der oberen Normgrenze 15 % eine normale glomeruläre Filtrationsrate aufwiesen; die Bestimmung von Statin C kann zur Identifizierung von Patienten mit einem präklinischen Zustand einer Nierenerkrankung nützlich sein.6
Die Ergebnisse der vorliegenden Studie stimmen bis zu einem gewissen Grad mit den berichteten Erkenntnissen überein, wonach Cystatin C ein unabhängiger Prädiktor für kardiovaskuläre Komplikationen bei Patienten mit koronarer Herzkrankheit ist.25-27 Darüber hinaus können unsere Daten dieses Konzept auf Patienten mit einer normalen glomerulären Filtrationsrate ausweiten. Jernberg et al.26 analysierten den Zusammenhang zwischen Cystatin-C-Plasmawerten und der Prognose bei einer Gruppe von Patienten, die wegen eines ACS ohne ST-Segmenterhöhung hospitalisiert wurden, und berichteten über einen signifikanten Zusammenhang zwischen Cystatin-C-Werten und der Mortalität. Außerdem wurde beschrieben, dass erhöhte Cystatin-C-Konzentrationen mit einem erhöhten Risiko für Tod, kardiovaskuläre Komplikationen und das Auftreten von Herzversagen bei ambulanten Patienten mit chronischer Koronarerkrankung einhergehen.24 Bei älteren Menschen ohne manifeste Nierenerkrankung ist Cystatin C ein Risikomarker für Tod, kardiovaskuläre Erkrankungen und chronische Nierenerkrankungen.6 In der aktuellen Studie stellten wir fest, dass Patienten mit erhöhten Cystatin-C-Werten ein schlechteres Risikoprofil aufwiesen; überraschend war jedoch der relativ niedrige C-reaktive Proteinwert. Wir glauben, dass dies durch die Kinetik des Proteins erklärt werden kann, das ein spezifisches, charakteristisches Spektrum aufweist, in dem sein Wert vom Zeitpunkt der Probenentnahme abhängt (der Spitzenwert tritt 49 Stunden nach Beginn der Symptome auf, und ein verzögerter Spitzenwert wird bei einem akuten Myokardinfarkt mit ST-Segmenterhöhung beobachtet); in unserer Studie wurden die Proben innerhalb der ersten 24 Stunden nach dem Krankenhausaufenthalt entnommen.28 Die kardiovaskulären Komplikationen, von denen die Patienten in unserer Studie betroffen waren, unterscheiden sich von denen, die in neueren Registern veröffentlicht wurden,29 was darauf zurückzuführen sein könnte, dass Patienten mit sehr hohem Risiko und einer höheren Inzidenz von Komplikationen eingeschlossen wurden. In dem kürzlich veröffentlichten MASCARA-Register waren nur 50 % der eingeschlossenen Patienten ursprünglich auf einer Intensiv- oder Herz-Intensivstation aufgenommen worden, während alle unsere Patienten von einer Herz-Intensivstation kamen, was zweifellos eine gewisse Selektionsverzerrung impliziert. Dennoch umfasste die Patientengruppe mit erhöhtem Cystatin C eine Population mit einem deutlich höheren Risikoprofil und einer höheren Anzahl kardiovaskulärer Komplikationen als die übrigen Patienten. Die vorliegende Studie trägt dazu bei, diese Assoziationen zu präzisieren, indem sie zum ersten Mal berichtet, dass erhöhte Cystatin-C-Werte in den ersten Stunden der Hospitalisierung bei Hochrisiko-ACS ein unabhängiger Prädiktor für kardiovaskuläre Komplikationen im Krankenhaus sind. Darüber hinaus ist der Zusammenhang zwischen Cystatin C und dem Risiko kardiovaskulärer Komplikationen höher als bei anderen häufig verwendeten Parametern zur Einschätzung der Nierenfunktion und bleibt auch in der Gruppe der Patienten mit normaler glomerulärer Filtration erhalten. Derzeit ist nicht genau bekannt, ob die Fähigkeit zur Vorhersage eines höheren Risikos für Komplikationen darauf zurückzuführen ist, dass Cystatin C ein besserer Marker für die Nierenfunktion ist als andere gängige Parameter (Serumkreatinin und glomeruläre Filtrationsrate), oder ob es neben der glomerulären Filtration noch andere Faktoren gibt, die die Cystatin C-Konzentration beeinflussen und direkt mit dem kardiovaskulären Risiko in Zusammenhang stehen könnten. In diesem Sinne wurde eine positive Korrelation von C-reaktiven Proteinwerten und Fibrinogen im Plasma mit erhöhten Cystatin-C-Konzentrationen und dem Vorliegen einer kardiovaskulären Erkrankung beschrieben.30 In der PRIME-Studie (Prospective Epidemiological Study of Myocardial Infarction) wurde der Zusammenhang zwischen Cystatin C und der Entwicklung eines akuten Myokardinfarkts, Herztod und Angina pectoris bei Patienten ohne koronare Erkrankung untersucht. Nach Anpassung an die üblichen kardiovaskulären Risikofaktoren war der Cystatin-C-Plasmaspiegel signifikant mit dem Auftreten der ersten koronaren Komplikation ischämischen Ursprungs verbunden. Die Autoren waren der Meinung, dass die verminderte glomeruläre Filtrationsrate die höheren Cystatin-C-Werte der Fälle im Vergleich zu den Kontrollen nicht rechtfertigt, und schlugen vor, dass Entzündungen die Ursache für den Zusammenhang zwischen Cystatin C und dem Risiko von Herz-Kreislauf-Erkrankungen sein könnten.31,32 Im Einklang mit diesen Daten zeigten unsere Ergebnisse eine positive Korrelation zwischen Cystatin C und dem hochsensitiven C-reaktiven Protein (r=0,2), das ebenfalls ein unabhängiger Prädiktor für kardiovaskuläre Komplikationen ist, und liefern weitere Beweise für das Vorhandensein direkter Beziehungen zwischen Nierenerkrankungen, Entzündungen und kardiovaskulären Erkrankungen.
Zu den wichtigsten Einschränkungen der vorgestellten Studie gehört, dass sich die Ergebnisse nur auf Patienten mit Hochrisiko-ACS beziehen, die auf einer kardiologischen Intensivstation stationär behandelt wurden, wobei die meisten von ihnen aggressiv mit einer frühen Koronarangiographie behandelt wurden. Andererseits sollten diese Merkmale hervorgehoben werden, da es nur wenige Informationen über diese spezielle Population gibt, bei der Cystatin C bei der Krankenhausaufnahme gemessen wurde. In fast allen veröffentlichten Studien wird der Zeitpunkt der Bestimmungen nicht angegeben, und zumindest bei Patienten mit ACS können die Cystatin-C-Konzentrationen im Plasma durch die Zeitspanne seit dem Ereignis und die durchgeführten diagnostischen und therapeutischen Maßnahmen beeinflusst werden. Die Einschränkung einer kurzen Nachbeobachtungszeit erschwert die Ausweitung unserer Beobachtungen auf den mittel- oder langfristigen Bereich. Dennoch bieten unsere Ergebnisse eine Möglichkeit zur Verbesserung der Risikostratifizierung bei Patienten, die wegen eines Hochrisiko-ACS ins Krankenhaus eingeliefert werden, was sowohl für die Entscheidung über die Therapie als auch für die Diagnosestellung von Nutzen sein wird.
SCHLUSSFOLGERUNGEN
Die Bestimmung von Cystatin C zum Zeitpunkt der Hospitalisierung von Patienten mit Hochrisiko-ACS kann ein gutes klinisches Instrument zur Stratifizierung des kardiovaskulären Risikos sein. Die Bestimmung dieses Proteins würde die Informationen ergänzen, die andere Methoden zur Beurteilung der Nierenfunktion liefern, und könnte neben der diagnostischen Bedeutung auch für die Identifizierung der Gruppe mit dem höchsten Risiko nützlich sein. Möglicherweise muss bei dieser Bevölkerungsgruppe besonders darauf geachtet werden, dass die in den Leitlinien für die klinische Praxis enthaltenen Empfehlungen eingehalten werden. Darüber hinaus könnte Cystatin C wichtige Informationen zur Stratifizierung von Patienten mit Hochrisiko-ACS und erhaltener Nierenfunktion liefern. Zusätzliche Studien mit einer längeren Nachbeobachtungszeit könnten erforderlich sein, um die Rolle von Cystatin C bei ACS genauer zu definieren.
ABBREVIATIONS
ACS: akutes Koronarsyndrom
MDRD: Modifikation der Ernährung bei Nierenerkrankungen
TpI: Troponin I
