![]()
Personen, die Hilfsmittel verwenden, können möglicherweise nicht vollständig auf die Informationen in dieser Datei zugreifen. Wenn Sie Hilfe benötigen, senden Sie bitte eine E-Mail an: [email protected]. Geben Sie 508 Accommodation und den Titel des Berichts in die Betreffzeile der E-Mail ein.
![]() PDF
PDF
Das Advisory Committee on Immunization Practices (ACIP) überprüft jährlich den empfohlenen Impfplan für Erwachsene, um sicherzustellen, dass der Plan die aktuellen Empfehlungen für die Verwendung zugelassener Impfstoffe widerspiegelt. Im Juni 2005 genehmigte das ACIP den Impfplan für Erwachsene für den Zeitraum Oktober 2005 bis September 2006. Dieser Plan wurde auch von der American Academy of Family Physicians und dem American College of Obstetricians and Gynecologists genehmigt.
Änderungen im Impfplan für Oktober 2005-September 2006
Der Impfplan 2005-2006 unterscheidet sich wie folgt vom vorherigen Impfplan:
- Die im altersabhängigen Impfplan (Abbildung 1) aufgeführten Impfstoffe werden so dargestellt, dass die für die routinemäßige Anwendung empfohlenen Impfstoffe von denen unterschieden werden können, die für Erwachsene mit bestimmten Risikoindikatoren empfohlen werden (ähnlich wie beim Impfplan für Kinder). Dies wird sowohl durch das Farbschema als auch durch die gestrichelte Linie veranschaulicht.
- Die gelben Balken („Für alle Personen in dieser Gruppe“) und die grünen Balken („Für Personen ohne Impfnachweis oder Krankheitsnachweis“) aus dem früheren Impfplan wurden zu einem gelben Balken zusammengefasst, der nun lautet: „Für alle Personen in dieser Kategorie, die die Altersanforderungen erfüllen und bei denen kein Immunitätsnachweis vorliegt (z. B.,
- Der violette Balken wurde von „Für Risikopersonen (z. B. mit medizinischer Indikation/Expositionsindikation)“ in „Empfohlen, wenn ein anderer Risikofaktor vorliegt (z. B. auf der Grundlage medizinischer, beruflicher, lebensstilbezogener oder anderer Indikationen)“ geändert.) Der violette Balken wurde in den Spalten für die Altersgruppen 50-64 Jahre und >65 Jahre für den Impfstoff gegen Masern, Mumps und Röteln (MMR) hinzugefügt.
- Die Spalte „Diabetes, Herzerkrankung, chronische Lungenerkrankung oder chronische Lebererkrankung, einschließlich chronischer Alkoholismus“ wurde mit der Spalte „Angeborene Immunschwäche, Leukämie, Lymphom, generalisiertes Malignom, Therapie mit Alkylierungsmitteln, Antimetaboliten, Liquoraustritt, Bestrahlung oder großen Mengen an Kortikosteroiden“ auf der Liste der medizinischen/sonstigen Indikationen (Abbildung 2) vertauscht, so dass die Kontraindikationen für MMR- und Varizellen-Impfstoffe nun nebeneinander stehen.
- Die Zeile für die Varizellen-Impfung wurde in beiden Abbildungen nach oben verschoben (d. h., unmittelbar nach dem MMR-Impfstoff), da der Impfstoff nun allgemein für bestimmte Altersgruppen empfohlen wird.
- Meningokokken-Impfstoff wurde in die Liste der medizinischen/anderen Indikationen aufgenommen (Abbildung 2). Die Fußnote wurde überarbeitet, um die kürzlich veröffentlichten ACIP-Empfehlungen für diesen Impfstoff zu berücksichtigen (1).
- Die Fußnote zu Tetanus und Diphtherie (Nr. 1) wurde umformuliert.
- Die Fußnote zu Windpocken (Nr. 3) wurde entsprechend den ACIP-Empfehlungen vom Juni 2005 umformuliert.
- Die Fußnote zur Influenza (Nr. 4) wurde überarbeitet, um die neueste Hochrisikokondition hinzuzufügen: neuromuskuläre Erkrankungen, die die Atemfunktion beeinträchtigen (2).
- Eine zehnte Fußnote wurde hinzugefügt, die sich auf die Impfung gegen Haemophilus influenzae Typ b für Bevölkerungsgruppen mit hohem Risiko bezieht (d.h.,
Der Impfplan für Erwachsene ist auf Englisch und Spanisch unter http://www.cdc.gov/nip/recs/adult-schedule.htm verfügbar. Allgemeine Informationen über Impfungen für Erwachsene, einschließlich Empfehlungen zur Impfung von Personen mit HIV und anderen immunsuppressiven Erkrankungen, sind bei den staatlichen und lokalen Gesundheitsämtern und beim National Immunization Program unter http://www.cdc.gov/nip erhältlich. Erklärungen zu Impfstoffen sind unter http://www.cdc.gov/nip/publications/vis verfügbar. ACIP-Erklärungen für jeden empfohlenen Impfstoff können auf der Website des National Immunization Program unter http://www.cdc.gov/nip/publications/acip-list.htm eingesehen, heruntergeladen und ausgedruckt werden. Anweisungen zur Meldung von unerwünschten Ereignissen an das Vaccine Adverse Event Reporting System finden Sie unter http://www.vaers.hhs.gov oder telefonisch unter 800-822-7967.
- CDC. Prävention und Kontrolle von Meningokokken-Erkrankungen: Empfehlungen des Beratenden Ausschusses für Immunisierungspraktiken (ACIP). MMWR 2005;54(No. RR-7).
- CDC. Prävention und Kontrolle der Influenza: Empfehlungen des Beratenden Ausschusses für Immunisierungspraktiken (ACIP). MMWR 2005;54(No. RR-8).
Abbildung 1
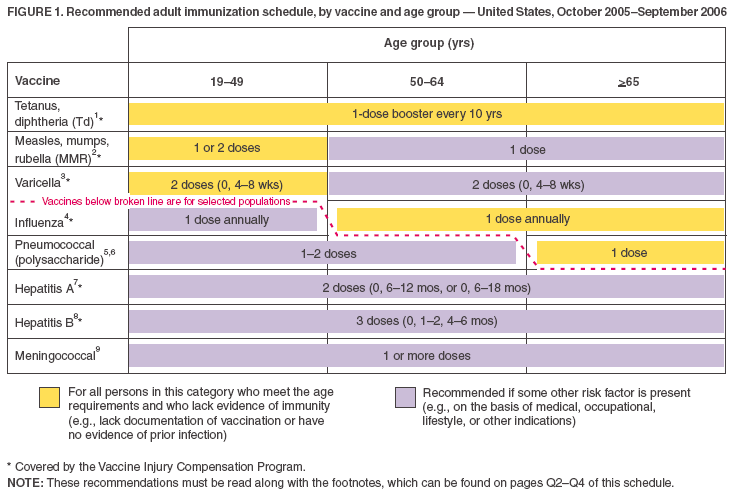
Zum Anfang zurückkehren.
Abbildung 2

Zum Anfang zurückkehren.
Genehmigt durch das Advisory Committee on Immunization Practices, das American College of Obstetricians and Gynecologists, und die American Academy of Family Physicians
1. Impfung gegen Tetanus und Diphtherie (Td). Erwachsene mit unklarer Vorgeschichte einer vollständigen Erstimpfungsserie mit Diphtherie- und Tetanustoxoid-haltigen Impfstoffen sollten eine Erstimpfungsserie mit kombiniertem Td-Toxoid erhalten. Eine Primärimpfserie für Erwachsene besteht aus 3 Dosen; die ersten beiden Dosen werden im Abstand von mindestens 4 Wochen verabreicht, die dritte Dosis 6 bis 12 Monate nach der zweiten. Eine Dosis wird verabreicht, wenn die Person die Primärserie erhalten hat und die letzte Impfung >10 Jahre zurückliegt. Empfehlungen für die Verabreichung von Td als Prophylaxe bei der Wundbehandlung finden Sie in der ACIP-Erklärung (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). Die American College of Physicians Task Force on Adult Immunization befürwortet eine zweite Option für die Anwendung von Td bei Erwachsenen: eine einmalige Td-Auffrischung im Alter von 50 Jahren für Personen, die die vollständige pädiatrische Impfserie, einschließlich der Auffrischung für Jugendliche/junge Erwachsene, abgeschlossen haben. Ein neu zugelassener Tetanus-Diphtherie-azellulärer-Pertussis-Impfstoff ist für Erwachsene verfügbar. Die ACIP-Empfehlungen für seine Verwendung werden veröffentlicht.
2. Masern, Mumps, Röteln (MMR) Impfung. Masernkomponente: Erwachsene, die vor 1957 geboren wurden, können als immun gegen Masern angesehen werden. Erwachsene, die während oder nach 1957 geboren wurden, sollten >1 Dosis MMR erhalten, es sei denn, es besteht eine medizinische Kontraindikation, der Nachweis einer >1 Dosis, eine auf der Diagnose eines Gesundheitsdienstleisters beruhende Vorgeschichte von Masern oder ein Labornachweis der Immunität. Eine zweite MMR-Dosis wird für Erwachsene empfohlen, die 1) kürzlich Masern ausgesetzt waren oder sich in einer Ausbruchssituation befanden; 2) zuvor mit einem abgetöteten Masernimpfstoff geimpft wurden; 3) zwischen 1963 und 1967 mit einem unbekannten Typ von Masernimpfstoff geimpft wurden; 4) Studenten in postsekundären Bildungseinrichtungen sind; 5) in einer Gesundheitseinrichtung arbeiten; oder 6) eine internationale Reise planen. HIV-Infizierte mit schwerer Immunsuppression dürfen nicht mit MMR oder anderen masernhaltigen Impfstoffen geimpft werden. Mumps-Komponente: 1 Dosis MMR-Impfstoff sollte für den Schutz von Personen ausreichen, die während oder nach 1957 geboren wurden und bei denen eine Mumps-Erkrankung aufgrund der Diagnose eines Gesundheitsdienstleisters nicht bekannt ist oder bei denen kein Labornachweis der Immunität vorliegt. Röteln-Komponente: Verabreichung von 1 Dosis MMR-Impfstoff an Frauen, deren Röteln-Impfanamnese unzuverlässig ist oder die keinen Labornachweis der Immunität haben. Bei Frauen im gebärfähigen Alter, unabhängig vom Geburtsjahr, routinemäßig die Rötelnimmunität feststellen und die Frauen über das kongenitale Rötelnsyndrom beraten. Frauen, die schwanger sind oder innerhalb von 4 Wochen nach Erhalt des Impfstoffs schwanger werden könnten, dürfen nicht geimpft werden. Frauen, bei denen keine Immunität nachgewiesen werden kann, sollten nach Abschluss oder Beendigung der Schwangerschaft und vor der Entlassung aus der Gesundheitseinrichtung eine MMR-Impfung erhalten.
3. Varizellen-Impfung. Die Varizellen-Impfung wird für alle Erwachsenen empfohlen, die keine Immunität gegen Varizellen nachweisen können. Besondere Aufmerksamkeit sollte denjenigen gewidmet werden, die 1) engen Kontakt zu Personen mit hohem Risiko für eine schwere Erkrankung haben (Mitarbeiter des Gesundheitswesens und Familienangehörige von immungeschwächten Personen) oder 2) einem hohen Expositions- oder Übertragungsrisiko ausgesetzt sind (z. B. Lehrer von Kleinkindern, Kinderbetreuungspersonal, Bewohner und Mitarbeiter von Einrichtungen, einschließlich Justizvollzugsanstalten, Studenten, Militärangehörige, Jugendliche und Erwachsene, die in Haushalten mit Kindern leben, nicht schwangere Frauen im gebärfähigen Alter und Auslandsreisende). Der Nachweis der Immunität gegen Varizellen bei Erwachsenen umfasst eine der folgenden Voraussetzungen: 1) dokumentierte altersgemäße Varizellenimpfung (d. h. 1 Dosis vor dem 13. Lebensjahr oder 2 Dosen nach dem 13. Lebensjahr); 2) vor 1966 in den USA geboren oder Vorgeschichte einer Varizellenerkrankung vor 1966 bei nicht in den USA geborenen Personen; 3) Vorgeschichte einer Varizellenerkrankung vor 1966 bei nicht in den USA geborenen PersonenGeboren vor 1966 oder Varizellen-Erkrankung vor 1966 bei nicht in den USA geborenen Personen; 3) Varizellen-Erkrankung in der Anamnese aufgrund der Diagnose eines Gesundheitsdienstleisters oder der elterlichen oder eigenen Angabe einer typischen Varizellen-Erkrankung bei Personen, die zwischen 1966 und 1997 geboren wurden (bei Patienten, die einen atypischen, milden Fall in der Anamnese angeben, sollten die Gesundheitsdienstleister entweder nach einer epidemiologischen Verbindung zu einem typischen Varizellen-Fall oder nach einem Nachweis für eine Laborbestätigung suchen, wenn diese zum Zeitpunkt der akuten Erkrankung durchgeführt wurde); 4) Herpes-Zoster-Erkrankung in der Anamnese aufgrund der Diagnose eines Gesundheitsdienstleisters; oder 5) Nachweis der Immunität im Labor. Frauen, die schwanger sind oder innerhalb von 4 Wochen nach Erhalt des Impfstoffs schwanger werden könnten, dürfen nicht geimpft werden. Bei schwangeren Frauen ist der Nachweis einer Varizellenimmunität zu erbringen. Frauen, bei denen keine Immunität nachgewiesen werden kann, sollten nach Abschluss oder Beendigung der Schwangerschaft und vor der Entlassung aus der Gesundheitseinrichtung Dosis 1 des Varizellen-Impfstoffs erhalten. Dosis 2 sollte 4 bis 8 Wochen nach Dosis 1 verabreicht werden.
4. Grippeimpfung. Medizinische Indikationen: chronische Erkrankungen des kardiovaskulären oder pulmonalen Systems, einschließlich Asthma; chronische Stoffwechselerkrankungen, einschließlich Diabetes mellitus, Nierenfunktionsstörungen, Hämoglobinopathien oder Immunsuppression (einschließlich medikamentös oder durch HIV verursachte Immunsuppression); jeder Zustand (z. B., kognitive Störungen, Rückenmarksverletzungen, Anfallsleiden oder andere neuromuskuläre Störungen), die die Atmungsfunktion oder die Handhabung von Atemwegssekreten beeinträchtigen oder das Aspirationsrisiko erhöhen können, sowie Schwangerschaft während der Grippesaison. Es gibt keine Daten über das Risiko einer schweren oder komplizierten Influenza-Erkrankung bei Personen mit Asplenie; die Influenza ist jedoch ein Risikofaktor für bakterielle Sekundärinfektionen, die bei Personen mit Asplenie schwere Erkrankungen verursachen können. Berufliche Indikationen: Beschäftigte im Gesundheitswesen und Angestellte von Langzeitpflegeeinrichtungen und Einrichtungen für betreutes Wohnen. Weitere Indikationen: Bewohner von Pflegeheimen und anderen Einrichtungen für Langzeitpflege und betreutes Wohnen; Personen, die Influenza auf Personen mit hohem Risiko übertragen können (d. h. Haushaltskontakte und Betreuungspersonen von Kindern im Alter von 0 bis 23 Monaten oder Personen aller Altersgruppen mit hohem Risiko), sowie alle Personen, die sich impfen lassen möchten. Gesunden, nicht schwangeren Personen im Alter von 5 bis 49 Jahren ohne Hochrisikobedingungen, die keine Kontaktpersonen von schwer immungeschwächten Personen in speziellen Pflegestationen sind, kann anstelle des inaktivierten Impfstoffs ein intranasal verabreichter Influenza-Impfstoff (FluMist®) verabreicht werden.
5. Pneumokokken-Polysaccharid-Impfung. Medizinische Indikationen: chronische Erkrankungen des Lungensystems (außer Asthma); Herz-Kreislauf-Erkrankungen; Diabetes mellitus; chronische Lebererkrankungen, einschließlich Lebererkrankungen infolge von Alkoholmissbrauch (z. B. Zirrhose); chronisches Nierenversagen oder nephrotisches Syndrom; funktionelle oder anatomische Asplenie (z. B., Sichelzellenkrankheit oder Splenektomie); immunsuppressive Zustände (z. B. angeborener Immundefekt, HIV-Infektion, Leukämie, Lymphom, multiples Myelom, Hodgkin-Krankheit, generalisierte Malignität oder Organ- oder Knochenmarktransplantation); Chemotherapie mit Alkylierungsmitteln, Antimetaboliten oder langfristigen systemischen Kortikosteroiden; und Cochlea-Implantate. Andere Indikationen: Alaska Natives und bestimmte indianische Bevölkerungsgruppen; Bewohner von Pflegeheimen und anderen Langzeit-Pflegeeinrichtungen.
6. Auffrischungsimpfung mit Pneumokokken-Polysaccharid-Impfstoff. Einmalige Auffrischungsimpfung nach 5 Jahren bei Personen mit chronischer Niereninsuffizienz oder nephritischem Syndrom, funktioneller oder anatomischer Asplenie (z. B. Sichelzellkrankheit oder Splenektomie), immunsuppressiven Erkrankungen (z. B., angeborener Immundefekt, HIV-Infektion, Leukämie, Lymphom, multiples Myelom, Morbus Hodgkin, generalisierte Malignität oder Organ- oder Knochenmarktransplantation) oder Chemotherapie mit Alkylierungsmitteln, Antimetaboliten oder langfristigen systemischen Kortikosteroiden. Für Personen im Alter von >65 Jahren, einmalige Auffrischungsimpfung, wenn sie >5 Jahre zuvor geimpft wurden und zum Zeitpunkt der Erstimpfung <65 Jahre alt waren.
7. Hepatitis A-Impfung. Medizinische Indikationen: Personen mit Gerinnungsfaktorkrankheiten oder chronischen Lebererkrankungen. Verhaltensbedingte Indikationen: Männer, die Sex mit Männern haben oder Konsumenten illegaler Drogen. Berufliche Indikationen: Personen, die mit Hepatitis-A-Virus (HAV)-infizierten Primaten oder mit HAV in einem Forschungslabor arbeiten. Weitere Indikationen: Personen, die in Länder mit hoher oder mittlerer Endemizität von Hepatitis A reisen oder dort arbeiten (Liste der Länder siehehttp://www.cdc.gov/travel/diseases.htm#hepa), sowie alle Personen, die Immunität erlangen möchten. Die aktuellen Impfstoffe sollten in einer 2-Dosis-Serie entweder im Alter von 0 und 6-12 Monaten oder 0 und 6-18 Monaten verabreicht werden. Wenn der kombinierte Hepatitis-A- und Hepatitis-B-Impfstoff verwendet wird, sind 3 Dosen im Alter von 0, 1 und 6 Monaten zu verabreichen.
8. Hepatitis-B-Impfung. Medizinische Indikationen: Hämodialysepatienten (spezielle Formulierung oder zwei 20-µg/ml-Dosen verwenden) oder Patienten, die Gerinnungsfaktorkonzentrate erhalten. Berufliche Indikationen: Mitarbeiter des Gesundheitswesens und der öffentlichen Sicherheit, die am Arbeitsplatz mit Blut in Berührung kommen, sowie Personen in der Ausbildung in medizinischen, zahnmedizinischen, pflegerischen, labortechnischen und anderen verwandten Gesundheitsberufen. Verhaltensindikationen: Injektionsdrogenkonsumenten; Personen, die in den letzten 6 Monaten mehr als einen Sexualpartner hatten; Personen mit einer kürzlich erworbenen sexuell übertragbaren Krankheit (STD); und Männer, die Sex mit Männern haben. Weitere Indikationen: Haushaltskontakte und Sexualpartner von Personen mit chronischer Hepatitis-B-Virusinfektion (HBV); Klienten und Mitarbeiter von Einrichtungen für Menschen mit Entwicklungsstörungen; alle Klienten von STD-Kliniken; Insassen von Justizvollzugsanstalten; und Auslandsreisende, die sich länger als 6 Monate in Ländern mit hoher oder mittlerer Prävalenz chronischer HBV-Infektionen aufhalten (Liste der Länder siehe http://www.cdc.gov/travel/diseases.htm#hepa).
9. Meningokokken-Impfung. Medizinische Indikationen: Erwachsene mit anatomischer oder funktioneller Asplenie oder terminalen Komplementkomponentenmängeln. Andere Indikationen: Studenten im ersten Studienjahr, die in Wohnheimen leben; Mikrobiologen, die routinemäßig Isolaten von Neisseria meningitidis ausgesetzt sind; Militärrekruten; und Personen, die in Länder reisen oder sich dort aufhalten, in denen die Meningokokken-Erkrankung hyperendemisch oder epidemisch ist (z. B. der „Meningitis-Gürtel“ in Afrika südlich der Sahara während der Trockenzeit), insbesondere wenn ein längerer Kontakt mit der örtlichen Bevölkerung besteht. Die Regierung Saudi-Arabiens schreibt die Impfung für alle Reisenden vor, die während der jährlichen Hadsch nach Mekka reisen. Meningokokken-Konjugatimpfstoff wird für Erwachsene, die eine der oben genannten Indikationen erfüllen und <55 Jahre alt sind, bevorzugt, obwohl Meningokokken-Polysaccharid-Impfstoff (MPSV4) eine akzeptable Alternative ist. Eine Auffrischungsimpfung nach 5 Jahren kann für Erwachsene angezeigt sein, die zuvor mit MPSV4 geimpft wurden und weiterhin ein hohes Infektionsrisiko haben (z. B. Personen, die in Gebieten wohnen, in denen die Krankheit epidemisch ist).
10. Ausgewählte Erkrankungen, für die der Impfstoff gegen Haemophilus influenzae Typ b (Hib) verwendet werden kann. Hib-Konjugatimpfstoffe sind für Kinder im Alter von 6 bis 71 Monaten zugelassen. Es liegen keine Wirksamkeitsdaten vor, die eine Empfehlung für die Verwendung des Hib-Impfstoffs bei älteren Kindern und Erwachsenen mit chronischen Erkrankungen, die mit einem erhöhten Risiko für eine Hib-Erkrankung verbunden sind, begründen könnten. Studien deuten jedoch auf eine gute Immunogenität bei Patienten mit Sichelzellanämie, Leukämie oder HIV-Infektion oder nach einer Splenektomie hin; die Verabreichung des Impfstoffs an diese Patienten ist nicht kontraindiziert.
Der empfohlene Impfplan für Erwachsene wurde vom Beratungsausschuss für Immunisierungspraktiken, dem American College of Obstetricians and Gynecologists und der American Academy of Family Physicians genehmigt. Das standardmäßige MMWR-Fußnotenformat wurde für die Veröffentlichung dieses Plans geändert.
Vorgeschlagene Zitierung: Centers for Disease Control and Prevention. Empfohlener Impfplan für Erwachsene—Vereinigte Staaten, Oktober 2005–September 2006. MMWR 2005;54:Q1–Q4.
Dieser Impfplan enthält die empfohlenen Altersgruppen und medizinischen Indikationen für die routinemäßige Verabreichung der derzeit zugelassenen Impfstoffe für Personen im Alter von >19 Jahren. Zugelassene Kombinationsimpfstoffe können immer dann verwendet werden, wenn einer der Bestandteile der Kombination indiziert ist und wenn die anderen Bestandteile des Impfstoffs nicht kontraindiziert sind. Detaillierte Empfehlungen finden Sie in den Packungsbeilagen der Hersteller und in den vollständigen Erklärungen des ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Melden Sie alle klinisch bedeutsamen Reaktionen nach der Impfung an das Vaccine Adverse Event Reporting System (VAERS). Meldeformulare und Anweisungen zur Einreichung einer VAERS-Meldung sind telefonisch unter 800-822-7967 oder auf der VAERS-Website unter http://www.vaers.hhs.gov erhältlich.
Informationen zur Einreichung einer Klage im Rahmen des Vaccine Injury Compensation Program finden Sie unter http://www.hrsa.gov/osp/vicp oder telefonisch unter 800-338-2382. Um eine Klage wegen Impfschäden einzureichen, wenden Sie sich an den U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, Telefon 202-357-6400.
Zusätzliche Informationen über die oben aufgeführten Impfstoffe und Kontraindikationen für die Impfung sind auch unter http://www.cdc.gov/nip oder beim CDC-INFO Contact Center unter 800-CDC-INFO (232-4636) in englischer und spanischer Sprache erhältlich, 24 Stunden am Tag, 7 Tage die Woche.
Die Verwendung von Markennamen und kommerziellen Quellen dient nur der Identifizierung und impliziert keine Billigung durch das US-Gesundheitsministerium.Verweise auf Nicht-CDC-Websites im Internet werden als Service für MMWR-Leser bereitgestellt und stellen keine Billigung dieser Organisationen oder ihrer Programme durch das CDC oder das US-Gesundheitsministerium dar oder implizieren diese. Die CDC ist nicht für den Inhalt der Seiten verantwortlich, die auf diesen Sites zu finden sind. Die im MMWR aufgeführten URL-Adressen waren zum Zeitpunkt der Veröffentlichung aktuell.
Haftungsausschluss Alle HTML-Versionen von MMWR-Artikeln sind elektronische Konvertierungen von ASCII-Text in HTML. Diese Umwandlung kann zu Zeichenübersetzungen oder Formatfehlern in der HTML-Version geführt haben. Benutzer sollten sich nicht auf dieses HTML-Dokument verlassen, sondern werden für den offiziellen Text, die Abbildungen und Tabellen auf die elektronische PDF-Version und/oder die Original-Papierausgabe des MMWR verwiesen. Ein Originalexemplar dieser Ausgabe in Papierform kann beim Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371, angefordert werden; Telefon: (202) 512-1800. Die aktuellen Preise sind beim GPO zu erfragen.
**Fragen oder Mitteilungen über Formatierungsfehler sind an [email protected] zu richten.
Datum der letzten Überprüfung: 10/13/2005
