Einführung
Divertikelkrankheit des Dickdarms ist die häufigste Erkrankung des Dickdarms in der westlichen Welt. Die Prävalenz der Divertikelkrankheit hat im letzten Jahrhundert weltweit zugenommen, wahrscheinlich aufgrund von Veränderungen im Lebensstil wie Rauchen, Übergewicht, Bewegungsmangel und ballaststoffarmer Ernährung. Die Prävalenz nimmt mit dem Alter zu und reicht von etwa 5 % bei Erwachsenen, die jünger als 40 Jahre sind, bis zu 50-70 % bei Menschen, die 80 Jahre oder älter sind; 80 % der Patienten, die an Divertikulitis erkranken, sind 50 Jahre oder älter. Die Anzahl der Divertikel kann von einzeln bis zu Hunderten reichen. Sie haben in der Regel einen Durchmesser von 5-10 mm, können aber auch größer als 2 cm sein. Divertikulose tritt bei mehr als 90 % der Patienten vor allem im Sigma und im absteigenden Dickdarm auf, kann aber in unterschiedlichem Ausmaß auch im übrigen Dickdarm vorkommen.1
Es gibt mehrere divertikelbezogene Begriffe, die in dieser Übersicht verwendet werden. Das Vorhandensein von Divertikeln im Dickdarm ohne erkennbare Entzündung wird als Divertikulose oder unkomplizierte Divertikelkrankheit (UDD) bezeichnet. Sie kann symptomatisch oder asymptomatisch sein. Der Begriff „akute Kolondivertikulitis“ (ACD) bezeichnet eine Entzündung der Divertikel, die zu Komplikationen führen kann oder auch nicht (komplizierte ACD). Es gibt auch die chronische Divertikulitis, die durch rezidivierende Divertikulitis oder durch die Entwicklung einer segmentalen Kolitis in Verbindung mit den Divertikeln entsteht. Zusammenfassend lässt sich sagen, dass das klinische Spektrum der Divertikelkrankheit breit gefächert ist.
Studien über den natürlichen Krankheitsverlauf weisen darauf hin, dass die große Mehrheit der Patienten mit Divertikeln (etwa 80 %) ihr Leben lang symptomlos bleibt. Von den 15-20 %, die Symptome entwickeln, kommt es bei etwa 1/4 zu einer symptomatischen, schmerzhaften Divertikelerkrankung ohne Entzündung und bei bis zu 10-25 % zu einer ACD-Episode. Etwa 1-2 % erfordern einen Krankenhausaufenthalt und 0,5 % eine Operation. Divertikel sind für die Mehrzahl (24-42 %) der Blutungen im unteren Gastrointestinaltrakt verantwortlich.2-4
Physiopathologie und Symptomentwicklung
Ein Kolondivertikel ist eine Herniation von Mukosa und Submukosa, die einer Schwachstelle entspricht, an der die Vasa recti die Tunica muscularis durchdringen. Die pathogenetischen Mechanismen der Divertikelkrankheit sind immer noch nicht vollständig geklärt, es wird jedoch allgemein anerkannt, dass sie wahrscheinlich mit komplexen Wechselwirkungen zwischen Ernährung, Kolonmikrobiota, genetischen Faktoren, Kolonmotilität und Struktur zusammenhängen, die im Laufe der Zeit zur Bildung von Kolondivertikeln führen.5 Siehe Abb. 1. 1971 veröffentlichten Painter und Burkitt ihre berühmte Hypothese, dass die Divertikelkrankheit durch einen übermäßigen Druck im Dickdarm infolge einer Segmentierung aufgrund einer unzureichenden Aufnahme von Ballaststoffen verursacht wird. Als Reaktion auf den erhöhten intraluminalen Druck können sich Ausstülpungen bilden, die an potenziell schwachen Stellen hervortreten.6 Eine Stauung oder Obstruktion in den enghalsigen Divertikeln kann zu einer bakteriellen Überwucherung und einer lokalen Gewebsischämie führen, die letztlich eine Perforation zur Folge hat.7 Seitdem wurde in zahlreichen Beobachtungsstudien versucht, die mögliche Wirkung von Ballaststoffen auf die Prävention von Divertikelerkrankungen nachzuweisen. Die meisten von ihnen kamen zu dem Schluss, dass das UDD-Risiko umgekehrt mit der Ballaststoffzufuhr zusammenhängt.8-10 Aufgrund dieser Erkenntnisse wird in den meisten aktuellen Leitlinien und Positionspapieren eine ballaststoffreiche Ernährung zur Vorbeugung von Divertikelkrankheiten empfohlen.11-15 Diese Hypothese wurde jedoch in letzter Zeit in Frage gestellt, da (1) der umgekehrte Zusammenhang zwischen Ballaststoffzufuhr und Divertikulose in einigen neueren epidemiologischen Studien16,17 in Frage gestellt wurde und (2) neue pathogene Hypothesen wie die neuropathische und myopathische Hypothese auftauchen.18-22 Andere Faktoren, die mit einem erhöhten Risiko für Divertikelkrankheiten in Verbindung gebracht werden, sind körperliche Inaktivität, Verstopfung, Übergewicht und Rauchen.23-27
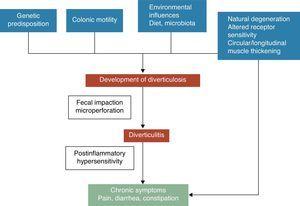
Die Entwicklung von Symptomen bei der Divertikelkrankheit hängt wahrscheinlich mit komplexen Wechselwirkungen zwischen genetischen Merkmalen, der Struktur des Dickdarms, der Darmmotilität, einer geringgradigen Entzündung und einer postinflammatorischen Hypersensibilität zusammen.
Der Zusammenhang zwischen unkomplizierter Divertikelkrankheit (UDD) und Symptomen ist ungewiss. Einiges deutet darauf hin, dass die schmerzhafte Divertikelkrankheit mit einer Entzündung und deren Auswirkungen auf die neuromuskuläre Funktion im Dickdarm zusammenhängt.22-28 Das Vorhandensein einer chronischen, geringgradigen Darmentzündung würde eine sensorisch-motorische Dysfunktion hervorrufen, die zur Entwicklung und/oder Persistenz von Symptomen führt. Veränderungen der intestinalen Mikroflora könnten einer der mutmaßlichen Mechanismen sein, die für eine geringgradige Entzündung verantwortlich sind. Eine bakterielle Überwucherung, die durch die Stauung von Fäkalien in den Divertikeln begünstigt wird, könnte zu einer chronischen geringgradigen Entzündung beitragen, die sowohl intrinsische primär efferente als auch extrinsische primär afferente Neuronen sensibilisiert. Diese Veränderungen könnten zu einer Hypertrophie der glatten Muskulatur und einer erhöhten Empfindlichkeit gegenüber abdominaler Dehnung und schließlich zur Entwicklung von Symptomen führen.3,22 Siehe Abb. 1.
Wie bereits erwähnt, bleiben die meisten Menschen mit Kolondivertikulose symptomlos, können aber schließlich Komplikationen wie ACD oder Divertikelblutungen entwickeln. In diesem Artikel konzentrieren wir uns auf die ACD. Die klinische Manifestation dieses Ereignisses hängt von einer Reihe von Faktoren ab, u. a. von der Größe der Perforation, dem Ausmaß der extrakolonalen Kontamination und der Fähigkeit des Körpers, diese Kontamination einzudämmen.29,30
Behandlung der DivertikelkrankheitBehandlung der unkomplizierten Divertikelkrankheit (UDD)
Bei Patienten mit asymptomatischer UDD2 kann eine ballaststoffreiche Ernährung empfohlen werden, da sie möglicherweise einen prophylaktischen Nutzen bei der Verhinderung von symptomatischer UDD und Komplikationen hat. Es gibt keine Belege dafür, dass andere Medikamente bei diesen Patienten nützlich sind.
Es gibt mehr Belege für den Nutzen einer Behandlung bei symptomatischer UDD. Das häufigste Symptom sind Bauchschmerzen, die sich durch Essen verschlimmern und durch Stuhlgang oder Blähungen abklingen können. Weitere Symptome sind Übelkeit, Durchfall, Verstopfung und Blähungen. Mehr als 61 % der Patienten mit symptomatischer UDD, die keine therapeutischen Maßnahmen ergreifen, um ein Wiederauftreten der Symptome zu verhindern, werden innerhalb eines Jahres symptomatisch, und etwa 4 % entwickeln Komplikationen.31
Fünf Wirkstoffe wurden für die Behandlung vorgeschlagen (siehe Abb. 2):

Behandlung der unkomplizierten Divertikelkrankheit. Wirkmechanismen.
A) Ballaststoffreiche Ernährung oder Quellstoffe
Einige randomisierte kontrollierte Studien (RCT) und andere Interventionsstudien bewerten die Wirkung von Ballaststoffen bei symptomatischer UDD, jedoch mit uneinheitlichen Ergebnissen.32-37 In jedem Fall werden Ballaststoffe in den meisten aktuellen Leitlinien und Positionspapieren zur Vorbeugung und Behandlung von symptomatischer UDD sowie zur Vorbeugung von ACD empfohlen.11-15
B) Antibiotikatherapie
Die Gründe für den Einsatz von Antibiotika bei symptomatischer UDD sind nicht eindeutig geklärt. Jüngste Studien deuten darauf hin, dass Veränderungen der Darmmikrobiota (bakterielle Überwucherung des Darms) aufgrund einer übermäßigen Produktion von Darmgasen durch die Fermentation von Kohlenhydraten zur Entwicklung der Symptome beitragen könnten. Um systematische Wirkungen zu vermeiden, scheinen schlecht absorbierte antimikrobielle Mittel, die gegen Darmpathogene wirken, aber nur ein minimales Risiko für systematische Toxizität oder Nebenwirkungen haben, die am besten geeigneten Antibiotika zu sein. Rifaximin wurde vorgeschlagen.
Rifaximin
Rifaximin ist ein nicht systematisches Rifamycin-Analogon mit einem breiten Wirkungsspektrum in vitro. Rifaximin kann die Stoffwechselaktivität der Darmflora vermindern, die Fäkalienmasse erhöhen und eine bakterielle Überwucherung beseitigen. Dieses Antibiotikum weist ein hohes Sicherheits- und Verträglichkeitsprofil auf.33,38 Der Plasmaspiegel von Rifaximin ist minimal, so dass nicht-enterische Krankheitserreger keinem Selektionsdruck ausgesetzt sind und das Risiko einer bakteriellen Resistenz gering ist.39 In drei offenen und zwei doppelblinden RCTs40-44 wurde die Wirksamkeit der zyklischen Verabreichung von Rifaximin und Ballaststoffen bei der Verringerung der Symptome im Vergleich zu Ballaststoffen allein untersucht. Diese Studien wurden in einer systematischen Übersichtsarbeit und zwei Metaanalysen analysiert.44-46 Sie kamen zu dem Schluss, dass die kombinierte Behandlung bei Patienten mit UDD nach einem Jahr zu einer wirksamen Linderung der Symptome führt. 35 % der Patienten, die nur mit Ballaststoffen behandelt wurden, waren asymptomatisch, gegenüber 64 % in den Gruppen mit kombinierter Behandlung. Die Zahl der erforderlichen Behandlungen lag bei drei für Rifaximin im Vergleich zu Placebo, um die Symptome zu lindern, und bei neun, um Komplikationen zu vermeiden. Zusammenfassend wurden die besten Ergebnisse mit einer Kombination aus löslichen Ballaststoffen wie Glucomannan und Rifaximin 1 Woche pro Monat erzielt.
C) Probiotika
Probiotika sind lebende Mikroorganismen, die die Darmflora wiederherstellen können, die bei der Divertikelkrankheit aufgrund von Stase und verkürzter Kolontransitzeit verändert sein kann.47 Leider gibt es nur wenige Daten über ihren Einsatz bei symptomatischer UDD und die meisten Studien sind klein und unkontrolliert. Die meisten von ihnen zeigen eine Verbesserung der Symptome.48-50
Probiotika wurden auch in Kombination mit 5-Aminosalicylat (5-ASA) untersucht. Tursi und Kollegen haben drei RCTs durchgeführt, in denen 5-ASA allein, Probiotika allein oder eine Kombinationstherapie verglichen wurden.51-53 Sowohl 5-ASA als auch Probiotika schienen bei der Vorbeugung von symptomatischer UDD wirksam zu sein, aber ihre Kombination war besser. Eine kürzlich von derselben wissenschaftlichen Gruppe veröffentlichte doppelbindige RCT kam zu dem Schluss, dass sowohl zyklisches Mesalazin als auch Lactobacillus casei subsp DG, insbesondere in Kombination, besser als Placebo zu sein scheinen, um die Remission der symptomatischen UDD aufrechtzuerhalten.54 Zusammenfassend lässt sich jedoch sagen, dass die schlechten Studiendesigns und die geringe Größe der Studien keine definitiven Schlussfolgerungen zulassen.
D) 5-ASA: Mesalazin
Mesalazin hat entzündungshemmende und antioxidative Wirkungen. Im Jahr 2010 veröffentlichten Gatta et al.55 einen systematischen Cochrane-Review, in dem die Rolle von 5-ASA bei Patienten mit Divertikelkrankheit bewertet wurde. Die Autoren kamen zu dem Schluss, dass 5-ASA bei der Behandlung dieser Erkrankung wirksam sein kann und dass die tägliche Einnahme von Mesalazin zur Verhinderung von Rückfällen besser ist als eine zyklische Verabreichung. Qualitativ hochwertige, gut konzipierte RCTs sind erforderlich, um ihre Beobachtungen zu bestätigen. Die erste placebokontrollierte Doppelblindstudie ergab, dass Mesalazin bei Patienten mit akuter UDD eine wirksame Schmerzlinderung bewirkt.56 Außerdem gibt es zwei interessante RCTs, die einen Vorteil für Mesalazin im Vergleich zu Rifaximin bei der Verhinderung eines symptomatischen Rückfalls und einen ähnlichen Erfolg bei der Aufrechterhaltung der langfristigen Remission im Vergleich zum Probiotikum Lactobacillus casei zeigten.53,57
E) Anticholinergika/Antispasmodika
Die Hüftmotilität des Dickdarms bei Divertikulose lässt vermuten, dass Antispasmodika wie Dicyclomin und Hyoscyamin die Symptome verbessern könnten, indem sie die Muskelkontraktion verringern. Es gibt jedoch keine RCTs, die diesen Nutzen bestätigen.
F) NSAID-Behandlung vermeiden
Mehrere kontrollierte Studien haben gezeigt, dass NSAIDs ein Risikofaktor für die Entwicklung von Symptomen, ACD, Perforation und Blutungen sind.7,58-60 NSAID-Anwender haben ein höheres Risiko, symptomatische Divertikelkrankheiten zu entwickeln als Nicht-Anwender (RR: 1,5, CI 95%: 1,1-2,1).58 Und bei Patienten mit komplizierten Divertikelkrankheiten wurde ein höherer NSAID-Konsum festgestellt als bei Kontrollpersonen ohne Erkrankung. Es wurde postuliert, dass dieses erhöhte Risiko auf eine Schädigung der Schleimhaut zurückzuführen ist, die zu einer Beeinträchtigung der Barrierefunktion der Dickdarmschleimhaut führt und die Verlagerung von Bakterien ermöglicht, die eine Entzündung hervorrufen.
G) Vitamin-D-Spiegel
Es scheint, dass die Häufigkeit von ACD mit geografischen und saisonalen Schwankungen in Verbindung gebracht wird. Aus diesem Grund führten Maguire et al. zwei interessante Beobachtungsstudien durch, die zeigten, dass ein niedriger Vitamin-D-Spiegel und eine geringe UV-Lichtexposition (die UV-Exposition bestimmt den Vitamin-D-Status) mit einem deutlich höheren ACD-Risiko verbunden sind. Bevor eine Empfehlung ausgesprochen werden kann, sind weitere qualitativ hochwertige Studien erforderlich.61,62
Behandlung der akuten Kolondivertikulitis (ACD)
Obwohl die meisten Menschen mit Divertikulose asymptomatisch bleiben, entwickeln schätzungsweise 10-25 % von ihnen eine Episode einer linken ACD.63 Im Allgemeinen ist die klinische Diagnose nicht genau genug, so dass radiologische Verfahren angezeigt sind. Bei Patienten mit leichten Symptomen (in den meisten Fällen) und ohne Anzeichen einer komplizierten ACD kann die Kombination aus Schmerzen im linken Unterbauch, dem Fehlen von Erbrechen und einem C-reaktiven Protein >50mg/l für die Diagnose ausreichen.64,65 Wenn eine Bildgebung indiziert ist, kann wahrscheinlich eine bedingte Strategie mit Ultraschall als erster Technik und gefolgt von Computertomographie (CT), wenn der Ultraschall nicht schlüssig oder zweifelhaft ist, die effektivste Vorgehensweise darstellen. Die Zahl der CT-Untersuchungen kann um 50 % reduziert werden. 1978 schlugen Hinchey et al. eine Klassifikation der ACD vor, die später modifiziert wurde.66,67 Sie unterscheidet fünf Stadien der ACD: Stadium 0, klinisch milde Divertikulitis, Stadium I (a: perikolische Entzündung und b: Abzess
cm in der Nähe der Primärentzündung), Stadium II, intraabdominaler, pelviner oder retroperitonealer Abzess oder Abzess entfernt von der Primärentzündung, Stadium III, generalisierte eitrige Peritonitis und Stadium IV, fäkale Peritonitis. Siehe Abb. 3.

Algorithmus für das Management der akuten Kolondivertikulitis.
Behandlung unkomplizierter ACD (Hinchey-Stadium 0 oder Ia)
Die meisten unkomplizierten ACD können sicher konservativ behandelt werden, wobei die Erfolgsquote zwischen 70 % und 100 % liegt.14 Die ambulante Behandlung kann den Gesundheitssystemen erhebliche Kosteneinsparungen ermöglichen. Bei unkomplizierter ACD sind die Kriterien für eine stationäre Behandlung signifikante Entzündungen (einschließlich Fieber oder Peritonitis), Unverträglichkeit von oraler Flüssigkeit, Alter über 80-85 Jahre, Immunsuppression oder schwere Begleiterkrankungen. In den meisten Fällen ist ein kurzer Krankenhausaufenthalt ausreichend. Es gibt keine Belege dafür, dass diätetische Einschränkungen die Behandlungsergebnisse beeinflussen, obwohl die meisten Ärzte in der Regel eine klare Flüssigkeitsdiät empfehlen.
Eine der größten Veränderungen der letzten Zeit bei der Behandlung der unkomplizierten ACD ist der abnehmende Einsatz von Antibiotika. Ein kürzlich durchgeführter Cochrane-Review, bei dem es sich lediglich um einen qualitativen Ansatz (ohne Metaanalyse) handelte, kam zu dem Ergebnis, dass die besten verfügbaren Daten den routinemäßigen Einsatz von Antibiotika nicht unterstützen.68 Antibiotika beschleunigen weder die Genesung noch verhindern sie Komplikationen oder ein Wiederauftreten. Daher ist der Einsatz von Antibiotika in diesem Fall fraglich. Wahrscheinlich wären sie bei Patienten mit Anzeichen einer generalisierten Infektion, Anzeichen einer Septikämie oder Bakteriämie und bei immungeschwächten Patienten angebracht. Die empfohlenen Therapien beruhen auf einem klinischen Konsens. Es können verschiedene Antibiotika verwendet werden, von Ampicilin bis zu Cephalosporinen der dritten Generation, solange sie gegen grampositive, gramnegative und anaerobe Bakterien wirksam sind. Die Kombination aus Ciprofloxacin und Metronidazol ist wahrscheinlich die am häufigsten verschriebene orale Behandlung. Wenn diese Kombination schlecht vertragen wird, kann Ampicilin-Sulfabactam eine gute Wahl sein. Andererseits haben neuere Daten gezeigt, dass eine intravenöse Behandlung keine Vorteile gegenüber einer oralen Antibiotikabehandlung und eine intravenöse 4-Tage-Behandlung keine Vorteile gegenüber einer 7-Tage-Behandlung bietet.69-71 In der Regel wird eine klinische Verbesserung innerhalb von 3-4 Tagen nach der Behandlung beobachtet. Schließlich wird eine stationäre Aufnahme mit intravenösem Antibiotikum empfohlen, wenn der Patient nicht in der Lage ist, oral Nahrung aufzunehmen, wenn er unter schweren Begleiterkrankungen leidet oder wenn die ambulante Behandlung keine Besserung bringt.
Behandlung von komplizierter ACD (Hinchey-Stadium Ib bis IV)ACD Hinchey Ib oder II: Abszess
Ungefähr 15 % der Patienten mit ACD entwickeln einen Abszess.67 Es gibt keine qualitativ hochwertigen Erkenntnisse über die optimale Behandlung von ACD mit Abszessbildung. Ein Krankenhausaufenthalt ist angezeigt. Die Größe ist ein wichtiger Faktor für den Behandlungserfolg. Bei kleineren Abszessen (
cm) wird eine konservative Behandlung mit Breitspektrum-Antibiotika empfohlen. Sie ist in bis zu 70 % erfolgreich.72 Wenn die konservative Behandlung versagt oder bei größeren Abszessen sollte eine perkutane Drainage durchgeführt werden. Sie ist in bis zu 80 % der Fälle erfolgreich.73 Eine Operation ist die Rettung, wenn die vorgenannten Behandlungen versagen.ACD Hinchey III oder IV: eitrige oder fäkale Peritonitis
Peritonitis ist die schwerwiegendste Komplikation mit einer Sterblichkeit von 14 %. Obwohl es keine Beweise gibt, gilt die frühzeitige Operation als Standardtherapie für diese Patienten. Die Wahl der Operation wird durch den Zustand des Patienten, den Operationsbefund und die Erfahrung des Chirurgen beeinflusst. Bei kritisch kranken Patienten mit hämodynamischer Instabilität wird das Verfahren nach Hartmann empfohlen. Bei hämodynamisch stabilen Patienten ist jedoch die primäre Anastomose mit oder ohne proximale Fäkalienableitung vorzuziehen.14,74
Traditionell wird in internationalen Leitlinien empfohlen, nach einer ACD-Episode eine Endoskopie durchzuführen, um ein kolorektales Karzinom auszuschließen. Diese Empfehlung stützt sich ausschließlich auf Expertenmeinungen. Neuere retrospektive Studien und eine systematische Übersichtsarbeit75-80 zeigen, dass die Krebsrate bei diesen Patienten eher gering ist. Auf der Grundlage dieser jüngsten Erkenntnisse könnte die wirksamste Strategie darin bestehen, nur Patienten mit anhaltenden Symptomen oder verdächtigen CT-Befunden zur Koloskopie zu überweisen. Für eine eindeutige Empfehlung sind jedoch weitere Studien erforderlich.
Behandlung nach einer ACD-Episode
Nach einer ACD-Episode erleidet etwa ein Drittel der Patienten eine zweite ACD, und nach einer zweiten Episode erleidet ein weiteres Drittel einen weiteren Anfall.73,74 Es gibt jedoch nur wenige Belege für die optimale Behandlung nach einer ACD-Episode, um eine neue Episode zu verhindern.
A) Ballaststoffreiche Ernährung
Nach Abklingen der akuten Episode wird allgemein eine ballaststoffreiche Ernährung empfohlen, um Rückfälle zu verringern. RCTs zu ballaststoffreichen Diäten bei Patienten mit ACD haben jedoch widersprüchliche Ergebnisse erbracht. In einer kürzlich veröffentlichten systematischen Übersicht über ballaststoffreiche Ernährung konnte keine Studie gefunden werden, die die Rolle von Ballaststoffen bei der Vorbeugung von rezidivierender ACD untersuchte.26,81 Einige Lebensmittel (Samen, Popcorn und Nüsse) werden klassischerweise vermieden, weil sie theoretisch in Divertikel eindringen, diese blockieren oder reizen können. Strate et al. fanden in ihrer großen, prospektiven Studie jedoch keinen Zusammenhang mit einem erhöhten Risiko für ACD. Daher sollte der Verzicht auf diese Lebensmittel nicht empfohlen werden.82 Auch eine Gewichtsreduktion und die Aufgabe des Rauchens können sich günstig auf die Prävention von ACD auswirken.9,83
B) Antibiotika
Es gibt drei neuere systematische Übersichten, in denen die Rolle von zyklischem Rifaximin bei der Verhinderung des Wiederauftretens von ACD bewertet wurde, die jedoch keinen eindeutigen Nutzen zeigten.46,84,85 Aus pathophysiologischer Sicht könnte eine plausible Erklärung für die Unwirksamkeit von Rifaximin bei der Vorbeugung von Rezidiven darin liegen, dass eine zyklische Behandlung die Bakterienpopulation im Dickdarm möglicherweise nicht während des gesamten Monats kontrolliert, da sich die Bakterienpopulation im Dickdarm innerhalb von 7-14 Tagen nach Beendigung der Rifaximin-Behandlung erholt. Eine kürzlich durchgeführte offene spanische RCT hat jedoch gezeigt, dass eine zyklische Rifaximin-Behandlung die Symptome verbessern und Remissionsphasen nach einer ACD aufrechterhalten kann.86 Rezidive traten bei 10,4 % der Patienten auf, die Rifaximin plus Ballaststoffe erhielten, im Vergleich zu 19,3 % der Patienten mit Ballaststoffen allein. Außerdem hatten Patienten, bei denen die Erstdiagnose vor ≥1 Jahr gestellt wurde, ein höheres Risiko einer Exazerbation (OR 3,34, 95% CI: 0,01-12,18). Es sind jedoch weitere Studien erforderlich, da zum jetzigen Zeitpunkt keine Empfehlungen ausgesprochen werden können. Es gibt keine Anhaltspunkte für die Verwendung anderer Antibiotika in dieser Situation.
C) Probiotika
Einige Open-Label-Studien haben die Rolle von Probiotika bei der Verhinderung des Wiederauftretens von ACD untersucht. Giaccari et al. untersuchten vor mehr als 20 Jahren die Rolle von Lactobacillus sp. nach einer Rifaximin-Behandlung bei 79 Patienten mit Kolonstenose nach Divertikulitis. 88 % der Patienten blieben über einen Zeitraum von 12 Monaten asymptomatisch.87 Diese Beobachtungsstudie war die erste, die eine mögliche Rolle von Probiotika in dieser Situation nahelegte. In einer neueren Studie wurde eine kombinierte Behandlung mit Balsalazid und VSL#3 (einer probiotischen Mischung aus acht Arten) untersucht. Nach 12 Monaten waren 73 % der Probanden unter der Kombinationstherapie asymptomatisch, verglichen mit 53 % unter der probiotischen Monotherapie (p>0,05).52 Zusammenfassend lässt sich sagen, dass Probiotika bei der Vorbeugung des Wiederauftretens von ACD wirksam zu sein scheinen, dass aber gut konzipierte Studien fehlen.
D) 5-ASA
Mehrere doppelblinde und offene RCTs haben die Rolle von Mesalazin bei der Vorbeugung des Wiederauftretens von ACD untersucht. Leider haben die meisten dieser Studien keinen Vorteil von Mesalazin gegenüber Placebo bei der Vorbeugung des Wiederauftretens von ACD festgestellt.88-90 Raskin et al. haben kürzlich zwei interessante und identische doppelblinde Phase-3-RCTs (PREVENT1 und PREVENT2) veröffentlicht, die ebenfalls zeigen, dass Mesalazin Placebo bei der Vorbeugung des Wiederauftretens von ACD nicht überlegen ist.91 Auch die kombinierte Behandlung, 5-ASA plus Rifaximin, wurde in mehreren Studien untersucht. Trivedi und Das werteten die Daten von fünf RCT und einer offenen Studie aus, an denen insgesamt mehr als 600 Patienten teilnahmen, und kamen zu dem Schluss, dass die Kombination bei der Vorbeugung von rezidivierender ACD Rifaximin allein überlegen zu sein scheint.92
E) Chirurgie
Bis vor einigen Jahren wurde nach zwei Anfällen von unkomplizierter ACD oder einem Anfall von komplizierter ACD eine elektive Operation empfohlen, um die Morbidität und Mortalität durch ein Rezidiv zu verringern. Eine elektive Operation birgt jedoch auch ein erhöhtes Morbiditäts- und Mortalitätsrisiko.93 Daher ist es wichtig, die Morbidität und Mortalität durch die Operation gegen das Risiko komplizierter Rezidive und die Schwere der Symptome abzuwägen.
Neue Daten zeigen, dass der natürliche Verlauf der ACD viel gutartiger ist als früher angenommen.73,94 Das langfristige Risiko eines Rückfalls ist geringer als bisher angenommen, und die langfristigen Risiken einer anschließenden Notoperation (3-7 %) und eines Todesfalls (95) zeigten, dass 16 % der Fälle mit einer ersten ACD dringend operiert wurden, verglichen mit nur 6 % bei rezidivierenden Fällen, und dass die 30-Tage-Mortalität bei der ersten Episode ebenfalls höher war als bei rezidivierenden Ereignissen (3 % gegenüber 0 %). Tatsächlich haben die meisten Patienten, die sich mit einer komplizierten ACD vorstellen, keine Krankheitsgeschichte.96 Es wird auch angenommen, dass eine rezidivierende ACD vor einer Perforation schützen kann, möglicherweise aufgrund einer entzündungsbedingten Adhäsionsbildung.95 Daher verringert eine elektive Operation nach einer ACD nicht die Wahrscheinlichkeit einer weiteren Operation (bis zu 3 %) und schützt nicht vollständig vor einem Rezidiv. Andererseits haben verbesserte Diagnose- und Behandlungsmethoden die Sterblichkeit bei komplizierter ACD verringert. Aufgrund dieser neuen Daten empfiehlt die American Society of Colon and Rectum Surgeons (Amerikanische Gesellschaft der Dickdarm- und Mastdarmchirurgen) in ihrer jüngsten Leitlinie, dass eine elektive Sigmaresektion nach der Genesung von ACD von Fall zu Fall entschieden werden sollte14 , und vertritt die Auffassung, dass die Anzahl früherer Episoden kein guter Indikator für die Auswahl von Kandidaten für eine elektive Operation ist. Ärzte sollten den Gesundheitszustand und das Alter des Patienten, die Häufigkeit und den Schweregrad der Anfälle und das Vorhandensein anhaltender Symptome nach der akuten Episode berücksichtigen.14
Es ist sehr schwierig, vorherzusagen, welche Fälle von ACD einen Rückfall erleiden werden. Der CT-Schweregrad der ersten ACD-Episode scheint ein Prädiktor für einen ungünstigen natürlichen Verlauf zu sein. Linkseitige ACD, >5 cm des Dickdarms und ein retroperitonealer Abszess waren Prädiktoren für ein Rezidiv und müssen berücksichtigt werden.97 Es besteht kein Konsens darüber, ob junges Alter (82 Nach den derzeitigen Erkenntnissen sollte das Alter nicht als Indikation für eine elektive Operation gelten, da es nicht mit einem schweren Krankheitsverlauf nach einer medikamentös behandelten ACD zusammenzuhängen scheint. In Anbetracht der Tatsache, dass ACD bei jüngeren Patienten häufiger auftritt, sind jedoch weitere Studien erforderlich, um diese spezifische Frage zu klären.
Ein Sonderfall sind immungeschwächte Personen. Kohortenstudien deuten darauf hin, dass diese Patienten ein hohes Risiko für komplizierte rezidivierende ACD (ein 5-fach höheres Perforationsrisiko) und ein hohes Risiko für Notoperationen haben.98 Daher könnte eine niedrigere Schwelle für elektive Operationen für sie von Vorteil sein.14 Biondo et al. zeigen jedoch in ihrer jüngsten Studie, dass immungeschwächte Patienten eine signifikant höhere Sterblichkeitsrate haben, allerdings nur bei der ersten Episode. Die Kontroverse bleibt also bestehen.99
Behandlung von FolgeerkrankungenA) Fistel
Eine Fistel entsteht, wenn ein Divertikelphlegma oder ein Abszess in ein benachbartes Organ reißt. Eine Fistel tritt bei weniger als 5 % der Patienten mit ACD auf. Die häufigsten sind kolovesikale und kolovaginale Fisteln. Vermutlich kann bei den meisten Patienten eine einzeitige operative Resektion mit Fistelverschluss und primärer Anastomose durchgeführt werden. Andere Fisteln wie koloenterische oder koluterine Fisteln sind selten.100,101
B) Obstruktion
Rezidivierende Episoden von ACD, die subklinisch sein können, können zu einer chronischen Verengung des Dickdarms führen, ohne dass eine Entzündung vorliegt. Es kann eine hochgradige oder vollständige Obstruktion auftreten. Vor der Behandlung der Obstruktion muss eine maligne Ätiologie ausgeschlossen werden. Wenn ein Neoplasma hinreichend ausgeschlossen ist und keine ACD vorliegt, können eine endoskopische Dilatation oder eine vorübergehende Dekompression mit einem Metallstent therapeutische Optionen sein.102 Später kann eine anschließende einzeitige Resektion ohne Divertikulose durchgeführt werden.
Behandlung der segmentalen Kolitis im Zusammenhang mit Divertikulose
Sie ist definiert als eine chronische Entzündung der interdivertikulären Schleimhaut eines betroffenen Kolonsegments. Das Rektum und der rechte Dickdarm bleiben verschont. Sie hat sich zu einer ausgeprägten klinischen und pathologischen Störung entwickelt und geht häufig mit blutigem Stuhl einher. Die Pathogenese ist unbekannt. Das Spektrum der histologischen Veränderungen reicht von leichten unspezifischen Entzündungen bis hin zu entzündlichen Darmerkrankungen ähnlichen Veränderungen. Aus diesem Grund ist die Differentialdiagnose oft schwierig. Die meisten Patienten erholen sich innerhalb weniger Wochen oder Monate vollständig. Einige von ihnen werden anfangs mit oralem 5-ASA behandelt, aber wahrscheinlich sind diese Medikamente nicht notwendig, da die meisten Fälle spontan abklingen.103
Schlussfolgerungen
Bei symptomatischer UDD zielt die Behandlung darauf ab, Komplikationen zu verhindern und die Symptome zu verringern. Nach den derzeitigen Erkenntnissen scheinen Ballaststoffe plus zyklisches Rifaximin oder Mesalazin plus Probiotika die wirksamsten Therapien zu sein. Bei der ACD scheinen Antibiotika nach wie vor die Hauptstütze der Behandlung zu sein, und eine ambulante Behandlung wird bei der überwiegenden Mehrheit der Patienten mit unkomplizierter ACD als optimaler Ansatz angesehen. Bei komplizierter ACD sind jedoch eine stationäre Behandlung und intravenöse Antibiotika erforderlich. Derzeit ändert sich die Rolle der Notfallchirurgie. Die meisten Divertikulitis-assoziierten Abszesse können mit intravenösen Antibiotika und/oder perkutaner Drainage behandelt werden, und eine Notoperation wird nur noch bei Patienten mit Peritonitis als Standardbehandlung angesehen. Schließlich sollte eine elektive Operation nach der Genesung von ACD von Fall zu Fall entschieden werden.
Beiträge der Autoren
Gargallo CJ, Sopeña F und Lanas A trugen gleichermaßen zum Design, zur redaktionellen Ausarbeitung und zur Überprüfung dieser Arbeit bei.
Interessenkonflikt
Dr. Carla J. Gargallo und Dr. Federico Sopeña melden keinen Interessenkonflikt. Dr. Angel Lanas war Berater von AlfaWasserman.
