Ein gramnegativer Bazillus aus der Familie der Enterobacteriaceae, Serratia marcescens ist ein Organismus, der Bakteriämie, Lungenentzündung, Harnwegsinfektionen, Endokarditis, Meningitis und septische Arthritis verursachen kann.1 Es wurde auch über ungewöhnliche Fälle von Zellulitis und nekrotisierender Fasziitis (NF) berichtet, die durch S. marcescens verursacht wurden.2,3 Diese Entität wurde zunächst bei immungeschwächten und nicht immungeschwächten Patienten beschrieben.4 Es wurden auch Fälle sowohl in der Gemeinschaft als auch nosokomial berichtet.3
Fallbericht
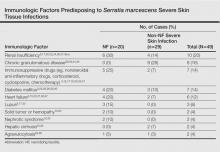
Eine 68-jährige krankhaft fettleibige Frau mit Bluthochdruck, Diabetes mellitus, chronischer Niereninsuffizienz, chronischer Veneninsuffizienz und Lymphödem am linken Bein wurde in unsere Notaufnahme eingewiesen. Sie hatte Schmerzen und ein zirkuläres Erythem mit multiplen Abszessen am linken Bein, die seit 2 Wochen bestanden. Es gab keine Anamnese eines Traumas, eines Geschwürs, einer Injektion oder eines Tierbisses. Zum Zeitpunkt der Vorstellung hatte sie kein Fieber und die Vitalparameter waren normal. Es wurde eine empirische Behandlung mit oralem Amoxicillin (6 g täglich) und Amoxicillin-Clavulanat (375 mg täglich) begonnen. Achtundvierzig Stunden später verschlimmerten sich Entzündung, Schmerzen und Abszesse (Abbildung 1A). Die Laboruntersuchungen ergaben eine erhöhte Anzahl weißer Blutkörperchen (15,9×109⁄L mit 86 % Neutrophilen) und einen erhöhten Spiegel an C-reaktivem Protein (322 mg/L). Die Serologie des humanen Immundefizienzvirus war negativ. Bei der Nadelaspiration eines Abszesses wurde S. marcescens nachgewiesen. Eine zweite Aspiration bestätigte das Vorhandensein desselben Organismus, eines Wildtyps von S. marcescens, der resistent gegen Amoxicillin und Clavulansäure, Cephalosporine der ersten Generation und Tobramycin, aber empfindlich gegen Piperacillin, Cephalosporine der dritten Generation, Amikacin, Ciprofloxacin und Co-Trimoxazol war. Cefepim, ein Cephalosporin der dritten Generation, wurde intravenös verabreicht. Innerhalb der nächsten 48 Stunden entwickelte der Patient eine schwere Sepsis mit Verwirrung, akutem Nierenversagen (Kreatinin: 231 µmol/L vs. 138 µmol/L bei Studienbeginn 9,11,35-38,40; Abszesse, Gumma oder Pyoderma gangrenosum-ähnliche Läsionen im Zusammenhang mit chronischen granulomatösen Erkrankungen im Kindesalter 29,44,45; schmerzhafte Knötchen mit sekundären Abszessen 31-34,46; akute bullöse Cellulitis 8,10,30; Sekundärinfektionen von Geschwüren 35,40; Abszesse bei immunkompetenten Patienten 41; und nekrotisierende Hautulzerationen 36). Häufig waren die unteren Extremitäten betroffen (NF-Fälle, n=13; Nicht-NF-Fälle, n=16). Eine zugrunde liegende Immunsuppression wurde in 14 NF-Fällen und in 17 Nicht-NF-Fällen beobachtet. Die prädisponierenden immunologischen Faktoren sind in der Tabelle zusammengefasst. Lokale Risikofaktoren, einschließlich chronischer Beinödeme, Traumata, chirurgischer Wunden, Füllstoffinjektionen und Ulcera, wurden bei NF- und Nicht-NF-Fällen häufig berichtet (16, 20, 26-28, 31, 32, 34, 35, 37, 38, 40, 46), auch in unserem Fall. In 19 NF-Fällen und in 7 Nicht-NF-Fällen war eine Operation erforderlich. Serratia marcescens-vermittelte NF führte zu einer höheren Sterblichkeit (n=12) als Nicht-NF-Fälle (n=1). Zu den anderen, nicht schwerwiegenden klinischen Manifestationen einer S. marcescens-Infektion, über die in der Literatur berichtet wurde, gehörten disseminierte papulöse Eruptionen mit Infektion durch das humane Immundefizienz-Virus42 und Follikulitis des Rumpfes.43 Unser Patient hatte viele Risikofaktoren, darunter chronische Ödeme, Diabetes mellitus, chronische Niereninsuffizienz und chronische Veneninsuffizienz. Das mögliche Vorhandensein von Abszessen und nekrotischem Gewebe behindert die antibiotische Penetration an der Infektionsstelle, und angesichts der hohen Sterblichkeitsrate der S. marcescens-Zellulitis sollte eine Operation systematisch und so früh wie möglich in Betracht gezogen werden.