Oppimistavoitteet
- Kuvaa lihassupistukseen osallistuvat komponentit
- Erittele, miten lihasten supistuvat ja rentoutuvat
- Kuvaa lihassupistuksen liukulankamalli
Tapahtumasarja, joka johtaa yksittäisen lihassäikeen supistumiseen, alkaa signaalista – hermovälittäjäaineesta, ACh:lla, joka tulee kyseistä kuitua hermottavasta motoneuronista. Kuidun paikallinen kalvo depolarisoituu, kun positiivisesti varautuneet natriumionit (Na+) pääsevät sisään, mikä laukaisee toimintapotentiaalin, joka leviää muuhun kalvoon depolarisoituu, mukaan lukien T-tubulukset. Tämä käynnistää kalsiumionien (Ca++) vapautumisen sarkoplasmisen retikulumin (SR) varastoista. Ca++ käynnistää sitten supistumisen, jota ATP ylläpitää (kuva 1). Niin kauan kuin Ca++ -ionit pysyvät sarkoplasmassa sitoutumassa troponiiniin, joka pitää aktiinin sitoutumiskohdat ”suojaamattomina”, ja niin kauan kuin ATP:tä on saatavilla ristisiltojen pyörimiseen ja myosiinin suorittamaan aktiinisäikeiden vetämiseen, lihassäie jatkaa lyhenemistä anatomiselle rajalle.

Kuva 1. Lihassyiden supistuminen. Aktiinin ja myosiinipäiden välille muodostuu ristisilta, joka käynnistää supistumisen. Niin kauan kuin Ca++ -ioneja jää sarkoplasmaan sitoutumaan troponiiniin ja niin kauan kuin ATP:tä on saatavilla, lihassyiden lyheneminen jatkuu.
Lihaksen supistuminen pysähtyy yleensä, kun motoneuronista tuleva signalointi loppuu, mikä repolarisoi sarkolemman ja T-tubulukset ja sulkee SR:ssä olevat jänniteohjatut kalsiumkanavat. Ca++ -ionit pumpataan sitten takaisin SR:ään, mikä saa tropomyosiinin suojaamaan (tai peittämään uudelleen) aktiinisäikeiden sitoutumiskohdat. Lihas voi myös lopettaa supistumisen, kun ATP loppuu ja se väsyy (kuva 2).

Kuva 2. Lihassyiden rentoutuminen. Ca++ -ionit pumpataan takaisin SR:ään, mikä saa tropomyosiinin suojaamaan uudelleen aktiinisäikeiden sitoutumiskohdat. Lihas voi myös lopettaa supistumisen, kun ATP loppuu ja se väsyy.
Lihassyiden lyhenemisen molekyylitapahtumat tapahtuvat kuidun sarkomeereissä (ks. kuva 3). Raidallisen lihassyyn supistuminen tapahtuu, kun sarkomeerit, jotka ovat lineaarisesti järjestäytyneet myofibrillien sisään, lyhenevät myosiinipäiden vetäessä aktiinifilamentteja.
Alue, jossa paksut ja ohuet filamentit menevät päällekkäin, näyttää tiheältä, koska filamenttien välissä on vähän tilaa. Tämä alue, jossa ohuet ja paksut filamentit menevät päällekkäin, on erittäin tärkeä lihaksen supistumisen kannalta, sillä se on kohta, jossa filamenttien liike alkaa. Ohuet filamentit, jotka ovat ankkuroituneet päistään Z-levyihin, eivät ulotu kokonaan keskialueelle, jossa on vain paksuja filamentteja, jotka ovat ankkuroituneet tyvestään kohtaan, jota kutsutaan M-linjaksi. Myofibrilli koostuu monista sarkomeereista, jotka kulkevat sen pituussuunnassa; näin ollen myofibrillit ja lihassolut supistuvat, kun sarkomeerit supistuvat.
Liukuvan filamentin supistumismalli
Motoneuronin antaman signaalin myötä luurankolihaskuitu supistuu, kun ohuet filamentit vetäytyvät ja liukuvat sen jälkeen paksujen filamenttien ohi kuitujen sarkomeerien sisällä. Tätä prosessia kutsutaan lihassupistuksen liukuvan filamentin malliksi (kuva 3). Liukuminen voi tapahtua vain, kun aktiinifilamenttien myosiiniin sitoutumiskohdat paljastuvat useiden vaiheiden kautta, jotka alkavat Ca++:n pääsystä sarkoplasmaan.

Kuva 3. Liukuvien filamenttien malli lihassupistuksesta. Kun sarkomeeri supistuu, Z-viivat siirtyvät lähemmäs toisiaan ja I-kaista pienenee. A-kaista pysyy saman levyisenä. Täydellisessä supistumisessa ohut ja paksu filamentti menevät päällekkäin.
Tropomyosiini on proteiini, joka kiertyy aktiinifilamentin ketjujen ympärille ja peittää myosiinin sitoutumiskohdat estääkseen aktiinin sitoutumisen myosiiniin. Tropomyosiini sitoutuu troponiiniin muodostaen troponiini-tropomyosiinikompleksin. Troponiini-tropomyosiinikompleksi estää myosiinin ”päitä” sitoutumasta aktiinimikrofilamenttien aktiivisiin kohtiin. Troponiinilla on myös Ca++ -ionien sitoutumiskohta.
Lihaksen supistumisen käynnistämiseksi tropomyosiinin on paljastettava myosiinin sitoutumiskohta aktiinifilamentissa, jotta aktiini- ja myosiinimikrofilamenttien välille muodostuu ristisilta. Supistumisprosessin ensimmäinen vaihe on, että Ca++ sitoutuu troponiiniin, jotta tropomyosiini voi liukua pois aktiinisäikeiden sitoutumiskohdista. Näin myosiinipäät voivat sitoutua näihin paljastuneisiin sitoutumiskohtiin ja muodostaa ristisiltoja. Myosiinipäät vetävät sitten ohuita filamentteja ohi paksujen filamenttien kohti sarkomeerin keskustaa. Kukin pää voi kuitenkin vetää vain hyvin lyhyen matkan, ennen kuin se on saavuttanut rajansa ja se on ”kiinnitettävä uudelleen”, ennen kuin se voi vetää uudelleen, mikä edellyttää ATP:tä.
ATP ja lihassupistus
Jotta ohuet filamentit voisivat jatkaa liukumista paksujen filamenttien ohi lihassupistuksen aikana, myosiinipäiden on vedettävä aktiinia sitoutumiskohdissa, irrotettava, kiinnitettävä uudelleen, kiinnitettävä lisää sitoutumiskohtia, vedettävä, irrotettava, kiinnitettävä uudelleen jne. Tätä toistuvaa liikettä kutsutaan ristisiltasykliksi. Tämä myosiinipäiden liike muistuttaa airoja, kun ihminen soutaa venettä: Airojen mela (myosiinipäät) vetää, nostetaan vedestä (irtoaa), asetetaan uudelleen paikalleen (kiinnittyy uudelleen) ja upotetaan sitten uudelleen vetämään (kuva 4). Jokainen sykli vaatii energiaa, ja sarkomeereissä olevien myosiinipäiden toiminta, jossa ne vetävät toistuvasti ohuita filamentteja, vaatii myös energiaa, jota saadaan ATP:stä.
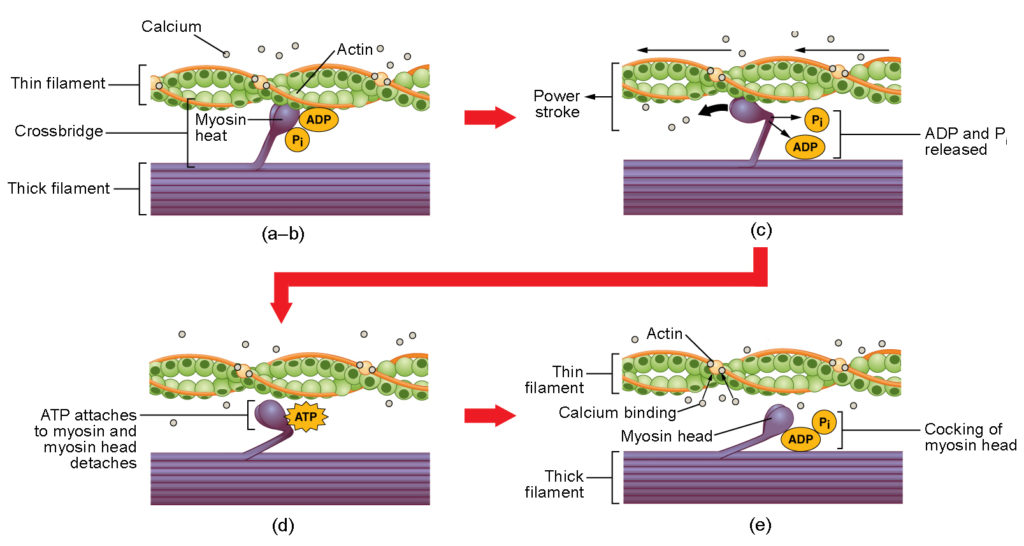
Kuva 4. Luustolihaksen supistuminen. (a) Aktiinin aktiivinen kohta paljastuu kalsiumin sitoutuessa troponiiniin. (b) Myosiinipää vetää puoleensa aktiinia, ja myosiini sitoutuu aktiiniin sen aktiinin sitoutumiskohtaan muodostaen ristisillan. (c) Voimanoton aikana edellisessä supistumissyklissä syntynyt fosfaatti vapautuu. Tämän seurauksena myosiinin pää kääntyy kohti sarkomeerin keskustaa, minkä jälkeen kiinnittynyt ADP ja fosfaattiryhmä vapautuvat. (d) Uusi ATP-molekyyli kiinnittyy myosiinipäähän, jolloin ristisilta irtoaa. (e) Myosiinipää hydrolysoi ATP:n ADP:ksi ja fosfaatiksi, jolloin myosiini palaa kallistuneeseen asentoon.
Ristisillan muodostuminen tapahtuu, kun myosiinipää kiinnittyy aktiiniin, kun adenosiinidifosfaatti (ADP) ja epäorgaaninen fosfaatti (Pi) ovat vielä sitoutuneina myosiiniin (kuva 4a,b). Tämän jälkeen Pi vapautuu, jolloin myosiini kiinnittyy vahvemmin aktiiniin, minkä jälkeen myosiinin pää liikkuu kohti M-linjaa vetäen aktiinin mukanaan. Kun aktiinia vedetään, filamentit liikkuvat noin 10 nm kohti M-linjaa. Tätä liikettä kutsutaan voima-iskuksi, koska ohuen filamentin liike tapahtuu tässä vaiheessa (kuva 4c). ATP:n puuttuessa myosiinin pää ei irtoa aktiinista.
Myosiinin pään yksi osa kiinnittyy aktiinissa olevaan sitoutumiskohtaan, mutta päässä on toinen ATP:n sitoutumiskohta. ATP:n sitoutuminen saa myosiinipään irtoamaan aktiinista (kuva 4d). Tämän jälkeen ATP muuttuu ADP:ksi ja Pi:ksi myosiinin luontaisen ATPaasiaktiivisuuden avulla. ATP-hydrolyysin aikana vapautuva energia muuttaa myosiinipään kulmaa kallistuneeseen asentoon (kuva 4e). Myosiinin pää on nyt asennossa jatkoliikettä varten.
Kun myosiinin pää on kallistuneena, myosiini on korkean energian konfiguraatiossa. Tämä energia kuluu myosiinipään liikkuessa voimahyökkäyksen aikana, ja voimahyökkäyksen lopussa myosiinipää on matalaenergisessä asennossa. Voimahyökkäyksen jälkeen ADP vapautuu; muodostunut ristisilta on kuitenkin edelleen paikallaan, ja aktiini ja myosiini ovat sitoutuneet toisiinsa. Niin kauan kuin ATP:tä on saatavilla, se kiinnittyy helposti myosiiniin, ristisiltasykli voi toistua ja lihassupistus voi jatkua.
Huomaa, että jokaisessa noin 300 myosiinimolekyylistä koostuvassa paksussa filamentissa on useita myosiinipäitä, ja monet ristisillat muodostuvat ja katkeavat jatkuvasti lihassupistuksen aikana. Kerro tämä yhden myofibrillin kaikilla sarkomeereillä, yhden lihassyiden kaikilla myofibrilleillä ja yhden luurankolihaksen kaikilla lihassyillä, ja voit ymmärtää, miksi luurankolihasten toiminnan ylläpitämiseen tarvitaan niin paljon energiaa (ATP:tä). Itse asiassa juuri ATP:n menetys aiheuttaa kuolonkankeuden, joka havaitaan pian kuoleman jälkeen. Koska ATP:n tuotanto ei ole enää mahdollista, myosiinipäiden ei ole mahdollista irrottaa ATP:tä aktiinin sitoutumiskohdista, joten ristisillat pysyvät paikoillaan aiheuttaen luurankolihasten jäykkyyden.
ATP:n lähteet
ATP:n avulla saadaan energiaa lihaksen supistumisen tapahtumiseen. Sen lisäksi, että ATP:llä on suora rooli ristisiltasyklissä, se tuottaa energiaa myös SR:n aktiivisen kuljetuksen Ca++-pumpuille. Lihassupistusta ei tapahdu ilman riittävää määrää ATP:tä. Lihakseen varastoituneen ATP:n määrä on hyvin vähäinen, ja se riittää vain muutaman sekunnin kestäviin supistuksiin. Koska ATP hajoaa, se on siksi regeneroitava ja korvattava nopeasti, jotta supistuminen voi jatkua. On olemassa kolme mekanismia, joilla ATP:tä voidaan regeneroida: kreatiinifosfaattiaineenvaihdunta, anaerobinen glykolyysi, käyminen ja aerobinen hengitys.
Kreatiinifosfaatti on molekyyli, joka voi varastoida energiaa fosfaattisidoksiinsa. Levossa olevassa lihaksessa ylimääräinen ATP siirtää energiansa kreatiiniin, jolloin syntyy ADP:tä ja kreatiinifosfaattia. Tämä toimii energiavarastona, jota voidaan käyttää nopeasti luomaan lisää ATP:tä. Kun lihas alkaa supistua ja tarvitsee energiaa, kreatiinifosfaatti siirtää fosfaattinsa takaisin ADP:hen muodostaen ATP:tä ja kreatiinia. Tätä reaktiota katalysoi entsyymi kreatiinikinaasi, ja se tapahtuu hyvin nopeasti, joten kreatiinifosfaatista peräisin oleva ATP antaa virtaa lihassupistuksen ensimmäisten sekuntien aikana. Kreatiinifosfaatti pystyy kuitenkin tuottamaan energiaa vain noin 15 sekunnin ajan, jolloin on käytettävä jotain muuta energianlähdettä (kuva 5).

Kuva 5. Lihaksen aineenvaihdunta. Lepovaiheessa olevaan lihakseen varastoituu jonkin verran ATP:tä. Kun supistuminen alkaa, se kuluu sekunneissa. Lisää ATP:tä tuotetaan kreatiinifosfaatista noin 15 sekunnin ajan.
Kun kreatiinifosfaatin tuottama ATP loppuu, lihakset kääntyvät glykolyysiin ATP:n lähteenä. Glykolyysi on anaerobinen (ei-hapesta riippuvainen) prosessi, joka hajottaa glukoosia (sokeria) ATP:n tuottamiseksi; glykolyysi ei kuitenkaan pysty tuottamaan ATP:tä yhtä nopeasti kuin kreatiinifosfaatti. Näin ollen siirtyminen glykolyysiin johtaa siihen, että ATP:n saatavuus lihakseen on hitaampaa. Glykolyysissä käytettävä sokeri voi olla peräisin verensokerista tai lihakseen varastoituneen glykogeenin aineenvaihdunnasta. Yhden glukoosimolekyylin hajoaminen tuottaa kaksi ATP:tä ja kaksi molekyyliä palorypälehappoa, jotka voidaan käyttää aerobisessa hengityksessä tai, kun happipitoisuus on alhainen, muuntaa maitohapoksi (kuva 6).

Kuva 6. Glykolyysi ja aerobinen hengitys. Glykolyysi ja aerobinen hengitys. Jokainen glukoosimolekyyli tuottaa kaksi ATP:tä ja kaksi molekyyliä palorypälehappoa, jotka voidaan käyttää aerobisessa hengityksessä tai muuntaa maitohapoksi. Jos happea ei ole saatavilla, palorypälehappo muuttuu maitohapoksi, mikä voi vaikuttaa lihasten väsymiseen. Näin tapahtuu rasittavassa liikunnassa, kun tarvitaan suuria määriä energiaa, mutta happea ei saada riittävästi lihakseen.
Jos happea on saatavilla, palorypälehappo käytetään aerobisessa hengityksessä. Jos happea ei kuitenkaan ole saatavilla, palorypälehappo muuttuu maitohapoksi, mikä voi osaltaan aiheuttaa lihasväsymystä. Tämä muuntaminen mahdollistaa NAD+ -entsyymin kierrättämisen NADH:sta, jota tarvitaan glykolyysin jatkumiseen. Näin tapahtuu rasittavassa liikunnassa, kun tarvitaan suuria määriä energiaa, mutta happea ei saada riittävästi lihakseen. Glykolyysiä itsessään ei voida ylläpitää kovin pitkään (noin 1 minuutti lihastoimintaa), mutta se on hyödyllinen lyhyen korkeaintensiteettisen suorituksen helpottamiseksi. Tämä johtuu siitä, että glykolyysi ei hyödynnä glukoosia kovin tehokkaasti, vaan tuottaa nettomääräisesti kaksi ATP:tä glukoosimolekyyliä kohti ja lopputuotteena maitohappoa, joka voi osaltaan vaikuttaa lihasten väsymiseen, kun sitä kertyy.
Aerobinen hengitys on glukoosin tai muiden ravintoaineiden hajoamista hapen (O2) läsnä ollessa hiilidioksidin, veden ja ATP:n tuottamiseksi. Noin 95 prosenttia lepotilassa olevien tai kohtalaisen aktiivisten lihasten tarvitsemasta ATP:stä saadaan aerobisesta hengityksestä, joka tapahtuu mitokondrioissa. Aerobisen hengityksen syötteitä ovat verenkierrossa kiertävä glukoosi, palorypälehappo ja rasvahapot. Aerobinen hengitys on paljon tehokkaampaa kuin anaerobinen glykolyysi, sillä se tuottaa noin 36 ATP:tä yhtä glukoosimolekyyliä kohti, kun glykolyysi tuottaa neljä ATP:tä. Aerobista hengitystä ei kuitenkaan voida ylläpitää ilman luurankolihaksen jatkuvaa O2-tarjontaa, ja se on paljon hitaampaa (kuva 7). Tämän kompensoimiseksi lihakset varastoivat pienen määrän ylimääräistä happea proteiineihin, joita kutsutaan myoglobiiniksi, mikä mahdollistaa tehokkaammat lihassupistukset ja vähentää väsymystä. Aerobinen harjoittelu lisää myös verenkiertojärjestelmän tehokkuutta, joten lihaksille voidaan toimittaa O2:ta pidempään.

Kuva 7. Soluhengitys. Aerobinen hengitys on glukoosin hajoaminen hapen (O2) läsnä ollessa hiilidioksidiksi, vedeksi ja ATP:ksi. Noin 95 prosenttia lepotilassa olevien tai kohtalaisen aktiivisten lihasten tarvitsemasta ATP:stä saadaan aerobisesta hengityksestä, joka tapahtuu mitokondrioissa.
Lihasväsymys syntyy, kun lihas ei enää pysty supistumaan vastauksena hermoston signaaleihin. Lihasväsymyksen tarkkoja syitä ei täysin tunneta, vaikka tietyt tekijät on yhdistetty väsymyksen aikana tapahtuvaan lihassupistuksen vähenemiseen. ATP:tä tarvitaan lihaksen normaaliin supistumiseen, ja kun ATP-varaukset vähenevät, lihaksen toiminta voi heikentyä. Tämä voi olla tärkeämpi tekijä lyhytaikaisissa, voimakkaissa lihasvoimisteluissa kuin pitkäkestoisissa, matalamman intensiteetin ponnisteluissa. Maitohapon kertyminen voi alentaa solunsisäistä pH:ta, mikä vaikuttaa entsyymien ja proteiinien toimintaan. Na+- ja K+-tasojen epätasapaino kalvon depolarisaation seurauksena voi häiritä Ca++ -virtausta SR:stä. Pitkään jatkuva rasitus voi vaurioittaa SR:ää ja sarkolemmaa, jolloin Ca++:n säätely heikkenee.
Intensiivinen lihastoiminta johtaa happivelkaan, joka on hapen määrä, joka tarvitaan kompensoimaan ilman happea tuotettua ATP:tä lihassupistuksen aikana. Happea tarvitaan ATP- ja kreatiinifosfaattitasojen palauttamiseen, maitohapon muuttamiseen palorypälehapoksi ja maksassa maitohapon muuttamiseen glukoosiksi tai glykogeeniksi. Myös muut liikunnan aikana käytettävät järjestelmät tarvitsevat happea, ja kaikki nämä yhdistetyt prosessit johtavat liikunnan jälkeen lisääntyneeseen hengitystaajuuteen. Kunnes happivelka on täytetty, hapen saanti on koholla myös sen jälkeen, kun liikunta on lopetettu.
Luurankolihaksen rentoutuminen
Luurankolihaksen lihassäikeiden ja viime kädessä luurankolihaksen rentoutuminen alkaa liikehermosolusta, joka lopettaa kemiallisen signaalinsa, ACh:n, vapauttamisen NMJ:n synapsiin. Lihassyyt repolarisoituvat, mikä sulkee portit SR:ssä, josta Ca++ vapautui. ATP-vetoiset pumput siirtävät Ca++:n sarkoplasmasta takaisin SR:ään. Tämä johtaa ohuiden filamenttien aktiinin sitoutumiskohtien ”uudelleen suojautumiseen”. Ilman kykyä muodostaa ristisiltoja ohuiden ja paksujen filamenttien välille lihaskuitu menettää jännityksensä ja rentoutuu.
Lihasvoima
Luuston lihassäikeiden määrä tietyssä lihaksessa on geneettisesti määräytynyt eikä se muutu. Lihasvoima on suoraan yhteydessä myofibrillien ja sarkomeerien määrään kussakin kuidussa. Lihakseen vaikuttavat tekijät, kuten hormonit ja stressi (ja keinotekoiset anaboliset steroidit), voivat lisätä sarkomeerien ja myofibrillien tuotantoa lihassyiden sisällä, muutosta kutsutaan hypertrofiaksi, joka johtaa luurankolihaksen lisääntyneeseen massaan ja bulkkiin. Vastaavasti luurankolihaksen käytön väheneminen johtaa surkastumiseen, jolloin sarkomeerien ja myofibrillien määrä häviää (mutta ei lihassyiden määrä). On tavallista, että kipsissä olevan raajan lihakset surkastuvat, kun kipsi poistetaan, ja tietyissä sairauksissa, kuten poliossa, lihakset surkastuvat.
Lihaksiston sairaudet
Duchennen lihasdystrofia (DMD) on luurankolihasten etenevä heikkeneminen. Se on yksi useista sairauksista, joista käytetään yhteisnimitystä ”lihasdystrofia”. DMD:n aiheuttaa dystrofiiniproteiinin puute, joka auttaa myofibrillien ohuita filamentteja sitoutumaan sarkolemmaan. Ilman riittävää dystrofiinia lihassupistukset aiheuttavat sarkolemman repeämisen, mikä aiheuttaa Ca++:n virtauksen, joka johtaa soluvaurioihin ja lihassyiden hajoamiseen. Ajan myötä lihasvaurioiden kasautuessa lihasmassa vähenee ja kehittyy suurempia toiminnallisia haittoja.
DMD on perinnöllinen sairaus, jonka aiheuttaa epänormaali X-kromosomi. Se vaikuttaa pääasiassa miehiin, ja se diagnosoidaan yleensä varhaislapsuudessa. DMD ilmenee yleensä ensin tasapaino- ja liikkumisvaikeuksina ja etenee sitten kävelykyvyttömyydeksi. Se etenee kehossa ylöspäin alaraajoista ylävartaloon, jossa se vaikuttaa hengityksestä ja verenkierrosta vastaaviin lihaksiin. Lopulta se aiheuttaa kuoleman hengitysvajauksen vuoksi, eivätkä sairastuneet yleensä elä yli 20-vuotiaiksi.
Koska DMD:n aiheuttaa mutaatio geenissä, joka koodaa dystrofiinia, ajateltiin, että terveiden myoblastien lisääminen potilaisiin voisi olla tehokas hoito. Myoblastit ovat alkion soluja, jotka vastaavat lihasten kehityksestä, ja ihanteellisessa tapauksessa ne kantaisivat terveitä geenejä, jotka voisivat tuottaa normaaliin lihassupistukseen tarvittavaa dystrofiinia. Tämä lähestymistapa on ollut suurelta osin epäonnistunut ihmisillä. Viimeaikaisessa lähestymistavassa on yritetty lisätä lihaksen tuotantoa utrofiinilla, joka on dystrofiinin kaltainen proteiini, joka saattaa pystyä ottamaan dystrofiinin roolin ja estämään soluvaurioiden syntymisen.
Itsetarkistuskysymykset
Toteuta alla oleva tietokilpailu tarkistaaksesi ymmärryksesi lihassäikeiden supistumisesta ja rentoutumisesta:
