Ionisilla, kovalenttisilla (yksinkertaiset molekyylit ja jättiläisatomit) ja metallisilla yhdisteillä on kaikilla erilaisia ominaisuuksia. Näin ollen aineen luokittelemiseksi jompaankumpaan näistä yhdisteistä on suoritettava sarja testejä/kokeita, jotta saadaan selville, mitä ominaisuuksia sillä on. Tarkkaile seuraavaa taulukkoa:
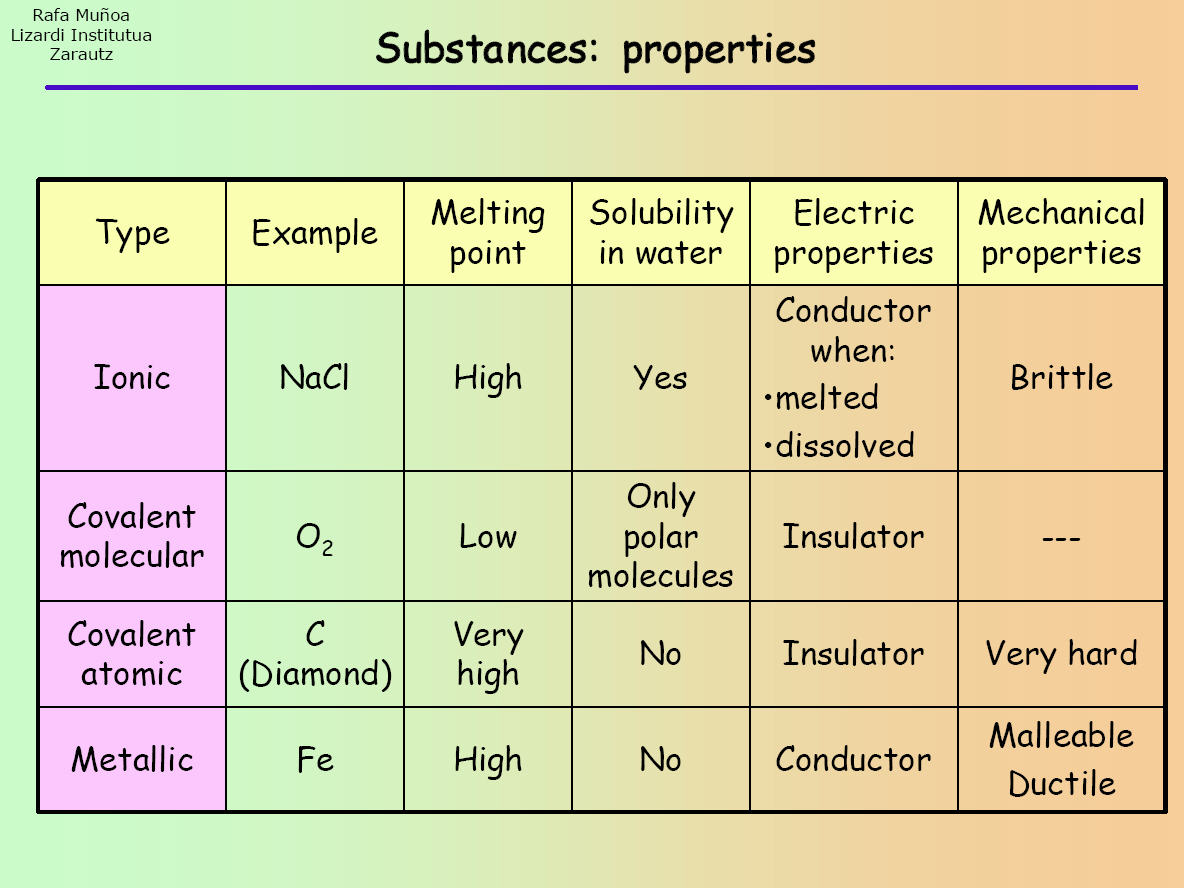
Kun koe on suoritettu, saatuja tuloksia voidaan verrata taulukossa oleviin tuloksiin, jotta voidaan selvittää, minkälainen yhdiste aine on.
Aluksi näyte tuntemattomasta aineesta voidaan laittaa koeputkeen ja laittaa liekin päälle. Näin tehdään sulamispisteen määrittämiseksi. Jos aine sulaa, se on todennäköisesti kovalenttinen yksinkertainen molekyyliaine (kuten taulukossa on esitetty). Jos sulamista ei kuitenkaan tapahdu, aine voi olla joko ioninen, kovalenttinen jättiläisatominen tai metallinen.
Tässä on oikeastaan se syy, miksi tuntemattomalle aineelle on tehtävä useampi kuin yksi koe, koska joillakin yhdisteryhmillä on samankaltaisia ominaisuuksia (esimerkiksi ionisilla yhdisteillä ja kovalenttisilla yhdisteillä on molemmilla korkeat sulamispisteet).
Seuraavaksi voit kokeilla liuottaa jonkin verran ainetta veteen (tai muuhun polaariseen liuottimeen). Jos se liukenee, se voi olla joko ioninen tai kovalenttinen yksinkertainen molekyyliyhdiste. Edellisestä ja seuraavasta kokeesta saamasi tulokset auttavat rajaamaan tulokset vain yhteen yhdystyyppiin.
Seuraavaksi voit liittää näytteen alla olevan kaltaiseen virtapiiriin nähdäksesi, johtaako se sähkövirtaa.
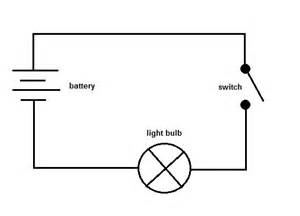
Voit korvata kytkimen näytteellä. Jos lamppu syttyy, se on johdin ja jos ei syty, se on ei-johdin.
Jos siis esimerkiksi tämän kokeen lopussa näyte pysyi sulamattomana, liukeni veteen ja johti sähkövirtaa, se on ioninen yhdiste.
Kaikki nämä havainnot voidaan selittää tarkemmin tutkimalla sidoksia ja molekyylien välisiä vetovoimia, jotka pitävät yhdisteen komponentit yhdessä.
