Esittely
Paksusuolen divertikkelitauti on yleisin paksusuolen sairaus länsimaissa. Divertikkelitaudin esiintyvyys on lisääntynyt viime vuosisadan aikana kaikkialla maailmassa, mikä johtuu todennäköisesti elämäntapojen muutoksista, kuten tupakoinnista, ylipainosta ja kaiken kaikkiaan fyysisestä passiivisuudesta ja vähäkuituisesta ruokavaliosta. Esiintyvyys kasvaa iän myötä, ja se vaihtelee noin 5 prosentista alle 40-vuotiailla aikuisilla 50-70 prosenttiin 80-vuotiailla tai sitä vanhemmilla; 80 prosenttia divertikuliittia sairastavista potilaista on 50-vuotiaita tai sitä vanhempia. Divertikkeleitä voi esiintyä yksittäin tai satoja, ja niiden halkaisija on tyypillisesti 5-10 mm, mutta ne voivat olla yli 2 cm:n kokoisia. Divertikuloosia esiintyy ensisijaisesti sigma- ja laskevassa paksusuolessa yli 90 %:lla potilaista, mutta sitä voi esiintyä vaihtelevassa määrin myös muualla paksusuolessa.1
Tässä katsauksessa käytetään useita divertikkeliin liittyviä termejä. Divertikkelien esiintymistä paksusuolessa ilman avointa tulehdusta kutsutaan divertikuloosiksi tai komplisoitumattomaksi divertikkelitaudiksi (UDD). Se voi olla oireinen tai oireeton. Termiä ”akuutti paksusuolen divertikuliitti” (ACD) käytetään kuvaamaan divertikkelien tulehdusta, joka voi edetä komplikaatioiksi (komplisoitunut ACD). On myös olemassa krooninen divertikuliitti, joka johtuu toistuvasta divertikuliitista tai divertikuliin liittyvän segmentaalisen koliitin kehittymisestä. Yhteenvetona voidaan todeta, että divertikkelitaudin kliininen kirjo on laaja.
Taudin luonnollista kulkua koskevissa tutkimuksissa todetaan, että suuri enemmistö divertikkelipotilaista (noin 80 %) pysyy koko elämänsä ajan oireettomana. Niistä 15-20 %:sta, joille kehittyy oireita, noin 1/4:llä on lopulta oireinen kivulias divertikkelitautikohtaus ilman tulehdusta, ja jopa 10-25 %:lla on ACD-kohtaus. Noin 1-2 % tarvitsee sairaalahoitoa ja 0,5 % leikkausta. Divertikkelit aiheuttavat suurimman osan (24-42 %) alemman ruoansulatuskanavan verenvuotojaksoista.2-4
Fysiopatologia ja oireiden kehittyminen
Paksusuolen divertikkeli on limakalvon ja submukoosan tyrä, joka vastaa heikkoa kohtaa, jossa vasa recti läpäisee tunica musculariksen. Divertikkelitaudin patogeneettiset mekanismit tunnetaan edelleen huonosti, mutta yleisesti tunnustetaan kuitenkin, että ne liittyvät todennäköisesti ruokavalion, paksusuolen mikrobiston, geneettisten tekijöiden, paksusuolen motiliteetin ja rakenteen välisiin monimutkaisiin vuorovaikutussuhteisiin, jotka johtavat ajan myötä paksusuolen divertikkelien muodostumiseen.5 Ks. kuva 1. Painter ja Burkitt julkaisivat vuonna 1971 kuuluisan hypoteesinsa, jonka mukaan divertikkelitaudit johtuvat paksusuolen ylipaineesta, joka johtuu ravintokuidun riittämättömään saantiin perustuvasta segmentoitumisesta. Vastauksena lisääntyneeseen intraluminaaliseen paineeseen voi kehittyä ulostyöntymiä, jotka työntyvät esiin potentiaalisesti heikoille alueille.6 Kapeakaulaisen divertikkelin pysähtyminen tai tukkeutuminen voi johtaa bakteerien liikakasvuun ja paikalliseen kudosiskemiaan, joka lopulta johtaa perforaatioon.7 Sittemmin lukuisissa havainnointitutkimuksissa on pyritty osoittamaan kuitujen mahdollinen vaikutus divertikkelitautien ehkäisyyn. Useimmissa niistä päädyttiin siihen, että UDD:n riski oli käänteisesti yhteydessä ravintokuidun saantiin.8-10 Näiden todisteiden perusteella useimmissa nykyisissä ohjeissa ja kannanotoissa suositellaan runsaskuituista ruokavaliota divertikkelitautien ehkäisemiseksi.11-15 Tämä hypoteesi on kuitenkin viime aikoina kyseenalaistettu, sillä: 1) kuitujen saannin ja divertikuloosin käänteinen yhteys on kyseenalaistettu eräissä viimeaikaisissa epidemiologisissa tutkimuksissa16,17 ja 2) uusia patogeneettisiä hypoteeseja, kuten neuropaattista ja myopaattista tautia koskevat hypoteesit, nousevat esiin18.-22 Muita tekijöitä, jotka on yhdistetty divertikkelitaudin lisääntyneeseen riskiin, ovat fyysinen passiivisuus, ummetus, liikalihavuus ja tupakointi23 .-27
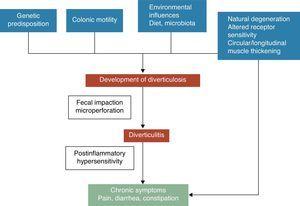
Oireiden kehittyminen divertikkelitaudissa liittyy todennäköisesti monimutkaisiin vuorovaikutussuhteisiin geneettisten ominaisuuksien, paksusuolen rakenteen, suolen motiliteetin matala-asteisen tulehduksen ja postinflammatorisen yliherkkyyden välillä.
Komplisoitumattoman divertikkelitaudin (UDD) ja oireiden välinen yhteys on epävarma. On jonkin verran näyttöä siitä, että kivulias divertikkelitauti saattaa olla tila, joka liittyy tulehdukseen ja sen vaikutuksiin paksusuolen neuromuskulaariseen toimintaan.22-28 Krooninen, matala-asteinen suolistotulehdus aiheuttaisi sensoris-motorisen toimintahäiriön, joka johtaisi oireiden kehittymiseen ja/tai pysyvyyteen. Suoliston mikroflooran muutokset voisivat olla yksi matala-asteisen tulehduksen aiheuttamista oletetuista mekanismeista. Bakteerien liikakasvu, jota ulosteen pysähtyminen divertikkelien sisällä edesauttaa, voisi edistää kroonista matala-asteista tulehdusta, joka herkistää sekä sisäisiä primaarisia efferentteja että ulkoisia primaarisia afferentteja hermosoluja. Nämä muutokset voivat johtaa sileän lihaksen hypertrofiaan ja lisääntyneeseen herkkyyteen vatsaontelon venytykselle ja lopulta oireiden kehittymiseen.3,22 Ks. kuva 1.
Kuten edellä mainitsimme, useimmat paksusuolen divertikuloosia sairastavat pysyvät oireettomina, mutta lopulta heille voi kehittyä komplikaatioita, kuten ACD:tä tai divertikkelivuoto. Tässä artikkelissa keskitymme ACD:hen. Tämän tapahtuman kliininen ilmenemismuoto riippuu useista tekijöistä, kuten perforaation koosta, ekstrakoolonisen kontaminaation tasosta ja elimistön kyvystä hillitä tätä kontaminaatiota.29,30
Divertikkelitaudin hoitoKomplisoitumattoman divertikkelitaudin (UDD)
Potilaille, joilla esiintyy oireetonta UDD:tä,2 voidaan suositella runsaskuituista ruokavaliota, koska siitä voi olla ennaltaehkäisevää etua oireilevan UDD:n ja sen aiheuttaman oireisen UDD:n ja sen aiheuttamien komplikaatioiden ehkäisyssä. Ei ole näyttöä siitä, että muista lääkkeistä olisi hyötyä näille potilaille.
Oireisen UDD:n hoidon hyödystä on enemmän näyttöä. Yleisin oire on vatsakipu, jota voi pahentaa syöminen ja lievittää ulostaminen tai ilmavaivat. Muita oireita ovat pahoinvointi, ripuli, ummetus ja turvotus. Yli 61 %:lla oireista UDD:tä sairastavista potilaista, jotka eivät ryhdy mihinkään hoitotoimenpiteisiin oireiden uusiutumisen estämiseksi, oireet muuttuvat vuoden kuluessa, ja noin 4 %:lle kehittyy komplikaatioita.31
Hoitoon on ehdotettu viittä ainetta (ks. kuva 2):

Komplisoitumattoman divertikkelitaudin hoito. Vaikutusmekanismit.
A) Runsaasti kuitua sisältävä ruokavalio tai täyteaineet
Monissa satunnaistetuissa kontrolloiduissa tutkimuksissa (RCT) ja muissa toimenpidetutkimuksissa on arvioitu kuitujen vaikutusta oireisen UDD:n hoidossa, mutta tulokset ovat epäjohdonmukaisia.32-37 Joka tapauksessa kuitua suositellaan oireisen UDD:n ennaltaehkäisyssä ja hoidossa sekä ACD:n ennaltaehkäisyssä useimmissa nykyisissä ohjeissa ja kannanotoissa.11-15
B) Antibioottihoito
Oireisen UDD:n hoidossa käytettävien antibioottien käyttöperusteita ei ole selkeästi vahvistettu. Viimeaikaiset tutkimukset viittaavat siihen, että suolistomikrobiston muutokset (suolistobakteerien liikakasvu) voivat osaltaan vaikuttaa oireiden kehittymiseen hiilihydraattien käymisen kautta tapahtuvan suolistokaasun liiallisen tuotannon vuoksi. Systemaattisten vaikutusten välttämiseksi sopivimpia antibiootteja näyttävät olevan huonosti imeytyvät mikrobilääkkeet, jotka vaikuttavat suolistopatogeeneihin mutta joilla on minimaalinen systemaattisen toksisuuden tai sivuvaikutusten riski. Rifaksimiinia on ehdotettu.
Rifaksimiini
Rifaksimiini on ei-systemaattinen rifamysiinianalogi, jolla on laaja aktiivisuusspektri in vitro. Rifaksimiini voi vähentää suolistoflooran metabolista aktiivisuutta, lisätä ulostemassaa ja voi myös hävittää bakteerien liikakasvua. Tämän antibiootin turvallisuus- ja siedettävyysprofiili on korkea.33,38 Rifaksimiinin pitoisuus plasmassa on minimaalinen, joten ei-enteroottiset patogeenit eivät altistu valikoivalle paineelle ja bakteerien resistenssin riski on pieni.39 Kolmessa avoimessa ja kahdessa kaksoissokkotutkimuksessa40-44 on tutkittu rifaksimiinin ja kuitujen jaksoittaisen annon tehoa oireiden vähentämisessä pelkkiin kuituihin verrattuna. Näitä tutkimuksia on analysoitu järjestelmällisessä katsauksessa ja kahdessa meta-analyysissä.44-46 Niissä päädyttiin siihen, että yhdistelmähoito on tehokasta oireiden lievittämisessä yhden vuoden kuluttua UDD-potilailla. Pelkkää kuitua saaneista potilaista 35 prosenttia oli oireettomia, kun taas yhdistelmähoitoa saaneista potilaista 64 prosenttia oli oireettomia. Oireiden lievittämiseksi tarvittava hoitomäärä oli kolme rifaksimiinia verrattuna lumelääkkeeseen ja yhdeksän komplikaatioiden välttämiseksi. Yhteenvetona voidaan todeta, että parhaat tulokset on saatu käyttämällä liukoisen kuidun, kuten glukomannaanin, ja rifaksimiinin yhdistelmää 1 viikko joka kuukausi.
C) Probiootit
Probiootit ovat eläviä mikro-organismeja, jotka voivat palauttaa suoliston kommenssiflooran, joka on saattanut muuttua divertikkelitaudissa staasin ja paksusuolen lyhentyneen läpimenoajan vuoksi.47 Valitettavasti sen käytöstä oireisen UDD:n hoidossa on vain vähän tietoa, ja useimmat tutkimukset ovat pieniä ja kontrolloimattomia. Suurin osa niistä osoittaa oireiden paranemista.48-50
Probiootteja on tutkittu myös yhdessä 5-aminosalisylaatin (5-ASA) kanssa. Tursi ja kollegat ovat tehneet kolme RCT-tutkimusta, joissa verrattiin 5-ASA:ta yksinään, probiootteja yksinään tai yhdistelmähoitoa.51-53 Sekä 5-ASA että probiootit näyttivät olevan tehokkaita oireisen UDD:n ehkäisyssä, mutta niiden yhdistelmä oli parempi. Saman tutkijaryhmän hiljattain julkaisemassa kaksoissidonnaisessa RCT:ssä päädyttiin siihen, että sekä syklinen mesalatsiini että Lactobacillus casei subsp DG, erityisesti yhdistelmänä, näyttävät olevan lumelääkettä parempia oireisen UDD:n remissiota ylläpitävässä hoidossa.54 Yhteenvetona voidaan kuitenkin todeta, että tutkimusten huonot tutkimusasetelmat ja pieni koko eivät salli lopullisia johtopäätöksiä.
D) 5-ASA: mesalatsiini
Mesalatsiinilla on tulehdusta ehkäiseviä ja hapettumista estäviä vaikutuksia. Gatta ym.55 julkaisivat vuonna 2010 Cochranen systemaattisen katsauksen, jossa arvioitiin 5-ASA:n merkitystä divertikkelitautipotilailla. Kirjoittajat päättelivät, että 5-ASA voi olla tehokas tämän taudin hoidossa ja että jokapäiväinen mesalatsiinin anto oli parempi kuin syklinen anto uusiutumisen estämiseksi. Heidän havaintojensa vahvistamiseksi tarvitaan laadukkaita, hyvin suunniteltuja RCT-tutkimuksia. Ensimmäisessä plasebokontrolloidussa kaksoissokkotutkimuksessa todettiin mesalatsiinin tehoavan kivunlievitykseen akuuttia UDD:tä sairastavilla potilailla.56 Lisäksi on kaksi mielenkiintoista RCT-tutkimusta, jotka osoittivat, että mesalatsiinista on hyötyä rifaksimiiniin verrattuna oireiden uusiutumisen estämisessä, ja että se on onnistunut yhtä hyvin pitkäkestoisen remissioprosessin ylläpitämisessä kuin probioottinen Lactobacillus casei53,57 .
E) Antikolinergiset/antiespasmodiset aineet
Paksusuolen hipermotiliteetti divertikuloosissa viittaa siihen, että antispasmodiset aineet, kuten disyklomiini ja hyoscyamiini, saattavat parantaa oireita vähentämällä lihassupistusta. Tätä hyötyä vahvistavia RCT-tutkimuksia ei kuitenkaan ole.
F) Vältä tulehduskipulääkehoitoa
Monissa kontrolloiduissa tutkimuksissa on osoitettu, että tulehduskipulääkkeet ovat riskitekijä oireiden, ACD:n, perforaation ja verenvuodon kehittymiselle.7,58-60 Tulehduskipulääkkeiden käyttäjillä on suurempi riski sairastua oireilevaan divertikkelitautiin kuin ei-käyttäjillä (RR-arvot: 1,5, CI-arvot 95 %:n luokkaa: 1,1 – 1,1,1).58 Ja komplisoitunutta divertikkelitautia sairastavilla potilailla tulehduskipulääkkeitä käytettiin runsaammin kuin kontrolliryhmissä, joilla ei ollut sairautta. Oletettiin, että tämä lisääntynyt riski johtui limakalvovauriosta, joka johti paksusuolen limakalvon heikentyneeseen estotoimintaan, joka sallii tulehdusta aiheuttavien bakteerien siirtymisen.
G) D-vitamiinitasot
Näyttää siltä, että ACD:n esiintyvyyteen on liittynyt maantieteellistä ja kausittaista vaihtelua. Tämän vuoksi Maguire et al. tekivät kaksi mielenkiintoista havainnointitutkimusta, jotka osoittivat, että alhaisemmat D-vitamiinitasot ja vähäinen UV-valoaltistus (UV-valoaltistus määrittää D-vitamiinistatuksen) liittyvät merkittävästi suurempaan ACD:n riskiin. Tarvitaan lisää laadukkaita tutkimuksia ennen suosituksen antamista.61,62
Akuutin paksusuolen divertikuliitin (ACD)
Vaikka suurin osa divertikuloosia sairastavista ihmisistä pysyy oireettomina, arviolta noin 10-25 %:lle heistä kehittyy vasemmanpuoleinen ACD-episodi.63 Yleensä kliininen diagnoosi ei ole riittävän tarkka, ja radiologiset menetelmät ovat aiheellisia. Potilailla, joilla on lieviä oireita (useimmilla) ja joilla ei ole merkkejä komplisoituneesta ACD:stä, vasemman alavatsan kipu, oksentelun puuttuminen ja C-reaktiivinen proteiini >50 mg/l voivat riittää diagnoosin tekemiseen.64,65 Jos kuvantaminen on aiheellista, tehokkain lähestymistapa on todennäköisesti ehdollinen strategia, jossa ensimmäisenä tekniikkana on ultraäänitutkimus, jota seuraa tietokonetomografia (CT), jos ultraäänitutkimus ei ole yksiselitteinen tulos tai jos sen tulokset ovat epävarmoja. TT-tutkimusten määrää voidaan vähentää 50 prosentilla. Hinchey ja muut ehdottivat vuonna 1978 ACD:n luokittelua, jota muutettiin myöhemmin.66,67 Siinä erotetaan viisi ACD:n vaihetta: vaihe 0, kliinisesti lievä divertikuliitti, vaihe I (a: perikolinen tulehdus ja b: absessi
cm primaaritulehduksen läheisyydessä), vaihe II, vatsaontelon sisäinen, lantion sisäinen tai retroperitoneaalinen absessi tai primäärisestä tulehduksesta etäällä sijaitseva absessi, vaihe III, generalisoitunut märkivän vatsakalvotulehduksen peritoniitti, ja vaihe IV, ulosteperitoniitti. Ks. kuva 3.

Algoritmi akuutin paksusuolen divertikuliitin hoitoon.
Komplisoitumattoman ACD:n hoito (Hinchey-vaihe 0 tai Ia)
Suurinta osaa komplisoitumattomasta ACD:stä voidaan hoitaa turvallisesti konservatiivisesti, ja hoidon onnistumisprosentti on 70 %:n ja 100 %:n välillä.14 Avohoito voi mahdollistaa merkittävät kustannussäästöt terveydenhuoltojärjestelmille. Komplisoitumattoman ACD:n sairaalahoidon kriteerit ovat merkittävä tulehdus (mukaan lukien kuume tai vatsakalvotulehdus), suun kautta otettavien nesteiden sietämättömyys, yli 80-85 vuoden ikä, immunosuppressio tai vakavat liitännäissairaudet. Useimmissa tapauksissa lyhyt sairaalassaoloaika riittää. Ei ole näyttöä siitä, että ruokavaliorajoitukset vaikuttaisivat hoitotuloksiin, vaikka useimmat lääkärit yleensä suosittelevat selkeää nestemäistä ruokavaliota.
Yksi suurimmista viimeaikaisista muutoksista komplisoitumattoman ACD:n hoidossa on antibioottien käytön väheneminen. Tuoreessa Cochrane-katsauksessa, jossa käytettiin ainoastaan kvalitatiivista lähestymistapaa (ilman meta-analyysiä), todettiin, että parhaat saatavilla olevat tiedot eivät tue sen rutiinikäyttöä.68 Antibiootit eivät nopeuta toipumista eivätkä estä komplikaatioita tai uusiutumista. Siksi antibioottien käyttö tässä tapauksessa on kyseenalaista. Ne olisivat todennäköisesti aiheellisia potilaille, joilla on merkkejä yleistyneestä infektiosta, septikemian tai bakteremian merkkejä ja immuunipuutteisille potilaille. Suositellut hoidot perustuvat kliiniseen konsensukseen. Erilaisia antibiootteja voidaan käyttää ampisilliinista kolmannen sukupolven kefalosporiineihin, kunhan ne tehoavat grampositiivisiin, gramnegatiivisiin ja anaerobisiin bakteereihin. Siprofloksasiinin ja metronidatsolin yhdistelmä on luultavasti eniten määrätty suun kautta annettava hoito. Jos tämä yhdistelmä on huonosti siedetty, ampisilliini-sulfabaktaami voi olla hyvä valinta. Toisaalta viimeaikaiset tiedot ovat osoittaneet, että suonensisäisestä antibioottihoidosta ei ole etua suun kautta annettaviin antibiootteihin nähden eikä suonensisäisestä 4 päivän hoidosta 7 päivän hoitoon nähden.69-71 Yleensä kliininen paraneminen havaitaan 3-4 päivän kuluessa hoidosta. Lopuksi suositellaan sairaalahoitoa suonensisäisellä antibiootilla, kun potilas ei pysty ottamaan ruokaa suun kautta, hänellä on vakava liitännäissairaus tai hänen vointinsa ei parane avohoidolla.
Komplisoituneen ACD:n hoito (Hinchey-vaiheet Ib-IV)ACD Hinchey Ib tai II: absessi
Jopa 15 %:lle ACD:tä sairastavista potilailta kehittyy abskessi.67 Abskessinmuodostusta aiheuttavan ACD:n optimaalisimmasta hoitomuodosta ei ole laadukasta näyttöä. Sairaalahoito on aiheellista. Koko on tärkeä tekijä hoidon onnistumisen kannalta. Pienemmissä paiseissa (
cm) suositellaan konservatiivista hoitoa laajakirjoisilla antibiooteilla. Se onnistuu jopa 70 %:ssa.72 Kun konservatiivinen hoito epäonnistuu tai suuremmissa paiseissa on tehtävä perkutaaninen dreeni. Se onnistuu jopa 80 %:lla.73 Leikkaus on pelastushoito, kun edellä mainitut hoidot epäonnistuvat.ACD Hinchey III tai IV: märkäinen tai ulosteperitoniitti
Peritoniitti on vakavin komplikaatio, jonka kuolleisuus on 14 %. Vaikka näyttöä ei ole, varhaista leikkausta pidetään näiden potilaiden vakiohoitona. Leikkausmenetelmän valintaan vaikuttavat potilaan olosuhteet, leikkauslöydökset ja kirurgin kokemus. Kriittisesti sairaille potilaille, joilla on hemodynaaminen epävakaus, suositellaan Hartmannin toimenpidettä. Hemodynaamisesti stabiileilla potilailla ensisijaisena vaihtoehtona on kuitenkin pidettävä primaarista anastomoosia proksimaalisen ulosteenpoiston kanssa tai ilman sitä.14,74
Kansainvälisissä ohjeissa suositellaan perinteisesti endoskopiaa ACD-episodin jälkeen paksusuolen syövän poissulkemiseksi. Tämä suositus perustuu ainoastaan asiantuntijalausuntoihin. Viimeaikaiset retrospektiiviset tutkimukset ja järjestelmällinen katsaus75-80 osoittavat, että syöpätapausten määrä näillä potilailla on melko alhainen. Tämän tuoreen näytön perusteella tehokkain strategia voi olla ohjata kolonoskopiaan vain ne potilaat, joilla on jatkuvia oireita tai joilla on epäilyttäviä CT-löydöksiä. Tiukkaa suositusta varten tarvitaan kuitenkin lisää tutkimuksia.
Hoito ACD-episodin jälkeen Uusintakohtausten ehkäisy
Yksi ACD-episodin jälkeen noin kolmasosa sairastuu toiseen ACD-episodiin, ja toisen episodin jälkeen kolmasosa sairastuu uudelleen.73,74 Näyttöä optimaalisen hoidon määrittelemisestä ACD-episodin jälkeen uuden episodin ehkäisemiseksi on kuitenkin niukasti.
A) Runsaasti kuitua sisältävä ruokavalio
Kun akuutti episodi on hävinnyt, suositellaan yleisesti runsaasti kuitua sisältävää dieettiä, jolla pyritään vähentämään episodin uusiutumista. Kuitupitoista ruokavaliota ACD-potilailla koskevissa RCT-tutkimuksissa on kuitenkin saatu ristiriitaisia tuloksia. Hiljattain julkaistussa runsaskuituista ruokavaliota käsittelevässä järjestelmällisessä katsauksessa ei löydetty yhtään tutkimusta, jossa olisi tutkittu kuitujen merkitystä ACD:n uusiutumisen ehkäisyssä.26,81 Joitakin elintarvikkeita (siemenet, popcorn ja pähkinät) vältetään klassisesti, koska ne teoriassa pääsevät divertikkeliin, tukkivat sen tai ärsyttävät sitä. Strate ym. eivät kuitenkaan havainneet laajassa prospektiivisessa tutkimuksessaan yhteyttä lisääntyneeseen ACD:n riskiin. Siksi näiden elintarvikkeiden jättämistä pois ruokavaliosta ei pitäisi suositella.82 Myös painonpudotuksella ja tupakoinnin lopettamisella voi olla suotuisa vaikutus ACD:n ennaltaehkäisyyn.9,83
B) Antibiootit
Kolme viimeaikaista systemaattista katsausta, joissa arvioitiin syklisen rifaksimiinin roolia ACD:n uusiutumisen ehkäisemisessä, eivät kuitenkaan osoittaneet selkeää etua.46,84,85 Patofysiologisesta näkökulmasta katsottuna uskottava selitys rifaksimiinin tehottomuudelle uusiutumisen ehkäisemisessä voisi olla se, että syklinen hoito ei ehkä kontrolloi paksusuolen bakteeripopulaatiota koko kuukauden ajan, koska paksusuolen bakteeripopulaatio palautuu 7-14 päivän kuluessa rifaksimiinin lopettamisesta. Tuore espanjalainen avoin RCT-tutkimus on kuitenkin osoittanut, että syklinen rifaksimiini voi parantaa oireita ja ylläpitää remissiojaksoja ACD:n jälkeen.86 Uusiutumisia esiintyi 10,4 %:lla potilaista, jotka saivat rifaksimiinia ja kuituja, verrattuna 19,3 %:iin, jotka saivat vain kuituja. Lisäksi potilailla, joilla diagnoosi oli tehty ensimmäisen kerran ≥ 1 vuoden kuluttua, oli suurempi pahenemisvaiheen riski (OR 3,34, 95 % CI: 0,01-12,18). Lisätutkimuksia kuitenkin tarvitaan, koska tällä hetkellä ei voida antaa suosituksia. Muiden antibioottien käytöstä tässä yhteydessä ei ole näyttöä.
C)) Probiootit
Joissain avoimissa tutkimuksissa on tutkittu probioottien merkitystä ACD:n uusiutumisen ehkäisyssä. Giaccari ym. arvioivat yli 20 vuotta sitten Lactobacillus sp:n roolia rifaksimiinin jälkeen 79 potilaalla, joilla oli divertikuliitin jälkeinen paksusuolen ahtauma. Potilaista 88 prosenttia pysyi oireettomana 12 kuukauden ajan.87 Tämä havainnointitutkimus oli ensimmäinen, jossa ehdotettiin probioottien mahdollista merkitystä tässä tilanteessa. Tuoreemmassa tutkimuksessa arvioitiin yhdistelmähoitoa; balsalatsidia ja VSL#3:a (kahdeksan lajin probioottiseos). Yhdistelmähoitoa saaneista henkilöistä 73 % oli 12 kuukauden kuluttua oireettomia verrattuna 53 %:iin probioottimonoterapiaa saaneista henkilöistä (p>0,05).52 Yhteenvetona voidaan todeta, että probiootit näyttävät olevan tehokkaita ACD:n uusiutumisen ehkäisyssä, mutta hyvin suunniteltuja tutkimuksia ei ole tehty.
D) 5-ASA
Monissa kaksoissokkoutetuissa ja avoimissa RCT-tutkimuksissa on selvitetty mesalatsiinin roolia ACD:n uusiutumisen ehkäisyssä. Valitettavasti useimmissa niistä ei ole todettu mesalatsiinista olevan hyötyä lumelääkkeeseen verrattuna uusiutumisen ehkäisyssä.88-90 Raskin ym. ovat hiljattain julkaisseet kaksi mielenkiintoista ja identtistä vaiheen 3 kaksoissokkoa, lumelääkettä sisältävää RCT-tutkimusta (PREVENT1 ja PREVENT2), jotka niin ikään osoittavat, että mesalatsiini ei ole lumelääkettä parempi ACD:n uusiutumisen ehkäisemisessä.91 Myös yhdistelmähoitoa 5-ASA:n ja rifaksiminin yhdistelmähoitoa on arvioitu useissa tutkimuksissa. Trivedi ja Das tarkastelivat tietoja viidestä RCT-tutkimuksesta ja yhdestä avoimesta tutkimuksesta, joihin osallistui yhteensä yli 600 potilasta, ja totesivat, että yhdistelmä näyttäisi olevan parempi kuin pelkkä rifaksimiini pelkän ACD:n uusiutumisen ehkäisemisessä.92
E) Leikkaus
Kun vielä muutama vuosi sitten suositeltiin elektiivistä leikkaushoitoa kahden komplisoitumattoman ACD-tapauksen tai yhden komplisoituneen ACD-tapauksen jälkeen, jotta voitaisiin vähentää sairastuvuus- ja kuolleisuusalttiutta, joka aiheutuu ACD:n uusiutumisesta. Mutta elektiiviseen leikkaukseen liittyy myös lisääntynyt morbiditeetti-kuolleisuusriski.93 Tämän vuoksi on tärkeää punnita leikkauksen aiheuttamaa sairastuvuutta ja kuolleisuutta suhteessa komplisoituneiden uusintakohtausten riskiin ja oireiden vakavuuteen.
Uudemmat tiedot osoittavat, että ACD:n luonnollinen taudinkulku on paljon hyvänlaatuisempi kuin aiemmin luultiin.73,94,94 Pitkän aikavälin uusiutumisriski on alhaisempi kuin aiemmin uskottiin, ja myöhempien kiireellisten leikkausten (3-7 %) ja kuoleman (95 osoitti, että 16 % tapauksista, joissa oli ensimmäinen ACD, leikattiin kiireellisesti verrattuna vain 6 %:iin uusiutuvissa tapauksissa, ja että 30 päivän kuolleisuus ensimmäiseen episodiin oli myös korkeampi verrattuna toistuviin tapahtumiin (3 % vs. 0 %). Itse asiassa suurimmalla osalla komplisoitunutta ACD:tä sairastavista potilaista ei ole sairaushistoriaa.96 On myös ehdotettu, että uusiutuva ACD voi suojata perforaatiolta, mikä saattaa johtua tulehduksen aiheuttamasta adheesiomuodostuksesta.95 Näin ollen ACD:n jälkeisen elektiivisen leikkauksen politiikka ei vähennä uusintaleikkauksen todennäköisyyttä (jopa 3 %) eikä suojaa täysin uusiutumiselta. Toisaalta parantunut diagnostiikka ja hoitomuodot ovat vähentäneet komplisoituneen ACD:n kuolleisuutta. Näiden uusien tietojen vuoksi American Society of Colon and Rectum Surgeons suosittelee uusimmissa ohjeissaan, että ACD:stä toipumisen jälkeinen elektiivinen sigmoidiresektio olisi tehtävä tapauskohtaisesti14 , ja katsoo, että aiempien leikkausjaksojen määrä ei ole hyvä indikaattori valittaessa ehdokkaita elektiiviseen leikkaukseen. Lääkäreiden olisi otettava huomioon potilaan terveydentila ja ikä, kohtauksen (kohtausten) esiintymistiheys ja vakavuus sekä akuutin kohtauksen jälkeen jatkuvat oireet.14
On hyvin vaikea ennakoida, mitkä ACD-tapaukset uusiutuvat. ACD:n ensimmäisen kohtauksen CT-asteikollinen vaikeusaste näyttää ennustavan epäsuotuisaa luonnollista taudinkulkua. Vasemmanpuoleinen ACD, >5 senttimetriä paksusuolta mukana ja retroperitoneaalinen abskessi ennustivat uusiutumista, ja ne on otettava huomioon.97 Ei ole päästy yksimielisyyteen siitä, pitäisikö nuorta ikää (82 Tämänhetkisen näytön mukaan ikää ei pitäisi pitää indikaationa elektiiviselle leikkaukselle, koska se ei näytä liittyvän taudin vaikeaan kulkuun lääkkeellisesti hoidetun ACD:n jälkeen. Kun kuitenkin otetaan huomioon, että ACD:n esiintyvyys on lisääntynyt nuoremmilla potilailla, lisätutkimukset ovat tarpeen tämän erityiskysymyksen selvittämiseksi.
Erikoistapauksia ovat immuunipuutteiset henkilöt. Kohorttitutkimukset osoittavat, että näillä potilailla oli suuri komplisoituneen toistuvan ACD:n riski (5-kertainen perforaatioriski) ja suuri riski joutua päivystysleikkaukseen.98 Siksi alhaisempi kynnys valita leikkaus voi hyödyttää näitä potilaita.14 Biondo ym. tuoreessa tutkimuksessaan osoittavat kuitenkin, että immuunipuutteisilla potilailla oli merkittävästi korkeampi kuolleisuus, mutta vain ensimmäisellä jaksolla. Siksi asiasta on kiistaa.99
Seurausten hoitoA) Fisteli
Fisteli syntyy, kun divertikulaarinen flegma tai paise repeää viereiseen elimeen. Fisteli ilmaantuu alle 5 %:lle ACD-potilaista. Yleisimpiä ovat kolovesikaaliset ja kolovaginaaliset fistelit. Oletettavasti useimmille potilaille voitaisiin tehdä yksivaiheinen operatiivinen resektio, jossa fisteli suljetaan ja tehdään primaarianastomoosi. Muut fistelit, kuten koloenteri- tai koluteriinifistelit, ovat harvinaisia.100,101
B) Obstruktio
Takaisin toistuvat ACD-episodit, jotka voivat olla subkliinisiä, voivat aiheuttaa paksusuolen kroonisen ahtauman ilman jatkuvaa tulehdusta. Voi syntyä korkea-asteinen tai täydellinen tukos. Tukoksen hoitamiseksi on ensin suljettava pois pahanlaatuinen etiologia. Kun kasvain on riittävästi poissuljettu ja ACD:tä ei ole, endoskooppinen dilataatio tai väliaikainen dekompressio metallistentin avulla voivat olla hoitovaihtoehtoja.102 Myöhemmin voidaan toteuttaa myöhempi yksivaiheinen resektio ilman diversiota.
Divertikuloosiin liittyvän segmentaalisen koliitin hoito
Se määritellään krooniseksi tulehdukseksi, joka koskee paksusuolisegmentin limakalvojen välistä tulehdusta. Peräsuoli ja oikea paksusuoli säästyvät. Siitä on tullut erillinen kliininen ja patologinen häiriö, ja siihen liittyy usein verisiä ulosteita. Patogeneesi on tuntematon. Histologisten muutosten kirjo vaihtelee lievästä epäspesifisestä tulehduksesta tulehduksellisen suolistosairauden kaltaisiin muutoksiin. Tämän vuoksi erotusdiagnostiikka on usein vaikeaa. Useimmat potilaat toipuvat täysin muutamassa viikossa tai kuukaudessa. Joitakin heistä hoidetaan aluksi suun kautta otettavalla 5-ASA:lla, mutta todennäköisesti nämä lääkkeet eivät ole tarpeen, koska useimmat tapaukset paranevat spontaanisti.103
Johtopäätökset
Oireisen UDD:n hoidon tavoitteena on ehkäistä komplikaatioita ja vähentää oireita. Tämänhetkisen näytön mukaan kuitu ja syklinen rifaksimiini tai mesalatsiini ja probiootit näyttävät olevan tehokkaimpia hoitomuotoja. ACD:ssä antibiootit näyttävät olevan edelleen hoidon peruspilari, ja avohoitoa pidetään optimaalisena lähestymistapana suurimmalle osalle potilaista, joilla on komplisoitumaton ACD. Komplisoituneessa ACD:ssä tarvitaan kuitenkin sairaalahoitoa ja suonensisäisiä antibiootteja. Tällä hetkellä päivystyskirurgian rooli on muuttumassa. Useimmat divertikuliittiin liittyvät paiseet voidaan hoitaa suonensisäisesti annettavilla antibiooteilla ja/tai perkutaanisella dreneerauksella, ja päivystysleikkausta pidetään vakiohoitona vain potilailla, joilla on vatsakalvotulehdus. Lopuksi, elektiivinen leikkaus ACD:stä toipumisen jälkeen tulisi tehdä tapauskohtaisesti.
Tekijöiden panos
Gargallo CJ, Sopeña F ja Lanas A osallistuivat tasapuolisesti tämän artikkelin suunnitteluun, muokkaukseen ja arvosteluun.
Esintäristiriita
Tohtori Carla J. Gargallo ja tohtori Federico Sopeña eivät ilmoita eturistiriitaa. Tohtori Angel Lanas on toiminut AlfaWassermanin neuvonantajana.
Mitä?
