Az Enterobacteriaceae családba tartozó gram-negatív bacillus, A Serratia marcescens olyan organizmus, amely ismert bakteriémia, tüdőgyulladás, húgyúti fertőzés, endokarditis, meningitis és szeptikus arthritis okozója.1 A S marcescens által okozott cellulitis és nekrotizáló fasciitis (NF) szokatlan eseteiről is beszámoltak.2,3 Ezt az entitást kezdetben immunhiányos és nem immunhiányos betegeknél írták le.4 Közösségi és nosocomiális esetekről is beszámoltak.3
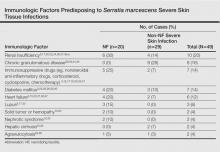
Egy 68 éves, kórosan elhízott nő magas vérnyomással, diabetes mellitusszal, krónikus veseelégtelenséggel, krónikus vénás elégtelenséggel és bal lábszár nyiroködémával került sürgősségi osztályunkra. Fájdalma és körkörös erythema volt, többszörös tályoggal a bal lábán 2 hete. Trauma, fekély, injekció vagy állatharapás nem szerepelt a kórtörténetben. A megjelenéskor nem volt láza, és a vitális paraméterek normálisak voltak. Empirikus kezelést kezdtek szájon át szedett amoxicillinnel (napi 6 g) és amoxicillin-clavulanáttal (napi 375 mg). Negyvennyolc órával később a gyulladás, a fájdalom és a tályogok súlyosbodtak (1A. ábra). A laboratóriumi vizsgálatok emelkedett fehérvérsejtszámot (15,9×109⁄L, 86%-ban neutrofilekkel ) és emelkedett C-reaktív fehérje szintet (322 mg/L ) mutattak. A humán immundeficiencia vírus szerológia negatív volt. A tályog tűs aspirációja S marcescens-t mutatott ki. Egy második aspiráció megerősítette ugyanannak a szervezetnek, a vad típusú S marcescensnek a jelenlétét, amely rezisztens volt az amoxicillinnel és klavulánsavval, első generációs cefalosporinnal és tobramicinnel szemben, de érzékeny volt a piperacillinre, harmadik generációs cefalosporinokra, amikacinra, ciprofloxacinra és ko-trimoxazolra. Intravénás cefepim, egy harmadik generációs cefalosporin adását kezdték el. A következő 48 órában a betegnél súlyos szepszis alakult ki zavartsággal, akut veseelégtelenséggel (kreatinin: 231 µmol/l vs. 138 µmol/l a kiindulási értéken 9,11,35-38,40; gyermekkori krónikus granulomatosus betegséghez társuló tályogok, gumma vagy pyoderma gangrenosum-szerű elváltozások 29,44,45; fájdalmas csomók másodlagos tályogokkal 31-34,46; akut bullous cellulitis 8,10,30; fekélyek másodlagos fertőzései 35,40; tályogok immunkompetens betegnél 41; és nekrotizáló bőrfekély 36). Az alsó végtagok gyakran érintettek (NF esetek, n=13; nem NF esetek, n=16). A háttérben álló immunszuppressziót 14 NF és 17 nem NF esetben figyelték meg. A hajlamosító immunológiai tényezőket a táblázat foglalja össze. A helyi kockázati tényezőket, beleértve a krónikus lábödémát, traumát, műtéti sebet, töltőanyag-injekciót és fekélyt, gyakran jelentették NF és nem NF esetekben,16,20,26-28,31,32,34,35,37,38,40,46 beleértve a mi esetünket is. Műtétre 19 NF és 7 nem NF esetben volt szükség. A Serratia marcescens által közvetített NF nagyobb mortalitással járt (n=12), mint a nem-NF esetek (n=1). Az irodalomban a S marcescens-fertőzés egyéb, nem súlyos klinikai manifesztációi közé tartozott a humán immunhiányos vírusfertőzéssel járó disszeminált papuláris kitörés42 és a törzsi folliculitis.43 Betegünknél számos rizikófaktor szerepelt, többek között krónikus ödéma, diabetes mellitus, krónikus veseelégtelenség és krónikus vénás elégtelenség. A tályogok és nekrotikus szövetek esetleges jelenléte akadályozza az antibiotikum penetrációját a fertőzés helyén, és a S marcescens-cellulitis magas mortalitására való tekintettel a lehető legkorábban szisztematikusan fontolóra kell venni a műtétet.