Bevezetés
A vastagbél divertikuláris betegsége a nyugati világban a vastagbelet érintő leggyakoribb betegség. A divertikuláris betegség előfordulási gyakorisága az elmúlt évszázadban világszerte nőtt, valószínűleg az életmódbeli változások, például a dohányzás, a túlsúly, és mindenekelőtt a fizikai inaktivitás és az alacsony rosttartalmú étrend miatt. A prevalencia az életkor előrehaladtával nő, a 40 évesnél fiatalabb felnőttek körében körülbelül 5%-tól a 80 éves vagy idősebbek körében 50-70%-ig terjed; a divertikulitisszel jelentkező betegek 80%-a 50 éves vagy idősebb. A divertikulák száma a magányostól a több százig terjedhet, átmérőjük jellemzően 5-10 mm, de meghaladhatja a 2 cm-t is. A divertikulózis a betegek több mint 90%-ánál elsősorban a szigmabélben és a leszálló vastagbélben fordul elő, de különböző mértékben a vastagbél többi részében is előfordulhat.1
Ebben az áttekintésben számos divertikulummal kapcsolatos kifejezést fogunk használni. A divertikulák jelenlétét a vastagbélben nyílt gyulladás hiányában divertikulózisnak vagy szövődménymentes divertikuláris betegségnek (UDD) nevezik. Ez lehet tüneti vagy tünetmentes. Az “akut vastagbél-divertikulitisz” (ACD) kifejezést a divertikulák gyulladásának leírására használják, amely szövődményekhez vezethet vagy nem vezethet (szövődményes ACD). Létezik krónikus divertikulitisz is, a visszatérő divertikulitisz vagy a divertikulákhoz kapcsolódó szegmentális vastagbélgyulladás kialakulása miatt. Összefoglalva, a divertikuláris betegség klinikai spektruma széles.
A betegség természetes lefolyására vonatkozó tanulmányok rámutatnak, hogy a divertikulában szenvedő betegek nagy többsége (kb. 80%-a) egész életében tünetmentes marad. A 15-20%-nak, akiknél tünetek jelentkeznek, körülbelül 1/4-ének lesz végül tüneteket okozó, gyulladás nélküli, fájdalmas divertikuláris betegség epizódja, és akár 10-25%-nak is lehet ACD epizódja. Körülbelül 1-2%-ban lesz szükség kórházi kezelésre és 0,5%-ban műtétre. A divertikulumok felelősek az alsó gasztrointesztinális vérzéses epizódok többségéért (24-42%).2-4
Fiziopatológia és a tünetek kialakulása
A vastagbél divertikulum a nyálkahártya és a submucosa sérve, amely egy olyan gyenge pontnak felel meg, ahol a vasa recti behatol a tunica muscularisba. A divertikuláris betegségek patogenetikai mechanizmusai még mindig kevéssé ismertek, azonban általánosan elismert, hogy ezek valószínűleg a táplálkozás, a vastagbél mikrobióta, a genetikai tényezők, a vastagbél motilitása és szerkezete közötti összetett kölcsönhatásokhoz kapcsolódnak, amelyek idővel a vastagbél divertikulumok kialakulásához vezetnek.5 Lásd az 1. ábrát. Painter és Burkitt 1971-ben publikálta híres hipotézisét, miszerint a divertikuláris betegséget az elégtelen élelmi rostbevitelen alapuló szegmentáció miatt a vastagbélben kialakuló túlnyomás okozza. A megnövekedett intraluminális nyomás hatására a potenciális gyenge pontokon kitüremkedések alakulhatnak ki és előrenyúlhatnak.6 A szűk nyakú divertikulumban kialakuló pangás vagy elzáródás bakteriális túlszaporodáshoz és helyi szöveti iszkémiához vezethet, ami végül perforációhoz vezethet.7 Azóta számos megfigyeléses vizsgálat próbálta bizonyítani a rostok lehetséges hatását a divertikuláris betegség megelőzésére. Legtöbbjük arra a következtetésre jutott, hogy az UDD kockázata fordítottan arányos az étrendi rostbevitellel.8-10 E bizonyítékok alapján a legtöbb jelenlegi irányelvben és állásfoglalásban magas rosttartalmú étrendet ajánlanak a divertikulózis megelőzésére.11-15 Ezt a hipotézist azonban nemrégiben megkérdőjelezték, mivel: (1) a rostbevitel és a divertikulózis fordított összefüggését néhány újabb epidemiológiai tanulmány16,17 megkérdőjelezte, és (2) új patogén hipotézisek, például a neuropátiás és myopátiás hipotézisek jelentek meg.18-22 A divertikuláris betegség fokozott kockázatával összefüggésbe hozott egyéb tényezők közé tartozik a fizikai inaktivitás, a székrekedés, az elhízás és a dohányzás23.-27
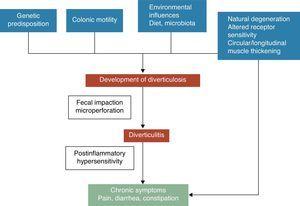
A divertikuláris betegség tüneteinek kialakulása valószínűleg a genetikai jellemzők, a vastagbélszerkezet, a bélmotilitás alacsony fokú gyulladás és a posztinflammatorikus túlérzékenység közötti összetett kölcsönhatásokhoz kapcsolódik.
A szövődménymentes divertikuláris betegség (UDD) és a tünetek közötti kapcsolat bizonytalan. Bizonyos bizonyítékok arra utalnak, hogy a fájdalmas divertikuláris betegség a gyulladással és annak a vastagbél neuromuszkuláris funkciójára gyakorolt hatásával összefüggő állapot lehet.22-28 A krónikus, alacsony fokú bélgyulladás jelenléte szenzomotoros diszfunkciót idézne elő, ami a tünetek kialakulásához és/vagy fennmaradásához vezet. A bélflóra változása lehet az egyik feltételezett mechanizmus, amely az alacsony fokú gyulladásért felelős. A baktériumok túlszaporodása, amelyet a divertikulákban lévő széklet pangása segíthet, hozzájárulhat a krónikus, alacsony fokú gyulladáshoz, amely mind az intrinzik primer efferens, mind az extrinsic primer afferens neuronokat szenzibilizálja. Ezek a változások a simaizomzat hipertrófiájához és a hasi distresszióra való fokozott érzékenységhez, végül pedig a tünetek kialakulásához vezethetnek.3,22 Lásd az 1. ábrát.
Amint fentebb említettük, a vastagbél divertikulózisban szenvedők többsége tünetmentes marad, de végül szövődmények, mint ACD vagy divertikulavérzés alakulhatnak ki. Ebben a cikkben az ACD-re összpontosítunk. Ennek az eseménynek a klinikai manifesztációja számos tényezőtől függ, beleértve a perforáció méretét, az extracolonális szennyeződés mértékét és a szervezet azon képességét, hogy ezt a szennyeződést megfékezze.29,30
A divertikuláris betegség kezeléseA szövődménymentes divertikuláris betegség kezelése (UDD)
A tünetmentes UDD-ben szenvedő betegeknél2 magas rosttartalmú diéta ajánlható, mivel annak lehetséges profilaktikus előnye a tüneti UDD és a szövődmények megelőzésében rejlik. Nincs bizonyíték arra, hogy más gyógyszerek hasznosak lennének ezeknél a betegeknél.
Tüneti UDD esetén több bizonyíték van a kezelés előnyére. A leggyakoribb tünet a hasi fájdalom, amelyet az evés súlyosbíthat, és a székletürítés vagy a puffadás enyhíthet. További tünetek a hányinger, hasmenés, székrekedés és puffadás. A tünetekkel járó UDD-ben szenvedő betegek több mint 61%-a, akik semmilyen terápiás intézkedést nem tesznek a tünetek kiújulásának megelőzésére, 1 éven belül tünetmentes lesz, és körülbelül 4%-uknál szövődmények alakulnak ki.31
A kezelésre öt szer javasolt (lásd a 2. ábrát):

A szövődménymentes divertikuláris betegség kezelése. A hatásmechanizmusok.
A) Magas rosttartalmú diéta vagy tömegnövelő szerek
Sok randomizált, kontrollált vizsgálat (RCT) és egyéb intervenciós tanulmány értékeli a rostok hatását tüneti UDD-ben, de ellentmondásos eredményekkel.32-37 Mindenesetre a rostokat a legtöbb jelenlegi irányelv és állásfoglalás ajánlja a tüneti UDD megelőzésében és kezelésében, valamint az ACD megelőzésében.11-15
B) Antibiotikum-terápia
Az antibiotikumok alkalmazásának indokoltsága tüneti UDD-ben nem egyértelműen megalapozott. A legújabb tanulmányok azt sugallják, hogy a bélmikrobióta megváltozása (bélbaktériumok túlszaporodása) hozzájárulhat a tünetek kialakulásához a szénhidrátok fermentációján keresztül történő túlzott bélgáztermelés miatt. A szisztematikus hatások elkerülése érdekében a legmegfelelőbb antibiotikumnak a gyengén felszívódó antimikrobás szerek tűnnek, amelyek az enterális kórokozók ellen hatnak, de minimális a szisztematikus toxicitás vagy mellékhatások kockázata. A rifaximint javasolták.
Rifaximin
A rifaximin egy nem szisztematikus rifamicin-analóg, amely széles hatásspektrummal rendelkezik in vitro. A rifaximin csökkentheti a bélflóra metabolikus aktivitását, növelve a széklet tömegét, és felszámolhatja a baktériumok túlszaporodását is. Ez az antibiotikum magas biztonsági és tolerálhatósági profillal rendelkezik.33,38 A rifaximin plazmaszintje minimális, ezért a nem enterális kórokozók nincsenek kitéve szelekciós nyomásnak, és a bakteriális rezisztencia kockázata alacsony.39 Három nyílt és két kettős vak RCT40-44 vizsgálta a rifaximin és rostok ciklikus adagolásának hatékonyságát a tünetek csökkentésében a csak rostokkal összehasonlítva. Egy szisztematikus áttekintés és két metaanalízis elemezte ezeket a vizsgálatokat.44-46 Arra a következtetésre jutottak, hogy a kombinált kezelés hatékony a tünetek enyhítésének elérésében 1 év alatt az UDD-ben szenvedő betegeknél. A csak rosttal kezelt betegek 35%-a tünetmentes volt, szemben a kombinált kezeléssel kezelt csoportok 64%-ával. A tünetek enyhítéséhez szükséges kezelések száma a rifaximin esetében három volt a placebóval szemben, a szövődmények elkerülése érdekében pedig kilenc. Összefoglalva, a legjobb eredményeket az oldható rostok, például a glükomannán és a rifaximin kombinációjával értek el havonta 1 hétig.
C) Probiotikumok
A probiotikumok olyan élő mikroorganizmusok, amelyek helyreállíthatják a komensális bélflórát, amely divertikuláris betegségben a pangás és a csökkent vastagbél tranzitidő miatt megváltozhatott.47 Sajnos kevés adat áll rendelkezésre a tüneti UDD-ben való alkalmazásáról, és a legtöbb vizsgálat kicsi és nem kontrollált. Többségük a tünetek javulását mutatja.48-50
A probiotikumokat 5-aminosaliciláttal (5-ASA) kombinálva is vizsgálták. Tursi és munkatársai három RCT-t végeztek, amelyekben összehasonlították az 5-ASA-t önmagában, a probiotikumot önmagában vagy a kombinált terápiát.51-53 Mind az 5-ASA, mind a probiotikumok hatásosnak tűntek a tüneti UDD megelőzésében, de kombinációjuk jobb volt. Egy nemrégiben ugyanezen tudományos csoport által publikált kettős kötésű RCT arra a következtetésre jutott, hogy mind a ciklikus mezalazin, mind a Lactobacillus casei subsp DG, különösen kombinációban, jobbnak tűnik a placebónál a tüneti UDD remissziójának fenntartásában.54 Összességében azonban a rossz vizsgálati tervek és kis méretük miatt nem lehet végleges következtetéseket levonni.
D) 5-ASA: mezalazin
A mezalazin gyulladáscsökkentő és antioxidáns hatású. Gatta és munkatársai,55 2010-ben publikáltak egy Cochrane szisztematikus áttekintést, amely az 5-ASA szerepét értékelte divertikuláris betegségben szenvedő betegeknél. A szerzők arra a következtetésre jutottak, hogy az 5-ASA hatékony lehet e betegség kezelésében, és hogy a mindennapos mezalazin jobb, mint a ciklikus adagolás a visszaesés megelőzésére. Megfigyeléseik megerősítéséhez magas színvonalú, jól megtervezett RCT-kre van szükség. Az első placebokontrollos, kettős vak vizsgálat ugyanis a mezalazint hatékonynak találta a fájdalomcsillapítás elérésében akut UDD-ben szenvedő betegeknél.56 Két érdekes RCT is van, amely a rifaximinhez képest a tüneti kiújulás megelőzése szempontjából a mezalazin előnyét mutatta, és a Lactobacillus casei probiotikummal összehasonlítva hasonló sikert ért el a hosszú távú remisszió fenntartásában.53,57
E) Antikolinerg / görcsoldó szerek
A vastagbél hipermotilitása divertikulózisban arra utal, hogy az olyan görcsoldó szerek, mint a diciklomin és a hyoscyamin az izomösszehúzódás csökkentése révén javíthatják a tüneteket. De nincs olyan RCT, amely ezt az előnyt megerősítené.
F) Kerülje az NSAID-kezelést
Más kontrollált vizsgálat kimutatta, hogy az NSAID-ok kockázati tényezőt jelentenek a tünetek, az ACD, a perforáció és a vérzés kialakulásában.7,58-60 Az NSAID-használóknál nagyobb a kockázata a tünetes divertikuláris betegség kialakulásának, mint a nem használóknál (RR: 1,5, CI 95%: 1,1-2,1).58 A bonyolult divertikuláris betegségben szenvedő betegeknél pedig nagyobb volt az NSAID-használat a betegség nélküli kontrollokhoz képest. Feltételezték, hogy ez a megnövekedett kockázat a nyálkahártya károsodásának köszönhető, ami a vastagbélnyálkahártya barrierfunkciójának károsodását eredményezi, ami lehetővé teszi a gyulladást kiváltó baktériumok transzlokációját.
G) A D-vitamin szintje
Úgy tűnik, hogy az ACD előfordulása földrajzi és szezonális eltérésekhez kapcsolódik. Emiatt Maguire és munkatársai két érdekes megfigyeléses vizsgálatot végeztek, amelyek kimutatták, hogy az alacsonyabb D-vitamin-szint és az alacsony UV-fényexpozíció (az UV-expozíció meghatározza a D-vitamin-státuszt) az ACD szignifikánsan magasabb kockázatával jár együtt. További jó minőségű vizsgálatokra van szükség az ajánlás megfogalmazása előtt.61,62
A heveny vastagbél-divertikulitis (ACD)
Bár a legtöbb divertikulózisban szenvedő ember tünetmentes marad, becslések szerint körülbelül 10-25%-uknál kialakul egy bal oldali ACD epizód.63 Általában a klinikai diagnózis nem elég pontos, és radiológiai technikák javallottak. Az enyhe tünetekkel (a legtöbb) és bonyolult ACD jelei nélkül rendelkező betegeknél a bal alsó hasi fájdalom, a hányás hiánya és a C-reaktív fehérje >50mg/l kombinációja elegendő lehet a diagnózis felállításához.64,65 Ha képalkotás indikált, valószínűleg a feltételes stratégia, az ultrahanggal mint első vonalbeli technikával, majd a számítógépes tomográfiával (CT), ha az ultrahang nem meggyőző vagy kétséges, a leghatékonyabb megközelítést jelentheti. A CT-vizsgálatok száma 50%-kal csökkenthető. 1978-ban Hinchey és munkatársai javasolták az ACD osztályozását, amelyet később módosítottak.66,67 Az ACD öt stádiumát különbözteti meg; 0. stádium, klinikailag enyhe divertikulitis, I. stádium (a: perikolikus gyulladás és b:
cm-es abcessus az elsődleges gyulladás közelében), II. stádium, intraabdominális, kismedencei vagy retroperitoneális abcessus vagy az elsődleges gyulladástól távoli abcessus, III. stádium, generalizált gennyes peritonitis és IV. stádium, székletperitonitis. Lásd a 3. ábrát.

A heveny vastagbél divertikulitis kezelésének algoritmusa.
A szövődménymentes ACD kezelése (Hinchey-stádium 0 vagy Ia)
A szövődménymentes ACD többsége biztonságosan kezelhető konzervatív módon, 70% és 100% közötti sikeraránnyal.14 A járóbeteg-kezelés jelentős költségmegtakarítást jelenthet az egészségügyi rendszereknek. A szövődménymentes ACD esetében a fekvőbeteg-ellátás kritériumai a jelentős gyulladás (beleértve a láz vagy peritonitis jelenlétét), az orális folyadékok intoleranciája, a 80-85 év feletti életkor, az immunszuppresszió vagy a súlyos társbetegségek. A legtöbb esetben elegendő a rövid kórházi tartózkodás. Nincs bizonyíték arra, hogy az étrendi korlátozások befolyásolták volna a kezelés kimenetelét, bár a legtöbb orvos általában tiszta folyékony étrendet javasol.
A szövődménymentes ACD kezelésében a közelmúlt egyik legnagyobb változása az antibiotikumok használatának csökkenése. Egy nemrégiben készült, kizárólag minőségi megközelítésű (metaanalízis nélküli) Cochrane-áttekintés megállapította, hogy a rendelkezésre álló legjobb adatok nem támasztják alá a rutinszerű alkalmazását.68 Az antibiotikumok nem gyorsítják a gyógyulást, és nem előzik meg a szövődményeket vagy a kiújulást. Ezért az antibiotikumok alkalmazása ebben az esetben megkérdőjelezhető. Valószínűleg az általános fertőzés jeleivel, szepszis vagy bakteriémia jeleivel rendelkező betegeknél, valamint az immunhiányos betegeknél lenne indokolt. Az ajánlott kezelési sémák klinikai konszenzuson alapulnak. Különböző antibiotikumok alkalmazhatók, az ampicilintől a harmadik generációs cefalosporinokig, amennyiben hatásosak a gram-pozitív, gram-negatív és anaerob baktériumok ellen. A ciprofloxacin és metronidazol kombinációja valószínűleg a leggyakrabban felírt orális kezelés. Ha ez a kombináció rosszul tolerálható, az ampicilin-szulfabaktám jó választás lehet. Másrészt a legújabb adatok azt mutatják, hogy az intravénás kezelésnek nincs előnye az orális antibiotikumokkal szemben, illetve a 4 napos intravénás kezelésnek a 7 napos kezeléssel szemben.69-71 Általában a klinikai javulás a kezelést követő 3-4 napon belül megfigyelhető. Végül intravénás antibiotikummal történő kórházi felvétel akkor javasolt, ha a beteg nem képes szájon át táplálékot bevenni, súlyos társbetegségben szenved, vagy ambuláns kezeléssel nem javul.
A bonyolult ACD kezelése (Hinchey Ib-IV. stádium)ACD Hinchey Ib vagy II: tályog
Az ACD-s betegek kb. 15%-ánál alakul ki tályog.67 Nincs jó minőségű bizonyíték a tályogképződéssel járó ACD legoptimálisabb kezeléséről. A kórházi kezelés javallott. A méret fontos meghatározója a sikeres kezelésnek. Kisebb tályogok (
cm) esetén konzervatív kezelés javasolt széles spektrumú antibiotikumokkal. Ez akár 70%-ban sikeres lesz.72 Ha a konzervatív kezelés sikertelen, vagy nagyobb tályogok esetén perkután drénezést kell végezni. Ez akár 80%-ban sikeres.73 A műtét mentőkezelés, ha az előzőekben említett kezelések sikertelenek.ACD Hinchey III vagy IV: gennyes vagy székletszerű peritonitis
A peritonitis a legsúlyosabb szövődmény, 14%-os mortalitással. Bár nincs bizonyíték, a korai műtétet standard terápiának tekintik ezeknél a betegeknél. A műtét megválasztását a beteg körülményei, a műtéti leletek és a sebész tapasztalata befolyásolja. Kritikusan beteg, hemodinamikai instabilitással rendelkező betegeknél a Hartmann-eljárás ajánlott. Hemodinamikailag stabil betegeknél azonban a primer anasztomózist kell előnyben részesíteni proximális széklettereléssel vagy anélkül.14,74
Tradicionálisan a nemzetközi irányelvek az ACD epizódot követő endoszkópia alkalmazását javasolják a vastagbélrák kizárására. Ez az ajánlás kizárólag szakértői véleményeken alapul. A legújabb retrospektív tanulmányok és egy szisztematikus áttekintés75-80 azt mutatják, hogy a rák előfordulási aránya ezeknél a betegeknél meglehetősen alacsony. E legújabb bizonyítékok alapján a leghatékonyabb stratégia az lehet, ha csak azokat a betegeket utalják kolonoszkópiára, akiknél a tünetek tartósan fennállnak, vagy akiknél gyanús CT-leleteket találnak. A határozott ajánláshoz azonban további vizsgálatokra van szükség.
Az ACD epizódot követő kezelésA visszatérő ACD megelőzése
Egy ACD-epizód után körülbelül egyharmaduknak lesz egy második ACD-je, és a második epizód után további egyharmaduknak lesz egy újabb rohama.73,74 Kevés azonban a bizonyíték az ACD-epizódot követő optimális kezelés meghatározására az újabb epizód megelőzése érdekében.
A) Magas rosttartalmú étrend
Az akut epizód megszűnése után általában magas rosttartalmú étrendet javasolnak a kiújulások csökkentése érdekében. Az ACD-ben szenvedő betegek magas rosttartalmú diétájával kapcsolatos RCT-k azonban ellentmondásos eredményeket hoztak. A magas rosttartalmú diéta nemrégiben közzétett szisztematikus áttekintése nem tudott olyan tanulmányt tartalmazni, amely a rostok szerepét vizsgálta volna a visszatérő ACD megelőzésében.26,81 Egyes élelmiszereket (magvak, pattogatott kukorica és diófélék) klasszikusan kerülni kell, mert elméletileg bejutnak, elzárják vagy irritálják a divertikulumot. Strate és munkatársai azonban nagy, prospektív vizsgálatukban nem találtak összefüggést az ACD fokozott kockázatával. Ezért ezeknek az ételeknek az étrendből való kizárása nem javasolt.82 Emellett a testsúlycsökkentés és a dohányzás abbahagyása kedvezően befolyásolhatja az ACD megelőzését.9,83
B) Antibiotikumok
A közelmúltban három szisztematikus áttekintés is értékelte a ciklikus rifaximin szerepét az ACD kiújulásának megelőzésében, de nem mutattak ki egyértelmű előnyöket.46,84,85 Patofiziológiai szempontból a rifaximin kiújulások megelőzésében mutatkozó hatástalanságának plauzibilis magyarázata az lehet, hogy a ciklikus kezelés nem tudja kontrollálni a vastagbél baktériumpopulációját a teljes hónap alatt, mivel a vastagbél baktériumpopulációja a rifaximin szedésének befejezése után 7-14 napon belül regenerálódik. Egy nemrégiben végzett spanyol nyílt RCT azonban kimutatta, hogy a ciklikus rifaximin javíthatja a tüneteket és fenntarthatja a remissziós időszakokat ACD-t követően.86 A rifaximint és rostot kapott betegek 10,4%-ánál fordult elő recidíva, míg a csak rostot kapott betegek 19,3%-ánál. Ezenkívül az először ≥1 év óta diagnosztizált betegeknél nagyobb volt a súlyosbodás kockázata (OR 3,34, 95% CI: 0,01-12,18). További vizsgálatokra van azonban szükség, mivel jelenleg nem lehet ajánlásokat tenni. Nincs bizonyíték arra, hogy más antibiotikumok alkalmazását támogatnák ebben a környezetben.
C) Probiotikumok
Egyes nyílt vizsgálatokban vizsgálták a probiotikumok szerepét az ACD kiújulásának megelőzésében. Giaccari és munkatársai több mint 20 évvel ezelőtt 79 diverticulitis utáni vastagbélszűkületben szenvedő betegnél értékelték a Lactobacillus sp. szerepét a rifaximint követően. A betegek 88%-a 12 hónapig tünetmentes maradt.87 Ez a megfigyeléses vizsgálat volt az első, amely a probiotikumok lehetséges szerepére utalt ebben a helyzetben. Egy újabb vizsgálat a kombinált kezelést értékelte; a balsalazidot és a VSL#3-at (nyolc fajból álló probiotikus keverék). 12 hónap elteltével a kombinált terápiát kapó alanyok 73%-a tünetmentes volt, szemben a probiotikum-monoterápiát kapó 53%-kal (p>0,05).52 Összefoglalva, a probiotikumok hatásosnak tűnnek az ACD kiújulásának megelőzésében, de jól megtervezett vizsgálatok hiányoznak.
D) 5-ASA
Sok kettős vak és nyílt RCT vizsgálta a mezalazin szerepét az ACD kiújulásának megelőzésében. Sajnos a legtöbbjük nem találta a mezalazin előnyét a placebóval szemben a kiújulás megelőzésében.88-90 Raskin és munkatársai nemrég publikáltak két érdekes és azonos fázis 3 kettős vak, placebóval végzett RCT-t (PREVENT1 és PREVENT2), amelyek szintén azt mutatják, hogy a mezalazin nem jobb a placebónál a kiújuló ACD megelőzésében.91 A kombinált kezelést, 5-ASA plusz rifaximin, szintén több vizsgálatban értékelték. Trivedi és Das öt RCT és egy nyílt vizsgálat adatait tekintette át, amelyekben együttesen több mint 600 beteg vett részt, és arra a következtetésre jutott, hogy a kombináció jobbnak tűnik, mint a rifaximin önmagában a visszatérő ACD megelőzésében.92
E) Műtét
Néhány évvel ezelőttig a szövődménymentes ACD két rohama vagy a szövődményes ACD egy rohama után elektív műtétet javasoltak a morbiditás és a mortalitás csökkentése érdekében a kiújulás miatt. Az elektív műtét azonban a morbi-mortalitás megnövekedett kockázatával is jár.93 Emiatt fontos mérlegelni a műtét miatti morbiditást és mortalitást a komplikált kiújulások kockázatával és a tünetek súlyosságával szemben.
A legújabb adatok azt mutatják, hogy az ACD természetes lefolyása sokkal jóindulatúbb, mint korábban gondolták.73,94 A visszaesés hosszú távú kockázata sokkal alacsonyabb, mint korábban hitték, és a későbbi sürgősségi műtét (3-7%), halálozás (95 kimutatta, hogy az első ACD-s esetek 16%-át sürgősen megoperálták, szemben a visszaeső esetek mindössze 6%-ával, és hogy az első epizód 30 napos mortalitása is magasabb volt az ismétlődő eseményekhez képest (3% vs. 0%). Tény, hogy a komplikált ACD-vel jelentkező betegek többségének nincs kórtörténete.96 Azt is javasolták, hogy a visszatérő ACD védelmet nyújthat a perforáció ellen, valószínűleg a gyulladás okozta adhézióképződés miatt.95 Ezért az ACD-t követő elektív műtét politikája nem csökkenti a további műtétek valószínűségét (legfeljebb 3%), és nem véd teljesen a kiújulás ellen. Másrészt a javuló diagnosztika és kezelési módok csökkentették a komplikált ACD morbi-mortalitását. Ezen új adatok miatt az Amerikai Vastagbél- és Végbélsebészek Társasága legújabb iránymutatásában azt ajánlja, hogy az ACD-ből való felépülést követő elektív szigma-rezekciót eseti alapon kell elvégezni14 , és úgy véli, hogy a korábbi epizódok száma nem jó indikátor az elektív műtétre jelöltek kiválasztásában. Az orvosoknak figyelembe kell venniük a beteg egészségi állapotát és életkorát, a roham(ok) gyakoriságát és súlyosságát, valamint az akut epizódot követő tartós tünetek jelenlétét.14
Nagyon nehéz megjósolni, hogy az ACD mely esetei fognak visszaesni. Úgy tűnik, hogy az ACD első epizódjának CT-osztályozott súlyossága a kedvezőtlen természetes lefolyás előrejelzője. A bal oldali ACD, >5 cm érintett vastagbél és a retroperitoneális tályog a kiújulás előrejelzői voltak, és ezeket figyelembe kell venni.97 Nincs konszenzus abban, hogy a fiatal életkor (82 A jelenlegi bizonyítékok szerint az életkor nem tekinthető az elektív műtét indikációjának, mivel úgy tűnik, hogy nincs összefüggésben a betegség súlyos lefolyásával a gyógyszeresen kezelt ACD után. Figyelembe véve azonban, hogy a fiatalabb betegeknél az ACD előfordulása megnövekedett, további vizsgálatokra van szükség e speciális kérdés tisztázására.
Az immunhiányos egyének különleges esetek. Kohorszvizsgálatok szerint ezeknél a betegeknél magas a komplikált, visszatérő ACD kockázata (ötször nagyobb a perforáció kockázata), és magas a sürgősségi műtét kockázata.98 Ezért az elektív műtét alacsonyabb küszöbértéke előnyös lehet számukra.14 Biondo és munkatársai legújabb tanulmányukban azonban azt mutatják, hogy az immunkompromittált betegeknél szignifikánsan magasabb a halálozási arány, de csak az első epizódban. Ezért az ellentmondás jelen van.99
A következmények kezeléseA) Sipoly
A sipoly akkor keletkezik, amikor egy divertikuláris flegma vagy tályog beszakad egy szomszédos szervbe. A sipoly az ACD-ben szenvedő betegek kevesebb mint 5%-ánál jelenik meg. A leggyakoribbak a colovesicalis és a colovaginalis sipolyok. Feltehetően a legtöbb betegnél egylépcsős műtéti reszekciót lehet végezni fisztulazárással és primer anasztomózissal. Egyéb sipolyok, mint a coloentericus vagy coluterinus, ritkák.100,101
B) Obstrukció
Az ACD ismétlődő epizódjai, amelyek lehetnek szubklinikaiak, a vastagbél krónikus szűkületét eredményezhetik folyamatos gyulladás nélkül. Magas fokú vagy teljes elzáródás léphet fel. Az obstrukció kezelése előtt először ki kell zárni a rosszindulatú etiológiát. Ha a daganatot kellőképpen kizárták, és nincs ACD, az endoszkópos tágítás vagy az ideiglenes dekompresszió fémstenttel terápiás lehetőség lehet.102 Később egy későbbi egylépcsős rezekció diverzió nélkül megvalósítható.
A divertikulózissal járó szegmentális vastagbélgyulladás kezelése
Ezt úgy definiálják, mint egy érintett vastagbélszegmens interdivertikuláris nyálkahártyájának krónikus gyulladása. A végbél és a jobb vastagbél megkímélt. Külön klinikai és patológiai rendellenességgé vált, és gyakran véres széklettel jár. A patogenezis ismeretlen. A szövettani elváltozások spektruma az enyhe, nem specifikus gyulladástól a gyulladásos bélbetegséghez hasonló elváltozásokig terjed. Emiatt a differenciáldiagnózis gyakran nehéz. A legtöbb beteg néhány hét vagy hónap alatt teljesen meggyógyul. Néhányukat kezdetben szájon át szedhető 5-ASA-val kezelik, de valószínűleg ezekre a gyógyszerekre nincs szükség, mert a legtöbb eset spontán megszűnik.103
Következtetések
A tüneti UDD-ben a kezelés célja a szövődmények megelőzése és a tünetek csökkentése. A jelenlegi bizonyítékok szerint a rost plusz ciklikus rifaximin vagy a mezalazin plusz probiotikumok tűnik a leghatékonyabb terápiának. Az ACD-ben úgy tűnik, hogy az antibiotikumok továbbra is a kezelés fő támasza maradnak, és a szövődménymentes ACD-ben szenvedő betegek túlnyomó többségénél az ambuláns kezelés tekinthető optimális megközelítésnek. Komplikált ACD esetén azonban fekvőbeteg-kezelésre és intravénás antibiotikumokra van szükség. Jelenleg a sürgősségi sebészet szerepe változóban van. A diverticulitishez társuló tályogok többsége intravénás antibiotikummal és/vagy perkután drénezéssel kezelhető, és a sürgősségi műtét csak a peritonitisben szenvedő betegek esetében tekinthető standard kezelésnek. Végül, az ACD-ből való felépülést követő elektív műtétet eseti alapon kell elvégezni.
A szerzők hozzájárulása
Gargallo CJ, Sopeña F és Lanas A egyformán hozzájárultak a tanulmány tervezéséhez, szerkesztéséhez és átdolgozásához.
Érdekütközés
Dr. Carla J. Gargallo és Dr. Federico Sopeña nem jelentenek érdekellentétet. Dr. Angel Lanas az AlfaWasserman tanácsadója volt.
