子宮循環はエストロゲン刺激に絶妙に敏感で、他のどの刺激に対しても、身体のどの器官よりも高い血管拡張を示す。2 卵巣周期中、エストロゲン分泌とプロゲステロンの調節効果を反映して、繰り返し血流パターンが発生する。 これらの周期的パターンは、ウシ、母豚、雌羊のような排卵前期が短い動物で最も劇的に示され、図1にエストロゲンとプロゲステロンの末梢レベルとともに示されている3、4、5。これらの種における受胎後、母体と胎児の組織が17日から28日後に相互接続されるまでUBFパターンは非妊娠動物のものと同様で、その後、確定的かつ進行性のUBF増加が見られ、正規妊娠まで継続する。 胎児の絨毛膜による子宮内膜の侵食は、霊長類では受胎後かなり早い時期に起こるため、これらの種ではUBFが早期に増加すると推定するのが妥当であるが、そのような反応はこれまで観察されたことはない。 図2に、ヒツジ妊娠期間中の総紫外線量、子宮とその内容物の単位重量あたりの紫外線量、胎盤に供給される紫外線量の割合、および胎児の体重の全体的なパターンを示す。 妊娠17日から70日の間が、UBFとPBFの最も急速な変化と関連しており、この種では最終的な胎盤形成の時期に相当する。 胎盤の成熟に伴い、胎盤に供給されるUBFの割合とPBFの絶対量は増加するが、その速度は胎児の成長とほぼ同じである。 この同じ時期に、1ml の血液から抽出される酸素の量は一定であり、したがって妊娠中の子宮の所定重量あたりに供給される酸素の量も一定である6 。女性における相関的な研究は、妊娠 10 週から 40 週まで同様の恒常性パターンと同様の酸素消費(約 10ml/kg)7 を示す。女性は雌牛よりも低い UBF 率で同量の酸素を供給するので(~150 ml/kg 対 ~270ml/kg)、この点で 人間の胎盤がより効率が良いことが理解できる。 したがって、同程度の体重の胎児であれば、より少ない絶対的なUBFが必要となり、心臓に対する妊娠の負荷は減少する」
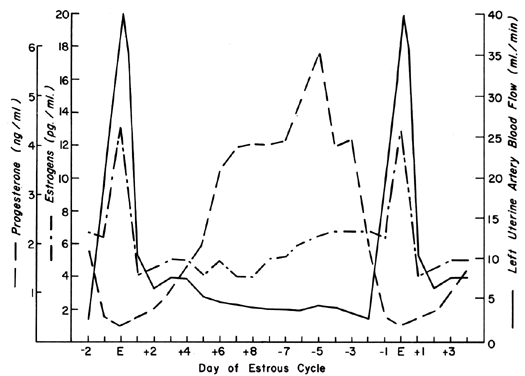 Fig. (Greiss FC, Jr, Anderson SG: Am J Obstet Gynecol 103:629, 1969; Yuthasastrakosol P et al: J Reprod Fertil 43:57, 1975から引用)
Fig. (Greiss FC, Jr, Anderson SG: Am J Obstet Gynecol 103:629, 1969; Yuthasastrakosol P et al: J Reprod Fertil 43:57, 1975から引用)
 図2.子宮血流波形(エストロゲンおよびプロゲステロンの報告血清レベルと示す。 251>
図2.子宮血流波形(エストロゲンおよびプロゲステロンの報告血清レベルと示す。 251>
PBFの変化は、妊娠の経過を通じて胎盤に供給する血管の血管拡張が常に増加することによって達成される。 しかし、第二期および第三期の間の任意の瞬間には、これらの血管のそれ以上の急性血管拡張は本質的に起こり得ない。 したがって、PBFが低下したときに一定の酸素供給量を維持するためには、酸素抽出量を増やさなければならない(Fig.3)。 報告されたデータによると、酸素抽出量の増加の限界は2倍であるように思われる。 したがって、酸素供給が低下する前にPBFが50%以上低下しなければならない。 これらの考察は、流量減少前の恒常的なPBFの速度が最適であったと仮定している。 しかし、毒素血症のように亜急性に、あるいは腎症のように慢性に、恒常的なレベルが最適でなくなることがあることもわかっている。 このような場合、安全係数、すなわち酸素供給が損なわれる前にPBFを低下させることができる割合が低くなる。
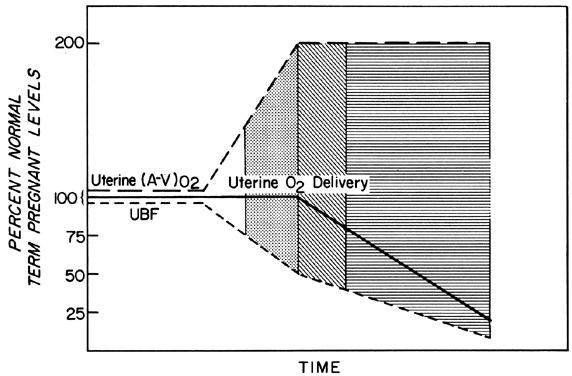 Fig.3. 子宮動静脈酸素抽出量(A-V)02の変化-ヒツジ妊娠の後半における子宮血流の減少に応答して。 (A-V)02を2倍にすることができるので、子宮血流が50%以上減少するまで子宮の酸素供給は恒常的なレベルに維持される。 透明、点線、線形の領域は、最適胎盤血流の関数として定義した場合の胎児予備能の仮想的な程度を示し、以降の図で同様のレベルの胎児予備能を示すために使用されている。 (Huckabee WE, Metcalfe J, Prystowsky H et al: Blood flow and oxygen consumption of the pregnant uterus.から引用した。 Physiol 200:274, 1961.)
Fig.3. 子宮動静脈酸素抽出量(A-V)02の変化-ヒツジ妊娠の後半における子宮血流の減少に応答して。 (A-V)02を2倍にすることができるので、子宮血流が50%以上減少するまで子宮の酸素供給は恒常的なレベルに維持される。 透明、点線、線形の領域は、最適胎盤血流の関数として定義した場合の胎児予備能の仮想的な程度を示し、以降の図で同様のレベルの胎児予備能を示すために使用されている。 (Huckabee WE, Metcalfe J, Prystowsky H et al: Blood flow and oxygen consumption of the pregnant uterus.から引用した。 Physiol 200:274, 1961.)
*人間およびヒト以下の霊長類では、絨毛間隙に供給することになる螺旋動静脈(胎盤子葉につき約1本)が毛細管接続を失い、栄養細胞による血管壁の置換の結果として約10倍に拡張されます。 この過程は、子宮筋層接合部以下にまで及び、螺旋細動脈を文字通り螺旋動脈に変えてしまうこともある。
ヒツジ種では、非妊娠時にカルンクルと呼ばれる子宮内膜の複数の離散的な領域が存在する。 妊娠中は、これらのcaruncleで胎児と母体の組織の相互結合が起こり、拡大して個々の胎盤子葉となる。 これらの部位に流れる血液は、まとめてPBFを構成している。 子葉動脈血管は著しく拡張するが、絨毛膜要素は含まず、母体-胎児間の移動は毛細血管-毛細管界面によるもので、絨毛間隙は存在しない。
子宮循環の動的反応
非妊娠時の子宮の血管は、エストロゲン刺激に対する独特の反応性、局所麻酔薬に対する反応、およびおそらくプロスタグランジンに対する反応を除いて、他の筋肉臓器の血管と同様の反応を示す(Table 1)。 妊娠中、胎盤に供給する血管は徐々に拡張し、最小限の、あるいはそれ以上の急拡大が起こりえない状態になる。24 したがって、非妊娠時の子宮で血管拡張を誘発する刺激は、確定的な胎盤形成が起こった後は効果がない。 しかしながら、胎盤の血管は非妊娠時と同様に血管収縮能力を保持している。 PBF は妊娠末期の全紫外線量の 80% から 90% を占めるので、子宮の全血管反応は胎盤血管の反応と同じように見える。 この点はしばしば誤解され、非胎盤血管の反応は妊娠の有無にかかわらず同じであることを忘れてはならない
TABLE 1. 非妊娠時の子宮血管の反応*
|
血管収縮 |
血管拡張 |
|
α-」。アドレナリン刺激 |
β- アドレナリン刺激 |
|
(ドーパミンのこと。 エピネフリン |
(イソプロテレノール、エピネフリン)8,9,16 |
|
ノルエピネフリン)8,9.10 |
アセチルコリン・副交感神経刺激薬23 |
|
交感神経刺激薬 剤11 |
アデノシン類17 |
|
(血管拡張剤) |
ブラディキニン17,18 |
|
低酸素症(重症)12 |
シアン化物19 |
|
局所麻酔薬 |
高窒素物質 |
|
(動脈内投与)13.高窒素物質(低酸素症)15 |
|
|
(動脈内投与)16 |
(遅効性だが延長される)2 |
|
ニコチン |
グルコサミン |
|
(αアドレナリンの仲介)15 |
(? 浸透圧効果)21 |
|
虚血19 |
|
|
Vasoactive intestinal polypeptide20 |
* 胎盤への供給血管の著しい拡張と子宮血流が優位に分布するので胎盤への反応は消されている。 したがって,妊娠中の血管拡張刺激の効果については,議論の余地がある。
ヒト胎盤の血流構造は、他の血管床の血流を通常制御するものにユニークな要因を追加している。 すなわち、血液は螺旋動脈を横断して沼のような絨毛間空間に入り、胎児の絨毛を灌流し、そして基底板の多くの集合静脈によって一般の循環に戻る。 事実上、血液は通常の血管経路を離れ、妊娠期間中、子宮に移植された新しい血管外空間を循環しているのである。 絨毛膜間スペースは子宮腔内にあり、胎盤は柔軟な構造であるため、子宮筋層の収縮によって生じる圧力は羊膜腔と絨毛膜間スペースに等しく伝達されることになる。 このように、子宮筋活動という通常の血管制御とは無関係な要因が、灌流圧への影響により、間質圧を変化させ、PBFに影響を与える可能性があるのである。 胎盤以外の組織と単一の子葉への血流を、それぞれの制御に関連する公式とともに図4に示す。 これらの式は、オームの法則をこれらの個々の心血管系の状況に適用したものに過ぎないことに注意すべきである
。 霊長類の子宮の非胎盤循環と胎盤循環、それぞれに影響する因子。 これらの因子と分布血流の関係は添付の式で定義されている。 UABP:子宮動脈血圧、UVBP:子宮静脈血圧、Re:外部血管抵抗、RiN-PLおよびRiPL:それぞれ非胎盤および胎盤の細動脈の反応性による内部血管抵抗。(Greiss FC, Jr: MCV/Q, 8:52, 1972より)
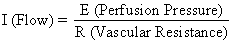
胎盤以外の組織に血液を送る灌流圧は、子宮動脈圧と静脈血圧の差であり、胎盤の動脈圧と静脈血圧の差は胎盤の動脈圧と静脈血流の差である。 しかし、絨毛間隙に血液を送る灌流圧は、子宮動脈血圧と絨毛間隙圧の差である。 後者は羊水膜圧(IUP)で最も近似される。 筋肉質な器官では、抵抗因子として血管平滑筋の反応による抵抗、すなわち固有抵抗(Ri)と、収縮した子宮筋層を横切る際に血管に与えられる圧迫、すなわち外来抵抗(Re)がある。 子宮収縮は、Reの増加と胎盤灌流圧の減少という2つのメカニズムによってPBFに影響を与えることが明らかになるはずである
臨床では、胎盤血管制御の3つの主要な特性が重要である。 これらは、灌流圧と流量の関係、血管作動性刺激に対するらせん動脈の反応、そして子宮筋収縮の効果である。
圧力-流量関係
心房静止中の灌流圧の低下に伴うUBFの変化を観察すると、傾き1の直線関係が成り立つ(Fig. 5). これは胎盤血管が広く拡張していることを反映しており、PBFは灌流圧の低下とほぼ同じ割合で減少することを示している。 子宮静脈圧はほとんどの状況下で極めて一定であるため、全身血圧(MBP)の変化を用いて、PBFの変化を近似的に表すことができる。 すなわち、平均動脈圧が25%低下すると、PBFは25%低下すると予想される。 しかし、大動脈に対する妊娠中の子宮の圧力だけで、骨盤内の血圧が上腕動脈で観察されるよりも低下することが示されているため、このような測定は側臥位で行うべきである
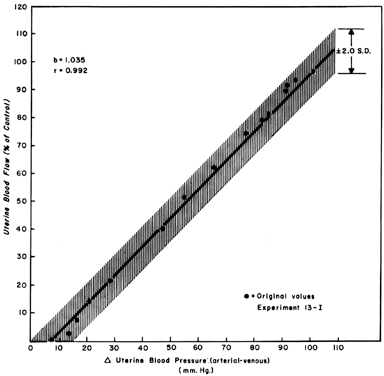 Figure 5. 期妊娠雌牛のプールされた比例データから決定された圧力-流量回帰線。 この関係は直線的なので、子宮血流は灌流圧の変化に比例して変化する(Greiss FC, Jr: Am J Obstet Gynecol 96:41, 1966より)
Figure 5. 期妊娠雌牛のプールされた比例データから決定された圧力-流量回帰線。 この関係は直線的なので、子宮血流は灌流圧の変化に比例して変化する(Greiss FC, Jr: Am J Obstet Gynecol 96:41, 1966より)
血管活性刺激に対する反応
らせん動脈は静止状態で最大拡張に近づいているので、血管拡張薬または刺激には、その薬の受容体が存在してもほとんど効果がない。 しかし、これらの血管の平滑筋は、他の多くの末梢血管床よりも血管収縮剤や刺激に対して絶妙に敏感である(図6)。 このことは、MPBがフェニレフリンなどの末梢で作用する血管収縮剤の刺激に反応して増加しても、それに比例して胎盤血管抵抗(Ri)の増加は非常に大きく、正味の効果はPBFの著しい減少であることを意味します。 このような血管収縮剤に対する感受性の違いは、血管拡張薬の適応となるたびに考慮しなければならない。 エフェドリンのような中枢に作用する薬物を使用すると、胎盤の血管収縮を少量引き起こすものの、PBFの絶対的な増加を伴うMBPの改善が比例して大きくなるであろう。 レバルトレノール(ノルエピネフリン)とエピネフリンを静脈内投与したときの母体血圧、心拍出量、子宮血流に対する影響を示すオリジナル記録。 全身および子宮コンダクタンス(抵抗の逆数)のコントロールレベルからの比例した変化を括弧内に挿入した。 子宮コンダクタンスの減少(抵抗の増加)は、他の薬剤による全身コンダクタンスの減少を上回ることに注意されたい。 (Greiss FC, Jr: Obstet Gynecol 21:295, 1963より. Courtesy of Harper & Row, Publishers.)
子宮筋収縮
上で述べた二つのメカニズム、Reの増加と灌流圧の減少によって作用し、子宮筋収縮はそれぞれの収縮強度および持続時間に直接比例して、PBFを減少させる。 この関係は非常に精密で、子宮内圧のトレースはPBFのほぼ正確な逆像となる(図7)。 収縮の頻度を上げると、子宮筋収縮期(PBFが恒常的なレベルにある時間)の持続時間が短くなり、一定時間中のPBFが減少する。 さらに、胎盤剥離のように収縮間トヌスが上昇すると、収縮間PBFはそれに比例して減少する。 霊長類と女性におけるラジオアンギオグラフィーの研究では、平均的な強さの子宮筋収縮の頂点にあるとき、PBFは停止することが示されている25。したがって、子宮収縮の頻度と強度が増すにつれて、一定期間ごとに胎児絨毛に灌流するPBFの平均量は徐々に減少するので、分娩は本来胎児にとってストレスとなることが明らかだ
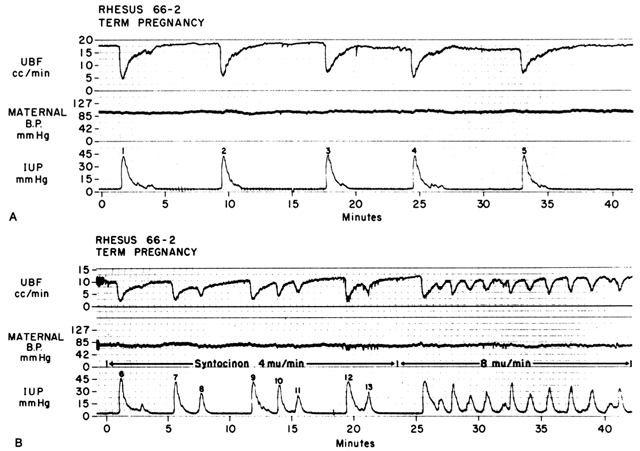 Figure 7. A.アカゲザルの自然分娩時の子宮血流(UBF)と子宮収縮の関係。 逆像関係,収縮開始時にUBFが急激に減少すること,UBFが基礎値からゆっくり回復することに注目。 UBFが基底レベルを回復したのは、「正常」トーヌス時のみである。 B. Aに示した自然分娩のオキシトシン刺激によるUBFに対する収縮回数の増加の影響。正常なトーヌスの相の持続時間が減少していることに注意する。 収縮と収縮の間に到達するUBF速度は、先行する収縮の強度と正常な緊張状態の相の持続時間に依存する。 7回目および12回目の収縮の後、流れの回復は不完全であったが、これは後続の収縮が正常なトーヌス相を伴わずに起こったためである。 (Creiss FC Jr, Anderson SG: Clin Obstet Gynecol 11:96, 1968. Courtesy of Harper & Row, Publishers.)
Figure 7. A.アカゲザルの自然分娩時の子宮血流(UBF)と子宮収縮の関係。 逆像関係,収縮開始時にUBFが急激に減少すること,UBFが基礎値からゆっくり回復することに注目。 UBFが基底レベルを回復したのは、「正常」トーヌス時のみである。 B. Aに示した自然分娩のオキシトシン刺激によるUBFに対する収縮回数の増加の影響。正常なトーヌスの相の持続時間が減少していることに注意する。 収縮と収縮の間に到達するUBF速度は、先行する収縮の強度と正常な緊張状態の相の持続時間に依存する。 7回目および12回目の収縮の後、流れの回復は不完全であったが、これは後続の収縮が正常なトーヌス相を伴わずに起こったためである。 (Creiss FC Jr, Anderson SG: Clin Obstet Gynecol 11:96, 1968. Courtesy of Harper & Row, Publishers.)
局所麻酔薬
これらの薬は、誤って血管内に注入された後のように血管床に直接効果を及ぼすことも、通常の血管緊張を維持する自律神経が麻痺する結果として間接的にも作用することもある。 ほとんどの臓器では、血管内注射は血管抵抗に大きな影響を与えない。 しかし、子宮や胎盤の血管は、このような刺激に対して有意な血管収縮を起こす。 さらに、子宮筋層はこのような薬物によって様々な刺激を受ける(Fig.8)。 単独でまたは一緒になって、これらの反応はPBFを減少させる。 分娩中に行われる子宮頸管傍ブロック麻酔の後、遅発性胎児徐脈が起こることがある。 この胎児反応を説明する最良の仮説は、局所麻酔薬が子宮動脈の近くに注射され、その優れた浸透性のために動脈壁を越えて子宮に作用し、PBFを低下させ、胎児の低酸素を引き起こすというものである
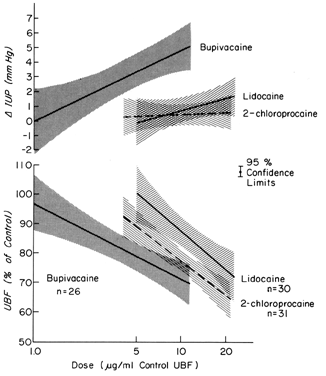 Fig. 8. 子宮動脈に直接投与された局所麻酔薬の子宮血管コンダクタンスと子宮内圧に対するヒツジ妊娠中の用量反応関係。 有効量レベルは、子宮頸部傍ブロック麻酔後の徐脈時に胎児に観察される範囲内である(Fishburne JI, Jr et al: Responses of the gravid uterine vasculature to arterial levels of local anesthetic agents.から)。 Am J Obstet Gynecol 133:753, 1979. 提供:The C. V. Mosby Company.)
Fig. 8. 子宮動脈に直接投与された局所麻酔薬の子宮血管コンダクタンスと子宮内圧に対するヒツジ妊娠中の用量反応関係。 有効量レベルは、子宮頸部傍ブロック麻酔後の徐脈時に胎児に観察される範囲内である(Fishburne JI, Jr et al: Responses of the gravid uterine vasculature to arterial levels of local anesthetic agents.から)。 Am J Obstet Gynecol 133:753, 1979. 提供:The C. V. Mosby Company.)
