Geachte redacteur:
Peritonitis is de belangrijkste oorzaak van het verlies van een peritoneale dialysekatheter (PD) en de belangrijkste reden waarom patiënten overschakelen van PD naar hemodialyse1. Het veroorzaakt de dood bij 6% van de patiënten, vooral wanneer het wordt veroorzaakt door Staphylococcus aureus, enterische organismen en schimmels2.
Prompt starten met antibiotica is van cruciaal belang en deze moeten worden gestart zodra een troebele effluent wordt gezien, zelfs zonder bevestiging van het celtal door het laboratorium3. Richtlijnen bevelen empirische behandeling aan met een combinatie van vancomycine of een cefalosporine met aminoglycoside of cefalosporine van de derde generatie3.
Chemische peritonitis, beschreven als peritoneale ontsteking veroorzaakt door een niet-infectieus agens (zoals antibiotica en dialyseoplossingen) is een zeldzamere aandoening.
Chemische peritonitis geïnduceerd door vancomycine werd voor het eerst beschreven in 19864 en bijna 90 gelijkaardige gevallen werden gemeld in het 80-90ste decennium5,6. Sindsdien werd geen enkel ander geval meer vastgesteld.
Icodextrinegeïnduceerde peritonitis werd voor het eerst beschreven in 19997, maar de prevalentie ervan is niet duidelijk. In 2002 deed zich in Europa een epidemische uitbraak voor die verband hield met de verontreiniging van oplossingen8. Er werden weinig gevallen gemeld na verbetering van het productieproces, die allemaal verband hielden met “sensibilisatie” in die periode of met andere contaminaties8.
Wij meldden een geval van chemische peritonitis bij een patiënt die werd behandeld met icodextrine en intraperitoneale vancomycine, waarbij vancomycine de beledigende stof lijkt te zijn.
Een 34-jarige man, met nierfalen secundair aan diabetische nefropathie, was sinds 2006 in PD. Icodextrine werd een jaar na het begin van de PD toegediend. In de daaropvolgende jaren werden geen peritonitis-episoden vastgesteld.
In 2009 kwam hij naar het ziekenhuis met milde buikpijn met een evolutie van vier uur. Hij had geen andere symptomen, exit-site had geen inflammatoire tekenen en effluent was helder. Analyse van de effluent toonde 26 cellen/µl (tabel 1), abdominale radiografie en echografie waren normaal.
Intraperitoneale vancomycine (2 g elke 5 dagen) en ceftazidime (1 g elke dag) werden toegediend en patiënt werd ontslagen, met behoud van icodextrine.
De volgende dag kwam hij terug met troebele effluent (tabel 1). Dezelfde behandeling werd gehandhaafd en troebele effluent verdween in de twee volgende dagen.
Op de 5e dag, was hij asymptomatisch en kwam voor de tweede vancomycine toediening. Later op die dag verschenen buikpijn en troebele effluent opnieuw (tabel 1).
PD werd opgeschort en hemodialyse werd gestart. Vancomycine en ceftazidime werden overgeschakeld op intraveneuze route en een extra dagelijkse dosis intraperitoneale ceftazidime (500 mg) werd gehandhaafd. Hij werd asymptomatisch en troebele effluent verdween in de volgende twee dagen. Alle kweken, inclusief schimmel en Mycobacterium tuberculosis waren steriel.
Op de 9e dag nam hij de PD weer op (met icodextrine) en op de 10e dag werd intraperitoneaal vancomycine toegediend. Troebele effluent verscheen opnieuw na toediening van vancomycine. Op de 12e dag was hij asymptomatisch en ontkrampt (tabel 1).
Drie maanden later is hij nog steeds asymptomatisch, met behouden ultrafiltratie en schone effluent.
Patiënten met peritonitis presenteren zich meestal met troebele vloeistof en buikpijn. Leukocyten in het effluent hoger dan 100/ml (met 50% polymophonucleaire cellen) wijzen op de aanwezigheid van ontsteking, waarbij infectieuze peritonitis de meest waarschijnlijke oorzaak is3. Bij een korte verblijfsduur is het echter mogelijk dat de leukocyten de 100/ml niet bereiken3 en dat de peritonitis zich presenteert met buikpijn en zonder troebele effluent3.
In onze patiënt werden andere oorzaken van buikpijn, zoals gastro-enteritis, pancreatitis, appendicitis of pneumoperitoneum uitgesloten en werd een empirische behandeling voor infectieuze peritonitis gestart. De troebele effluent die de volgende dag aanwezig was, werd verondersteld een late uiting te zijn van peritonitis in vloeistof met een langere verblijftijd.
De buikpijn en troebele effluent verschenen opnieuw na de tweede toediening van vancomycine en hij werd opgenomen met verdenking op refractaire peritonitis. Als de verdenking werd bevestigd, zou de peritoneale katheter moeten worden verwijderd en zou de patiënt moeten worden overgeschakeld op hemodialyse9. Hij vertoonde echter niet de typische evolutie van een refractaire infectieuze peritonitis en andere oorzaken van troebele effluent, zoals hemoperitoneum, maligniteit, eosinofiele en chylous effluent werden uitgesloten10. Chemische peritonitis gerelateerd aan icodextrine of vancomycine bleef een plausibele diagnose5,6.
Icodextrine geïnduceerde peritonitis lijkt te worden veroorzaakt door besmetting van de oplossing met peptidoglycanen die vrijkomen uit bacteriën (Alicylobacillus acidocaldarius) tijdens het fabricageproces8. Door verbetering van het proces daalde de frequentie van een piek van 0,912% in 2002 tot 0,013% in 20038.
Patiënten presenteren zich met milde buikpijn en troebele effluent, zonder rebound, koorts of huiduitslag11,12. Effluent leukocyten varieert van 100 tot 6.000/µl11,13, met mononucleaire overheersing11. De kweek is altijd steriel11.
De tijdspanne tussen het begin van de icodextrine en de eerste symptomen varieert van enkele uren tot verscheidene jaren7,12. Het klinisch beloop is golvend, met intermitterende pijn en troebelheid van het dialysaat na elke icodextrine inname, zonder reactie op antibiotica12. Stopzetting van de icodextrine leidt tot verlichting van de symptomen en normalisering van de leukocyten binnen 24-48 uur, maar terugval wordt steevast geïnduceerd na rechallenge12.
Bij onze patiënt werd geen temporele relatie met de icodextrine toediening vastgesteld, noch werd terugval na rechallenge opgemerkt.
Een temporele relatie met de vancomycinetoediening ondersteunde de diagnose van door vancomycine geïnduceerde chemische peritonitis.
De klinische presentatie varieert van alleen troebele effluent tot ernstige buikpijn en koorts. Het begint 2-12 uur na vancomycine toediening5 en verdwijnt binnen 3 tot 4 dagen na suspensie6. Er is een overwicht aan neutrofielen, met eosinofielen variërend van 0-10%5,6.
De gerapporteerde incidentie van vancomicyn (Vancoled®)-geïnduceerde peritonitis was 23%6. Het onderliggende mechanisme is onbekend5,14. Sommige patiënten ervaren een herhaling van buikpijn en/of effluente leukocytenstijgingen bij hernieuwde blootstelling aan intraperitoneale vancomycine, zonder klachten wanneer intraveneuze of intraperitoneale vancomycine van een ander merk van de fabrikant wordt toegediend5. Deze resultaten ondersteunen het vermoeden dat de ontsteking niet volledig te wijten is aan vancomycine zelf, maar aan een ander bestanddeel van het preparaat14,15.
Vancomycine bevat 5,2-16,7% onzuiverheden, afhankelijk van zowel het merk als het lot van het preparaat14,15. De variërende hoeveelheid onzuiverheden die in afzonderlijke partijen aanwezig is, kan bepalen of er een ontstekingsreactie optreedt6.
Er zijn geen sterfgevallen gemeld6,7 en er wordt geen behandeling aanbevolen, behalve het schorsen van het product in kwestie7.
Hoewel het klinisch goedaardig is met spontane oplossing, zijn de gevolgen op lange termijn nog steeds onbekend. Bovendien kan het worden verward met infectieuze peritonitis en leiden tot het onnodig voorschrijven van antibiotica of tot katheterverwijdering en PD-suspensie7.
In de afgelopen 15 jaar werd geen enkel geval van vancomycine-geïnduceerde peritonitis gemeld, misschien als gevolg van de geleidelijke verbetering van de zuiveringen. In een tijd waarin generische preparaten steeds meer worden gebruikt, kan ons geval artsen waarschuwen voor de aanwezigheid van deze vergeten bijwerking.
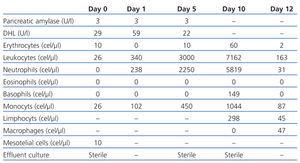
Tabel 1. Evolutie van de kenmerken van effluenten
