INLEIDING
Basis- en klinisch onderzoek van de afgelopen jaren heeft een direct, tweerichtingsverband aangetoond tussen chronische nierziekte en hart- en vaatziekten.1,2 In de dagelijkse klinische praktijk worden serumcreatinineconcentraties en de glomerulaire filtratiesnelheid, geschat met de Cockcroft-Gault3 -formule of de Modification of Diet in Renal Disease (MDRD)4 -vergelijking, vaak gebruikt om de nierfunctie te schatten. Plasma creatinine concentraties kunnen echter worden beïnvloed door een aantal factoren, zoals leeftijd, geslacht, spiermassa, lichamelijke activiteit, dieet en medicatie.5
Cystatine C is een eiwitremmer van cysteïne protease die door alle gekernende cellen in een stabiel tempo wordt gesynthetiseerd. Door zijn lage molecuulgewicht en hoge iso-elektrisch punt kan het bijna uitsluitend door glomerulaire filtratie worden geëlimineerd. Cystatine C-concentraties worden niet beïnvloed door leeftijd, geslacht of eiwitinname, en zijn gevoelig voor kleine veranderingen in glomerulaire filtratie. Vanwege deze kenmerken wordt de plasmacystatine C-concentratie beschouwd als een van de beste markers voor de glomerulaire filtratiestatus.6-9 Recentelijk is in verschillende onderzoeken een verband aangetoond tussen verhoogde cystatine C-waarden en de ontwikkeling van cardiovasculaire complicaties bij patiënten met coronaire aandoeningen. Het is momenteel niet bekend of dit verband te wijten is aan het feit dat cystatine C een betere marker van de nierfunctie is dan serumcreatinine, of dat er naast glomerulaire filtratie nog andere factoren zijn die de concentratie van dit eiwit beïnvloeden en die bovendien verband houden met cardiovasculaire risico’s.10
Het doel van deze studie was om de prognostische waarde van de plasma cystatine C-concentratie te beoordelen bij patiënten die waren opgenomen in het ziekenhuis voor een acuut coronair syndroom (ACS) met een hoog risico, en om de relatie tussen cystatine C en andere markers van nierfunctie en ontsteking te onderzoeken.
METHODEN
Dit is een prospectieve, observationele studie uitgevoerd tussen mei 2006 en juli 2007. Een totaal van 203 patiënten ouder dan 18 jaar en opeenvolgend opgenomen in de cardiale intensive care unit (ICU) van ons centrum met een diagnose van hoog-risico ACS werden geïncludeerd.
De diagnostische criteria voor hoog-risico ACS omvatten ten minste 2 van de volgende factoren: pijn met ischemische kenmerken, elektrocardiografische veranderingen die consistent zijn met ischemie, en/of verhoogde myocardiale necrose markers. De behandeling en de aanvullende onderzoeken die tijdens het verblijf van de patiënt in het ziekenhuis werden uitgevoerd, waren gebaseerd op de klinische beslissingen van de behandelend arts. Bij de meeste patiënten werd een invasieve strategie gebruikt, met urgente coronaire angiografie (voor myocardinfarct met ST-segmentstijging of linkerbundeltakblok) of vroeg geplande coronaire angiografie tijdens de eerste 24 tot 72 uur na ziekenhuisopname.
Clinische kenmerken
De volgende gegevens werden geregistreerd uit de klinische dossiers van de patiënten: demografische informatie, aanwezigheid van klassieke cardiovasculaire risicofactoren (diabetes mellitus, systemische hypertensie, dyslipidemie, en roken), en voorgeschiedenis van bekende vaatziekten (ischemische hartziekte, cerebrovasculaire ziekte, perifere arteriële ziekte, en voorafgaande myocardiale revascularisatiebehandeling). De andere geanalyseerde klinische variabelen omvatten het type ACS, Killip-klasse ten tijde van de ziekenhuisopname, systolische en diastolische drukwaarden, polsdruk (geschat als het verschil tussen systolische en diastolische slagaderlijke druk), en hartslag.
Alle patiënten ondergingen echocardiografie, waarbij de linker ventrikel ejectiefractie werd geschat met de Simpson methode met behulp van een 4-kamer benadering; het gemiddelde van 3 bepalingen werd berekend bij patiënten met sinusritme, en het gemiddelde van 5 bepalingen bij degenen met atriumfibrilleren.
Bij 95% van de patiënten werd coronaire angiografie verricht, en de ernst van de coronaire laesies werd geëvalueerd met een score op basis van het aantal aangetaste epicardiale coronaire arteriën.
Analytische gegevens
Baseline hemoglobine, hematocriet, leukocyten, glucose, en creatinine waarden werden geregistreerd in de eerste laboratoriumanalyses uitgevoerd in ons centrum op het moment van ziekenhuisopname. Concentraties van totaal cholesterol, hoge-densiteit lipoproteïne cholesterol (HDL-C), lage-densiteit lipoproteïne cholesterol (LDL-C), glucose, hoog-gevoelig C-reactief proteïne, en cystatine C werden geregistreerd in de eerste 24 uur, samen met de piek troponine I (TpI) niveau.
Cystatine C werd gemeten met een geautomatiseerde homogene immunoassay met behulp van een Dade-Behring BN ProSpec nefelometer. Het reagens voor de analyse bestond uit polystyreen deeltjes gecoat met antilichamen tegen het eiwit die agglutineren wanneer gemengd met monsters die cystatine C bevatten en licht dispergeren met een intensiteit die evenredig is met de concentratie van de analyt.
Het referentie-interval voor de serumcystatine C-concentratie bij volwassenen met de gebruikte nefelometrische methode is 0,51 tot 0,95 mg/L. De concentraties van hooggevoelig C-reactief proteïne werden ook bepaald door middel van immunoassay. De glomerulaire filtratiesnelheid werd geschat met de MDRD-vergelijking.
Geanalyseerde episodes
De cardiovasculaire complicaties die werden geanalyseerd, omvatten sterfte in het ziekenhuis, sterfte door alle oorzaken tijdens de follow-up, ontwikkeling van een nieuw myocardinfarct, gedefinieerd als pijn op de borst of gelijkwaardige anginale pijn met ECG-veranderingen, of verhoogde tumornecrose-markers tijdens de eerste 24 uur na ziekenhuisopname (patiënten met verhoogde markers na coronaire interventieprocedures werden uitgesloten), en ontwikkeling van hartfalen tijdens ziekenhuisopname of follow-up.
Clinische follow-up
De gemiddelde follow-up was 186 (SD, 110; mediaan, 156) dagen, gedurende welke tijd alle klinische gebeurtenissen van de patiënten werden geregistreerd. De follow-up werd uitgevoerd door telefonisch contact, in poliklinieken, en door het bekijken van de medische dossiers van de patiënten in het ziekenhuis.
Statistische analyse
Alle informatie werd prospectief geregistreerd in een database gemaakt met Microsoft Office Access 2003 SP2. De statistische analyses werden uitgevoerd met SPSS (Statistical Package for the Social Sciences), versie 12.0. De categorische of dichotome variabelen werden uitgedrukt in absolute waarden en percentages, en werden vergeleken met de Pearson χ2 test. De continue variabelen met een normale verdeling zijn beschreven als het gemiddelde (SD), en de Student t test werd gebruikt voor de vergelijkingen tussen groepen. Variabelen die geen Gaussische verdeling vertoonden, werden vergeleken met de Mann-Whitney U-test.
Spearman’s correlatiecoëfficiënt werd gebruikt om de correlaties van cystatine C-concentratie met hoog-gevoelig C-reactief proteïne en glomerulaire filtratiesnelheid te evalueren. Een logistische regressieanalyse werd gebruikt om de onafhankelijke rol van klinische en laboratoriumfactoren met betrekking tot cystatine C te beoordelen voor het voorspellen van de ontwikkeling van cardiovasculaire complicaties tijdens ziekenhuisopname, inclusief de significante variabelen in de univariate analyse. De aangepaste odds ratio’s en 95% betrouwbaarheidsintervallen (CI) worden gepresenteerd. Kaplan-Meier overlevingscurven tijdens follow-up werden geconstrueerd en vergeleken met behulp van de long-rank test.
Om een beschrijvende analyse van de bestudeerde populatie uit te voeren, werden enkele kwantitatieve variabelen in intervallen ingedeeld: de glomerulaire filtratiesnelheid (>90, 90-60, 55% en 0,95 en
Een P-waarde kleiner dan .05 werd als statistisch significant beschouwd.
RESULTATEN
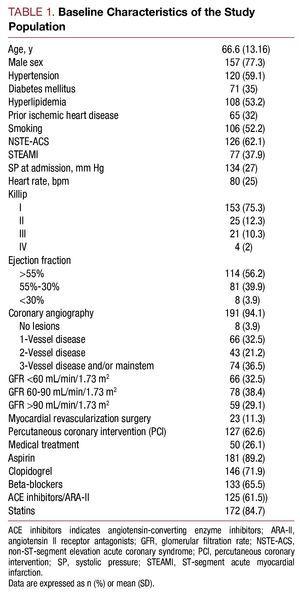
Van mei 2006 tot juli 2007 werden 203 patiënten die in het ziekenhuis waren opgenomen met een diagnose van hoog-risico ACS in de studie opgenomen. De gemiddelde leeftijd was 66,6 (13,16) jaar. Van het totaal presenteerde 62,1% van de patiënten (n=126) niet-ST-segment elevatie ACS en 37,9% (n=77), ST-segment elevatie ACS. De basislijnkenmerken van de studiepopulatie zijn beschreven in tabel 1.
De mediane cystatine C-concentratie was 1,01 (range, 0,83-1,35) mg/L, plasmacreatinine bij de eerste uitgevoerde analyse was 1 (0.9-1,3) mg/L, glomerulaire filtratiesnelheid was 72,4 (49,12-93,73) ml/min/1,73 m2, en hoog-gevoelig C-reactief proteïne was 1,37 (0,46-5,02) mg/L. De glomerulaire filtratie ten tijde van de ziekenhuisopname was 2 bij 32,5% van de patiënten en het serum cystatine C was >0,95 mg/L bij 113 (55,7%) patiënten.
Patiënten met hogere cystatine C-waarden presenteerden een slechter klinisch profiel, waren ouder, hadden een hoge prevalentie van hypertensie, slechtere Killip-klasse op het moment van ziekenhuisopname, ernstiger coronaire ziekte op coronaire angiografie, en hogere plasma creatinine en C-reactief proteïne waarden (tabel 2).
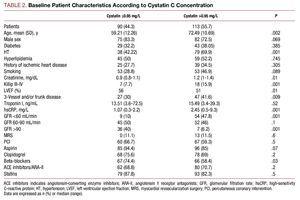
Er waren geen significante verschillen tussen de 2 cystatine C-groepen wat betreft de uitgevoerde coronaire interventie; het uiteindelijke angiografische resultaat gaf een vergelijkbaar succespercentage en geen significante complicaties (3,27% voor patiënten met cystatine C ≤0,95 en 4,09% in de andere groep). Analyse van de farmacologische behandeling toonde een aanzienlijk hoger gebruik van bètablokkers en aspirine in de groep met cystatine C ≤0,95 (Tabel 2).
Serum cystatine C waarden vertoonden een hogere correlatie met geschatte glomerulaire filtratiesnelheid (r=-0,655; P=,001) (figuur 1) dan met microalbuminurie (r=0,302, P=,01) en een lagere correlatie met C-reactief proteïne (r=0,29; P=,01).
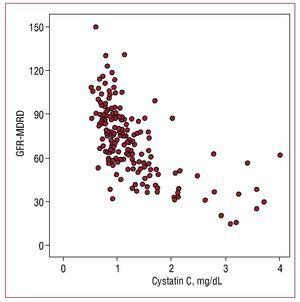
Figuur 1. Correlatie tussen cystatine C-waarden en glomerulaire filtratiesnelheid geschat met de MDRD-formule (GFR-MDRD).
In de groep patiënten met cystatine C-waarden >0,95, vertoonde 6,5% normale glomerulaire filtratiesnelheden en 46%, glomerulaire filtratiesnelheden tussen 60 en 90 ml/min/1,73 m2. Bovendien had 10% van de patiënten met nierdisfunctie met een filtratiesnelheid van 2 cystatine C-waarden
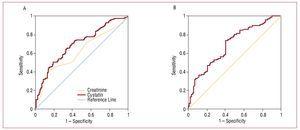
Figuur 2. A, ROC’s van cystatine C en creatinine in relatie tot de ontwikkeling van cardiovasculaire complicaties (hartfalen, infarct, en cardiovasculair overlijden). B, ROC-curve van de glomerulaire filtratiesnelheid geschat met de MDRD in relatie tot de ontwikkeling van cardiovasculaire complicaties (hartfalen, infarct, en cardiovasculair overlijden).
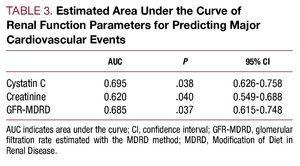
Het verblijf in het ziekenhuis duurde mediaan 9 (6-19) dagen. Vanaf het moment van opname tot de voltooiing van de follow-up van de studie hadden 56 (27,58%) patiënten uit de totale steekproef hartfalen ontwikkeld, de meesten van hen in de groep met verhoogde cystatine C-waarden (45 patiënten). De ziekenhuissterfte was significant hoger in de groep met verhoogde cystatine C-waarden (17,6% vs 3,3%; P=,001), en deze verschillen bleven bestaan tijdens de follow-up (figuur 3, tabel 4).
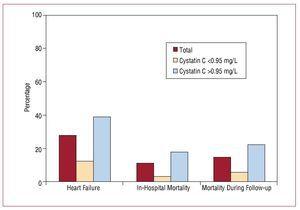
Figuur 3. Associatie tussen cystatine C 0,95 mg/L en de ontwikkeling van cardiovasculaire voorvallen in het ziekenhuis.

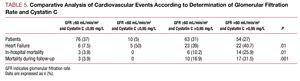
In de univariate analyse werd geen associatie waargenomen tussen cardiovasculaire complicaties en het type ACS, hyperlipidemie, of piek TpI-concentratie, maar er werd wel een associatie gevonden met de overige cardiovasculaire risicofactoren: aantal aangetaste bloedvaten, ejectiefractie, nierfunctie-markers, cystatine C, en hoog-gevoelig C-reactief proteïne. Wanneer de resultaten van patiënten met een glomerulaire filtratiesnelheid van >60 ml/min/1,73 m2 werden geanalyseerd, vonden we dat patiënten met cystatine C >0.95 mg/L een significant hoger percentage cardiovasculaire complicaties vertoonden dan patiënten met een glomerulaire filtratie >60 en cystatine C
De geschatte gebeurtenisvrije overleving (d.w.z. geen hartfalen, myocardinfarct of overlijden) na een gemiddelde follow-up van 186 dagen was significant hoger in de groep van patiënten met cystatinewaarden ≤0.95 mg/L: 75% versus 44% (P=.02) (figuur 4).

Figuur 4. Kaplan-Meier-curven voor de schatting van de waarschijnlijkheid van overleving vrij van belangrijke cardiovasculaire gebeurtenissen, afhankelijk van de cystatine C-waarde.
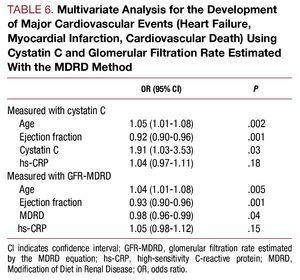
In de multivariate analyse werden leeftijd, ejectiefractie en cystatine C-concentratie geïdentificeerd als onafhankelijke voorspellende factoren voor cardiovasculaire complicaties tijdens ziekenhuisopname (tabel 6).
DISCUSSIE
De resultaten van de huidige studie geven aan dat verhoogde cystatine C-waarden de ontwikkeling van hartfalen, myocardinfarct en cardiovasculair overlijden in het ziekenhuis voorspellen bij patiënten met hoog-risico ACS, onafhankelijk van andere klassieke risicofactoren. Bovendien kunnen plasma cystatine C-waarden patiënten met een hoog risico op cardiovasculaire complicaties tijdens ziekenhuisopname mogelijk beter stratificeren dan andere methoden voor het beoordelen van de nierfunctie. Wij vonden dat een verhoogde cystatine C-waarde geassocieerd was met een slechtere cardiovasculaire prognose, zelfs in de groep van patiënten met een normale glomerulaire filtratie. Voor zover wij weten, is dit het eerste verslag van deze associatie, die volgens ons implicaties kan hebben voor de risicostratificatie in deze patiëntenpopulatie.
In de afgelopen jaren hebben verschillende artikelen een nauw verband beschreven tussen nierdisfunctie en cardiovasculaire complicaties tijdens de follow-up van patiënten met acute en chronische ischemische hartziekte, evenals andere klinische presentaties van cardiovasculaire ziekte, in het bijzonder hartfalen.1,10-12 Een verlaging van de glomerulaire filtratie tot minder dan 60 mL/min is gerelateerd aan een aanzienlijke toename van het risico op overlijden, myocardinfarct en beroerte, zowel bij patiënten met als zonder eerdere hart- en vaatziekten.13 Deze relatie is met name beschreven bij ACS-patiënten met ST-segment-elevatie en patiënten zonder ST-segment-elevatie.10,13-15 In de VALIANT-studie16 (patiënten met ventrikeldisfunctie en hartfalen na ST-segment-elevatie myocardinfarct) was verslechtering van de nierfunctie (beoordeeld met de glomerulaire filtratiesnelheid) geassocieerd met een toename van de mortaliteit en cardiovasculaire complicaties tijdens de follow-up. Soortgelijke resultaten zijn gerapporteerd voor de patiëntenpopulaties in de SAVE- (postinfarct ventriculaire disfunctie), HOPE- (patiënten met een hoog cardiovasculair risico, de meerderheid met chronische ischemische hartziekte) en PEACE-studies (patiënten met chronische ischemische hartziekte). In deze studies werd het verband tussen nierdisfunctie en de prognose waargenomen voor zowel de verlaagde glomerulaire filtratiesnelheid als voor de uitscheiding van albumine in de urine.16-19
Zoals hierboven vermeld, is een direct 2-weg verband beschreven tussen nierdisfunctie en hart- en vaatziekten. Chronisch nierfalen bevordert de ontwikkeling van hypertensie en dyslipidemie, en de activering van het renine-angiotensinaldosteronsysteem. Deze factoren lijken, samen met de toename van ontstekingsmediatoren, bij te dragen tot een hogere productie van vrije radicalen, die een rol spelen in het atherosclerotische proces en de cardiovasculaire schade. Bovendien bevorderen veranderingen in het mineraalmetabolisme (toename van de promotors en afname van de remmers van calcificatie) calciumafzettingen in de coronaire vaten.20,21 Ten slotte is bij patiënten met nierdisfunctie een minder intensief gebruik van therapeutische interventies met erkend klinisch en prognostisch voordeel beschreven. Met name bij ACS-patiënten kunnen een minder agressieve behandeling en een langer uitstel van interventionele coronaire procedures, evenals een lager gebruik van IIb/IIIa, blokkers van de renineangiotensine-aldosteron-as, bètablokkers, statines en bloedplaatjesaggregatieremmers, bijdragen aan de slechtere prognose die bij deze patiëntenpopulatie wordt beschreven.22
In de dagelijkse klinische praktijk is de beoordeling van de nierfunctie gewoonlijk gebaseerd op serumcreatininebepalingen en schattingen van de glomerulaire filtratiesnelheid met behulp van de Cockcroft-Gault- of MDRD-formules. Deze beide methoden vertonen een aantal beperkingen, waarvan vele voortvloeien uit factoren die de creatinineproductie beïnvloeden, zoals leeftijd, vrouwelijk geslacht, rasgebonden kenmerken, voeding en het verloop van chronische ziekten.
Deze vergelijkingen werden onlangs geëvalueerd bij patiënten met hartfalen en vergeleken met NT-proBNP, een prognostische marker. De prognostische informatie van NT-proBNP bleek superieur te zijn aan die van de nierfunctie die wordt geschat met de MDRD-formule.23
Cystatine C bezit moleculaire en metabolische eigenschappen die van plasmaconcentraties van dit eiwit een goede biologische marker maken voor het schatten van de nierfunctie; kleine functionele veranderingen worden gedetecteerd met een hogere gevoeligheid dan de conventionele parameters die voor dit doel worden gebruikt.24 Dit kan het feit rechtvaardigen dat in de groep patiënten met serum cystatine C concentraties boven de bovenste normaalgrens, 15% een normale glomerulaire filtratiesnelheid vertoonde; bepaling van statine C kan nuttig zijn voor het identificeren van patiënten met een preklinische toestand van nierziekte.6
De in de huidige studie verkregen resultaten komen tot op zekere hoogte overeen met de gerapporteerde bevindingen die erop wijzen dat cystatine C een onafhankelijke voorspeller is van cardiovasculaire complicaties bij patiënten met coronaire aandoeningen.25-27 Bovendien kunnen onze gegevens dit concept uitbreiden tot patiënten met een normale glomerulaire filtratiesnelheid. Jernberg et al26 analyseerden de relatie tussen plasma cystatine C-waarden en prognose in een groep patiënten die in het ziekenhuis waren opgenomen voor niet-ST-segment-elevatie ACS, en rapporteerden een significant verband tussen cystatine C-waarden en mortaliteit. Er is ook beschreven dat verhoogde cystatine C concentraties geassocieerd zijn met een verhoogd risico op overlijden, cardiovasculaire complicaties, en het optreden van hartfalen bij poliklinische patiënten met chronische coronaire ziekte.24 Bij oudere personen zonder manifeste nierziekte is cystatine C een risicomarker voor overlijden, cardiovasculaire ziekte, en chronische nierziekte.6 In de huidige studie vonden wij dat patiënten met verhoogde cystatine C waarden een slechter risicoprofiel hadden; de relatief lage C-reactief proteïne spiegel was echter verrassend. Wij denken dat dit kan worden verklaard door de kinetica van het eiwit, dat een specifiek, gekarakteriseerd spectrum heeft waarin de waarde afhangt van het tijdstip waarop het monster wordt genomen (de piek treedt op 49 uur na het begin van de symptomen, en een meer vertraagde piek wordt gezien in ST-segment-elevatie acuut myocardinfarct); in onze studie werden monsters genomen binnen de eerste 24 uur na ziekenhuisopname.28 De cardiovasculaire complicaties bij de patiënten in onze studie verschillen van die welke in recente registers zijn gepubliceerd,29 en dit kan komen doordat patiënten met een zeer hoog risico en een hogere incidentie van complicaties werden geïncludeerd. In het recent gepubliceerde MASCARA-register was slechts 50% van de geïncludeerde patiënten aanvankelijk opgenomen op een ICU of hart-ICU, terwijl al onze patiënten afkomstig waren van een hart-ICU, een feit dat ongetwijfeld enige selectiebias impliceert. Niettemin bestond de patiëntengroep met verhoogde cystatine C uit een populatie met een significant hoger risicoprofiel en aantal cardiovasculaire complicaties dan de overige patiënten. De huidige studie draagt bij tot een grotere nauwkeurigheid in deze associaties door voor het eerst te rapporteren dat verhoogde cystatine C-spiegels in de eerste uren van ziekenhuisopname voor hoog-risico ACS een onafhankelijke voorspeller zijn van cardiovasculaire complicaties in het ziekenhuis. Bovendien is de associatie tussen cystatine C en een risico op cardiovasculaire complicaties hoger dan die van andere veel gebruikte parameters voor het schatten van de nierfunctie, en blijft deze zelfs gehandhaafd in de groep patiënten met een normale glomerulaire filtratie. Momenteel is niet precies bekend of het vermogen om een hoger risico op complicaties te voorspellen voortkomt uit het feit dat cystatine C een betere marker van de nierfunctie is dan andere gangbare parameters (serumcreatinine en glomerulaire filtratiesnelheid), of dat er naast glomerulaire filtratie nog andere factoren zijn die van invloed zijn op de cystatine C-concentratie en die rechtstreeks in verband kunnen worden gebracht met het cardiovasculaire risico. In deze lijn is een positieve correlatie van plasma C-reactief proteïne waarden en fibrinogeen met verhoogde cystatine C concentraties en de aanwezigheid van hart- en vaatziekten beschreven.30 In de PRIME studie (Prospective Epidemiological Study of Myocardial Infarction) werd de associatie tussen cystatine C en de ontwikkeling van acuut myocardinfarct hartdood en angina onderzocht bij patiënten zonder coronaire aandoeningen. Na correctie voor de gemeenschappelijke cardiovasculaire risicofactoren was de cystatine C-spiegel in plasma significant geassocieerd met de ontwikkeling van de eerste coronaire complicatie van ischemische oorsprong. Volgens de auteurs zou de lagere glomerulaire filtratiesnelheid de hogere cystatine C-waarden van de gevallen ten opzichte van de controles niet rechtvaardigen, en zij stelden voor dat ontsteking aan de basis zou kunnen liggen van het verband tussen cystatine C en het risico van hart- en vaatziekten.31,32 In overeenstemming met deze gegevens toonden onze resultaten een positieve correlatie aan tussen cystatine C en hooggevoelig C-reactief proteïne (r=0,2), dat ook een onafhankelijke voorspeller is van cardiovasculaire complicaties, en leveren verder bewijs om de aanwezigheid van directe relaties tussen nieraandoeningen, ontsteking en cardiovasculaire aandoeningen te rechtvaardigen.
Tot de belangrijkste beperkingen van de gepresenteerde studie moet worden gerekend dat de resultaten alleen betrekking hebben op patiënten met hoog-risico ACS die in een hart-IC werden opgenomen en waarvan de meerderheid agressief werd behandeld met vroege coronaire angiografie. Anderzijds moeten deze kenmerken worden benadrukt, omdat er weinig informatie is over deze specifieke populatie, bij wie cystatine C werd gemeten bij ziekenhuisopname. In bijna alle gepubliceerde studies is het tijdstip van de bepalingen niet aangegeven en, althans bij ACS-patiënten, kunnen de plasma-cystatine C-concentraties worden beïnvloed door de tijd die is verstreken sinds de gebeurtenis en de uitgevoerde diagnostische en therapeutische interventies. De beperking van een korte follow-up belemmert de uitbreiding van onze waarnemingen tot de middellange of lange termijn. Niettemin bieden onze bevindingen een mogelijkheid om de risicostratificatie te verbeteren bij patiënten die in het ziekenhuis zijn opgenomen voor ACS met een hoog risico, wat nuttig zal zijn voor het bepalen van de therapie en voor het vaststellen van de diagnose.
CONCLUSIES
Cystatine C-bepaling op het moment van ziekenhuisopname bij patiënten met hoog-risico ACS kan een goed klinisch hulpmiddel zijn voor stratificatie van cardiovasculair risico. Bepaling van dit eiwit zou een aanvulling zijn op de informatie die andere methoden voor de beoordeling van de nierfunctie opleveren en zou, naast de diagnostische implicaties, nuttig kunnen zijn voor de identificatie van de groep met het hoogste risico. Het kan nodig zijn bijzondere aandacht te besteden aan de naleving van de aanbevelingen in de richtlijnen voor klinische praktijk bij deze populatie. Bovendien zou cystatine C belangrijke informatie kunnen leveren voor het stratificeren van patiënten met ACS met een hoog risico en een behouden nierfunctie. Aanvullende studies met een langere follow-up kunnen nodig zijn om de rol van cystatine C bij ACS met grotere precisie te definiëren.
ABBREVIATIES
ACS: acuut coronair syndroom
MDRD: Modification of Diet in Renal Disease
TpI: troponine I
