![]()
Personen die gebruik maken van ondersteunende technologie hebben mogelijk niet volledig toegang tot de informatie in dit bestand. Voor hulp kunt u een e-mail sturen naar: [email protected]. Typ 508 Accommodatie en de titel van het rapport in de onderwerpregel van de e-mail.
![]() PDF
PDF
De Advisory Committee on Immunization Practices (ACIP) herziet jaarlijks het aanbevolen vaccinatieschema voor volwassenen om ervoor te zorgen dat het schema de huidige aanbevelingen voor het gebruik van toegestane vaccins weerspiegelt. In juni 2005 heeft de ACIP het Immunisatieschema voor volwassenen voor oktober 2005-september 2006 goedgekeurd. Dit schema is ook goedgekeurd door de American Academy of Family Physicians en het American College of Obstetricians and Gynecologists.
Veranderingen in het schema voor oktober 2005-september 2006
Het schema voor 2005-2006 verschilt als volgt van het vorige schema:
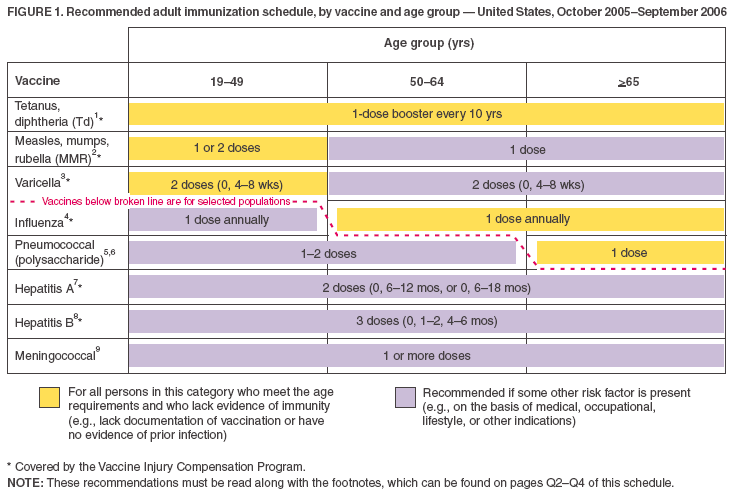
- Vaccins die zijn opgenomen in het leeftijdsgebaseerde schema (Figuur 1) worden weergegeven zodat vaccins die worden aanbevolen voor routinematig gebruik kunnen worden onderscheiden van vaccins die worden aanbevolen voor volwassenen met bepaalde risico-indicatoren (vergelijkbaar met het kinderimmunisatieschema). Dit wordt zowel geïllustreerd door het kleurenschema als door de onderbroken lijn.
- De gele balken (“Voor alle personen in deze groep”) en de groene balken (“Voor personen zonder documentatie van vaccinatie of bewijs van ziekte”) uit het vorige schema zijn samengevoegd tot één gele balk, die nu luidt: “Voor alle personen in deze categorie die voldoen aan de leeftijdsvereisten en die geen bewijs van immuniteit hebben (b.v, geen documentatie van vaccinatie hebben of geen bewijs van eerdere infectie hebben).”
- De paarse balk is veranderd van “Voor personen die een risico lopen (bv. met medische/blootstellingsindicaties)” in “Aanbevolen indien er een andere risicofactor aanwezig is (bv. op basis van medische, beroeps-, leefstijl-, of andere indicaties).” De paarse balk werd toegevoegd aan de leeftijdskolommen 50-64 jaar en >65 jaar voor mazelen, bof, rodehond (MMR)-vaccin.
- De kolom, “Diabetes, hartaandoening, chronische longaandoening, of chronische leveraandoening met inbegrip van chronisch alcoholisme” is omgezet met de kolom, “Aangeboren immunodeficiëntie, leukemie, lymfoom, gegeneraliseerde maligniteit, therapie met alkylerende middelen, antimetabolieten, hersenvochtlekkage, bestraling, of grote hoeveelheden corticosteroïden” op het medische/andere indicatieschema (figuur 2), zodat contra-indicaties voor MMR- en varicellavaccins nu naast elkaar staan.
- De rij voor varicella-vaccin is op beide figuren naar boven verplaatst (d.w.z, naar onmiddellijk na het MMR-vaccin) omdat het vaccin nu universeel wordt aanbevolen voor bepaalde leeftijdsgroepen.
- Meningokokkenvaccin is toegevoegd aan het schema voor medische/andere indicaties (figuur 2). De voetnoot is herzien om de recent gepubliceerde ACIP-aanbevelingen voor dit vaccin op te nemen (1).
- De tetanus en difterie voetnoot (#1) is geherformuleerd.
- De varicella voetnoot (#3) is geherformuleerd in overeenstemming met de ACIP-aanbevelingen die in juni 2005 zijn aangenomen.
- De influenza-voetnoot (#4) is herzien om de nieuwste hoogrisicoconditie toe te voegen: neuromusculaire aandoeningen die de ademhalingsfunctie aantasten (2).
- Er is een 10e voetnoot toegevoegd over Haemophilus influenzae type b vaccinatie voor populaties met een hoog risico (d.w.z., personen met asplenie, leukemie, en humaan immunodeficiëntie virus infectie).
Het Volwassenen Immunisatie Schema is beschikbaar in het Engels en Spaans op http://www.cdc.gov/nip/recs/adult-schedule.htm. Algemene informatie over immunisatie van volwassenen, inclusief aanbevelingen betreffende vaccinatie van personen met HIV en andere immunosuppressieve aandoeningen, is verkrijgbaar bij staats- en lokale gezondheidsafdelingen en bij het National Immunization Program op http://www.cdc.gov/nip. Vaccin informatie verklaringen zijn beschikbaar op http://www.cdc.gov/nip/publications/vis. ACIP-verklaringen voor elk aanbevolen vaccin kunnen worden bekeken, gedownload en afgedrukt van de website van het National Immunization Program op http://www.cdc.gov/nip/publications/acip-list.htm. Instructies voor het melden van ongewenste voorvallen aan het Vaccine Adverse Event Reporting System zijn beschikbaar op http://www.vaers.hhs.gov of per telefoon, 800-822-7967.
- CDC. Prevention and control of meningococcal disease: recommendations of the Advisory Committee for Immunization Practices (ACIP). MMWR 2005;54(No. RR-7).
- CDC. Prevention and control of influenza: recommendations of the Advisory Committee for Immunization Practices (ACIP). MMWR 2005;54(No. RR-8).
Figuur 1
Return to top.
Figuur 2

Return to top.
Goedgekeurd door de Advisory Committee on Immunization Practices, het American College of Obstetricians and Gynecologists, en de American Academy of Family Physicians
1. Tetanus en difterie (Td) vaccinatie. Volwassenen met een onzekere voorgeschiedenis van een volledige primaire vaccinatieserie met difterie- en tetanustoxoïd-bevattende vaccins dienen een primaire serie te krijgen met gecombineerd Td-toxoïd. Een primaire serie voor volwassenen bestaat uit 3 doses; dien de eerste 2 doses ten minste 4 weken na elkaar toe en de derde dosis 6-12 maanden na de tweede. Dien 1 dosis toe als de persoon de primaire serie heeft ontvangen en als de laatste vaccinatie >10 jaar daarvoor is ontvangen. Raadpleeg de ACIP-verklaring voor aanbevelingen voor het toedienen van Td als profylaxe bij wondbehandeling (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). De American College of Physicians Task Force on Adult Immunization ondersteunt een tweede optie voor het gebruik van Td bij volwassenen: een enkele Td-booster op de leeftijd van 50 jaar voor personen die de volledige pediatrische reeks hebben voltooid, inclusief de tiener/jonge-volwassene booster. Een nieuw toegelaten tetanus-diftheria-acellulair-pertussisvaccin is beschikbaar voor volwassenen. De aanbevelingen van de ACIP voor het gebruik ervan zullen worden gepubliceerd.
2. Mazelen, bof, rodehond (MMR) vaccinatie. Mazelencomponent: volwassenen geboren vóór 1957 kunnen worden beschouwd als immuun voor mazelen. Volwassenen geboren tijdens of na 1957 moeten >1 dosis MMR krijgen tenzij zij een medische contra-indicatie hebben, documentatie van >1 dosis, geschiedenis van mazelen gebaseerd op diagnose van de zorgverlener, of laboratoriumbewijs van immuniteit. Een tweede dosis MMR wordt aanbevolen voor volwassenen die 1) recentelijk zijn blootgesteld aan mazelen of in een uitbraaksituatie; 2) eerder zijn ingeënt met een gedood mazelenvaccin; 3) zijn ingeënt met een onbekend type mazelenvaccin in de periode 1963-1967; 4) student zijn aan een postsecundaire onderwijsinstelling; 5) werkzaam zijn in een gezondheidszorginstelling; of 6) van plan zijn internationaal te reizen. Onthoud MMR- of andere mazelen bevattende vaccins van HIV-geïnfecteerde personen met ernstige immunosuppressie. Bofcomponent: 1 dosis MMR-vaccin zou voldoende moeten zijn voor bescherming van degenen die tijdens of na 1957 geboren zijn en die geen bof in de anamnese hebben gehad op basis van een diagnose van de zorgverlener of die geen laboratoriumbewijs van immuniteit hebben. Rubellacomponent: Dien 1 dosis MMR-vaccin toe aan vrouwen wier rubellavaccinatiegeschiedenis onbetrouwbaar is of die geen laboratoriumbewijs van immuniteit hebben. Voor vrouwen in de vruchtbare leeftijd, ongeacht het geboortejaar, routinematig bepalen van rubella-immuniteit en vrouwen adviseren met betrekking tot congenitaal rubella-syndroom. Vaccineer geen vrouwen die zwanger zijn of zwanger zouden kunnen worden binnen 4 weken na ontvangst van het vaccin. Vrouwen die geen bewijs van immuniteit hebben, moeten MMR-vaccin krijgen na voltooiing of beëindiging van de zwangerschap en vóór ontslag uit de gezondheidszorg.
3. Varicellavaccinatie. Varicellavaccinatie wordt aanbevolen voor alle volwassenen zonder bewijs van immuniteit tegen varicella. Speciale aandacht moet worden gegeven aan degenen die 1) nauw contact hebben met personen met een hoog risico op ernstige ziekte (gezondheidswerkers en gezinscontacten van immuungecompromitteerde personen) of 2) een hoog risico lopen op blootstelling of transmissie (bijv. leraren van jonge kinderen; medewerkers in de kinderopvang; bewoners en medewerkers van instellingen, inclusief penitentiaire inrichtingen; universiteitsstudenten; militair personeel; adolescenten en volwassenen die in huishoudens met kinderen wonen; niet-zwangere vrouwen in de vruchtbare leeftijd; en internationale reizigers). Bewijs van immuniteit voor varicella bij volwassenen omvat een van de volgende zaken 1) gedocumenteerde leeftijdsgebonden varicellavaccinatie (d.w.z. ontvangst van 1 dosis vóór de leeftijd van 13 jaar of ontvangst van 2 doses na de leeftijd van 13 jaar); 2) in de V.S. geboren vóór 1966 of geschiedenis van varicellaziekte vóór 1966 voor niet in de V.S.3) een voorgeschiedenis van varicella gebaseerd op een diagnose van een gezondheidszorgverstrekker of een door de ouders of door de patiënt zelf gerapporteerde typische varicellaziekte voor personen geboren tussen 1966 en 1997 (voor een patiënt die een voorgeschiedenis van een atypisch, mild geval rapporteert, moeten gezondheidszorgverstrekkers een epidemiologisch verband met een typisch varicellageval of bewijs van laboratoriumbevestiging zoeken, indien dit ten tijde van de acute ziekte werd uitgevoerd); 4) een voorgeschiedenis van herpes zoster gebaseerd op een diagnose van een gezondheidszorgverstrekker; of 5) laboratoriumbewijs van immuniteit. Vaccineer geen vrouwen die zwanger zijn of zwanger zouden kunnen worden binnen 4 weken na ontvangst van het vaccin. Beoordeel zwangere vrouwen op bewijs van immuniteit voor varicella. Vrouwen die geen bewijs van immuniteit hebben, moeten dosis 1 van het varicellavaccin toegediend krijgen na voltooiing of beëindiging van de zwangerschap en vóór ontslag uit de instelling voor gezondheidszorg. Dosis 2 moet 4-8 weken na dosis 1 worden toegediend.
4. Influenza vaccinatie. Medische indicaties: chronische aandoeningen van het cardiovasculaire of pulmonale systeem, inclusief astma; chronische stofwisselingsziekten, inclusief diabetes mellitus, nierdisfunctie, hemoglobinopathieën of immunosuppressie (inclusief immunosuppressie veroorzaakt door medicijnen of HIV); elke aandoening (bijv, cognitieve stoornis, ruggenmergletsel, aanvalsstoornis of andere neuromusculaire stoornis) die de ademhalingsfunctie of de verwerking van ademhalingssecreties belemmert of die het risico op aspiratie kan verhogen; en zwangerschap tijdens het griepseizoen. Er bestaan geen gegevens over het risico op ernstige of gecompliceerde influenza bij personen met asplenie; influenza is echter een risicofactor voor secundaire bacteriële infecties die ernstige ziekte kunnen veroorzaken bij personen met asplenie. Beroepsindicaties: gezondheidswerkers en werknemers van instellingen voor langdurige zorg en zorginstellingen. Andere indicaties: bewoners van verpleeghuizen en andere instellingen voor langdurige zorg en begeleid wonen; personen die influenza kunnen overdragen op personen met een hoog risico (d.w.z. gezinscontacten en verzorgers van kinderen van 0-23 maanden, of personen van alle leeftijden met een hoog risico), en iedereen die gevaccineerd wil worden. Aan gezonde, niet-zwangere personen van 5 tot 49 jaar zonder hoogrisico-aandoeningen die geen contact hebben met ernstig immuungecompromitteerde personen op speciale zorgafdelingen, kan intranasaal toegediend influenzavaccin (FluMist®) worden toegediend in plaats van geïnactiveerd vaccin.
5. Pneumokokken polysaccharide vaccinatie. Medische indicaties: chronische aandoeningen van het longstelsel (met uitzondering van astma); hart- en vaatziekten; diabetes mellitus; chronische leveraandoeningen, inclusief leveraandoeningen als gevolg van alcoholmisbruik (bv. cirrose); chronisch nierfalen of nefrotisch syndroom; functionele of anatomische asplenie (bv, sikkelcelziekte of splenectomie ); immunosuppressieve aandoeningen (bv. aangeboren immunodeficiëntie, HIV-infectie, leukemie, lymfoom, multipel myeloom, ziekte van Hodgkin, gegeneraliseerde maligniteit, of orgaan- of beenmergtransplantatie); chemotherapie met alkylerende stoffen, antimetabolieten of langdurige systemische corticosteroïden; en cochleaire implantaten. Andere indicaties: Alaska Natives en bepaalde Amerikaans-Indiaanse bevolkingsgroepen; bewoners van verpleeghuizen en andere langdurige-zorginstellingen.
6. Herhalingsvaccinatie met pneumokokken polysaccharidenvaccin. Eenmalige herhalingsvaccinatie na 5 jaar voor personen met chronisch nierfalen of nefritisch syndroom; functionele of anatomische asplenie (bv. sikkelcelziekte of splenectomie); immunosuppressieve aandoeningen (bv, aangeboren immunodeficiëntie, HIV-infectie, leukemie, lymfoom, multipel myeloom, ziekte van Hodgkin, gegeneraliseerde maligniteit, of orgaan- of beenmergtransplantatie); of chemotherapie met alkylerende middelen, antimetabolieten of langdurige systemische corticosteroïden. Voor personen >65 jaar, eenmalige hervaccinatie indien zij >5 jaar eerder zijn gevaccineerd en <65 jaar waren ten tijde van de primaire vaccinatie.
7. Hepatitis A vaccinatie. Medische indicaties: personen met stollingsfactor stoornissen of chronische leverziekte. Gedragsindicaties: mannen die seks hebben met mannen of gebruikers van illegale drugs. Beroepsindicaties: Personen die werken met hepatitis A virus (HAV)-geïnfecteerde primaten of met HAV in een onderzoekslaboratorium. Andere indicaties: personen die reizen naar of werken in landen met een hoge of gemiddelde endemiciteit van hepatitis A (voor de lijst van landen, ziehttp://www.cdc.gov/travel/diseases.htm#hepa), alsook personen die immuniteit wensen te verkrijgen. De huidige vaccins moeten worden toegediend in een reeks van twee doses, hetzij op de leeftijd van 0 en 6-12 maanden, hetzij op de leeftijd van 0 en 6-18 maanden. Indien het gecombineerde hepatitis A- en hepatitis B-vaccin wordt gebruikt, dienen 3 doses te worden toegediend bij 0, 1, en 6 maanden.
8. Hepatitis B-vaccinatie. Medische indicaties: hemodialysepatiënten (gebruik speciale formulering of twee doses van 20-µg/mL) of patiënten die stollingsfactorconcentraten toegediend krijgen. Beroepsmatige indicaties: gezondheidswerkers en werknemers in de openbare veiligheid die op het werk aan bloed worden blootgesteld en personen in opleiding in scholen voor geneeskunde, tandheelkunde, verpleegkunde, laboratoriumtechnologie en andere beroepen in de toegepaste gezondheidszorg. Gedragsindicaties: gebruikers van injectiedrugs; personen met meer dan één sekspartner in de voorafgaande 6 maanden; personen met een recentelijk opgelopen seksueel overdraagbare aandoening (SOA); en mannen die seks hebben met mannen. Andere indicaties: gezinscontacten en sekspartners van personen met chronische hepatitis B-virus (HBV); cliënten en personeel van instellingen voor mensen met een ontwikkelingsachterstand; alle cliënten van SOA-klinieken; gedetineerden van penitentiaire inrichtingen; en internationale reizigers die langer dan 6 maanden in landen met een hoge of gemiddelde prevalentie van chronische HBV-infectie zullen verblijven (voor de lijst van landen, zie http://www.cdc.gov/travel/diseases.htm#hepa).
9. Meningokokkenvaccinatie. Medische indicaties: volwassenen met anatomische of functionele asplenie of terminale complementcomponentdeficiënties. Andere indicaties: eerstejaars studenten die in slaapzalen wonen; microbiologen die routinematig worden blootgesteld aan isolaten van Neisseria meningitidis; militaire rekruten; en personen die reizen naar of wonen in landen waar meningokokkenziekte hyperendemisch of epidemisch is (bijvoorbeeld de “meningitisgordel” van Afrika ten zuiden van de Sahara tijdens het droge seizoen), vooral als er langdurig contact met de plaatselijke bevolking zal zijn. Vaccinatie wordt door de regering van Saoedi-Arabië verplicht gesteld voor alle reizigers naar Mekka tijdens de jaarlijkse hadj. Meningokokkenconjugaatvaccin heeft de voorkeur voor volwassenen die aan een van de bovenstaande indicaties voldoen en <55 jaar oud zijn, hoewel meningokokkenpolysaccharidenvaccin (MPSV4) een aanvaardbaar alternatief is. Revaccinatie na 5 jaar zou geïndiceerd kunnen zijn voor volwassenen die eerder gevaccineerd zijn met MPSV4 en die een hoog risico op infectie blijven lopen (bijv. personen die verblijven in gebieden waar de ziekte epidemisch is).
10. Geselecteerde aandoeningen waarvoor Haemophilus influenzae type b (Hib)-vaccin kan worden gebruikt. Hib-conjugaatvaccins zijn toegelaten voor kinderen van 6-71 maanden. Er zijn geen gegevens beschikbaar over de werkzaamheid waarop een aanbeveling kan worden gebaseerd betreffende het gebruik van Hib-vaccin voor oudere kinderen en volwassenen met chronische aandoeningen die in verband worden gebracht met een verhoogd risico op Hib-ziekte. Studies suggereren echter een goede immunogeniciteit bij patiënten die sikkelcelziekte, leukemie of HIV-infectie hebben of die een splenectomie hebben ondergaan; het toedienen van vaccin aan deze patiënten is niet gecontra-indiceerd.
Het aanbevolen immunisatieschema voor volwassenen is goedgekeurd door de Advisory Committee on Immunization Practices, het American College of Obstetricians and Gynecologists, en de American Academy of Family Physicians. Het standaard MMWR-voetnootformaat is gewijzigd voor publicatie van dit schema.
Geadviseerde citatie: Centers for Disease Control and Prevention. Recommended Adult Immunization Schedule—Verenigde Staten, oktober 2005–september 2006. MMWR 2005;54:Q1–Q4.
Dit schema geeft de aanbevolen leeftijdsgroepen en medische indicaties voor routinetoediening van momenteel gelicentieerde vaccins voor personen van >19 jaar. Combinatievaccins waarvoor een vergunning is verleend, mogen worden gebruikt wanneer een van de componenten van de combinatie geïndiceerd is en wanneer de andere componenten van het vaccin niet gecontra-indiceerd zijn. Raadpleeg voor gedetailleerde aanbevelingen de bijsluiters van de fabrikanten en de volledige verklaringen van de ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Meld alle klinisch significante reacties na vaccinatie aan het Vaccine Adverse Event Reporting System (VAERS). Meldingsformulieren en instructies voor het indienen van een VAERS-rapport zijn verkrijgbaar per telefoon, 800-822-7967, of op de VAERS-website op http://www.vaers.hhs.gov.
Informatie over het indienen van een claim in het kader van het Vaccine Injury Compensation Program is verkrijgbaar op http://www.hrsa.gov/osp/vicp of per telefoon, 800-338-2382. Voor het indienen van een claim voor vaccinatieschade kunt u contact opnemen met de U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, telefoon 202-357-6400.
Aanvullende informatie over de hierboven genoemde vaccins en contra-indicaties voor vaccinatie is ook beschikbaar op http://www.cdc.gov/nip of bij het CDC-INFO Contact Center op 800-CDC-INFO (232-4636) in het Engels en Spaans, 24 uur per dag, 7 dagen per week.
Het gebruik van handelsnamen en commerciële bronnen dient uitsluitend ter identificatie en impliceert geen goedkeuring door het U.S. Department of Health and Human Services.Verwijzingen naar niet-CDC sites op het Internet worden aangeboden als een service aan MMWR lezers en impliceren geen goedkeuring van deze organisaties of hun programma’s door CDC of het U.S. Department of Health and Human Services. CDC is niet verantwoordelijk voor de inhoud van pagina’s die op deze sites te vinden zijn. URL-adressen die in MMWR zijn vermeld, waren actueel op de datum van publicatie.
Disclaimer Alle MMWR HTML-versies van artikelen zijn elektronische conversies van ASCII-tekst naar HTML. Deze conversie kan hebben geresulteerd in tekenvertaal- of formaatfouten in de HTML-versie. Gebruikers dienen niet te vertrouwen op deze HTML-versie, maar worden verwezen naar de elektronische PDF-versie en/of de originele papieren versie van MMWR voor de officiële tekst, figuren en tabellen. Een origineel papieren exemplaar van deze uitgave is verkrijgbaar bij de Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371; telefoon: (202) 512-1800. Neem contact op met GPO voor actuele prijzen.
**Vragen of berichten over fouten in de opmaak moeten worden gericht aan [email protected].
Datum laatste herziening: 10/13/2005
