 klik voor grote versie
klik voor grote versie
Röntgenfoto van de borst van vergrote, gehyperinflateerde longen, typisch voor patiënten met chronische obstructieve longziekte (COPD).
Case
Een 58-jarige rokende man met matig chronisch obstructieve longziekte (COPD) (FEV1 56% voorspeld) wordt voor de tweede keer dit jaar opgenomen met een acute exacerbatie van COPD. Hij kwam naar de spoedafdeling met toegenomen productieve hoest en kortademigheid, vergelijkbaar met eerdere exacerbaties. Hij ontkent koorts, myalgieën, of symptomen van de bovenste luchtwegen. Lichamelijk onderzoek is opmerkelijk voor bilateraal inspiratoir en expiratoir piepen. Zijn sputum is purulent. Hij krijgt continu verneveltherapie en één dosis oraal prednison, maar zijn dyspneu en piepende ademhaling houden aan. Op de röntgenfoto van de borstkas is geen infiltraat te zien.
Moet deze patiënt met antibiotica worden behandeld en, zo ja, welk schema is het meest geschikt?
Overzicht
Acute exacerbaties van COPD (AECOPD) vormen een grote last voor de gezondheid, maken meer dan 2,4% van alle ziekenhuisopnames uit en veroorzaken een aanzienlijke morbiditeit, mortaliteit en kosten.1 In 2006 en 2007 bedroeg het sterftecijfer aan COPD in de Verenigde Staten meer dan 39 sterfgevallen per 100.000 mensen, en meer recent werden de ziekenhuiskosten gerelateerd aan COPD geraamd op meer dan $13 miljard per jaar.2 Patiënten met AECOPD ervaren ook een verminderde kwaliteit van leven en een snellere achteruitgang van de longfunctie, wat de noodzaak van tijdige en passende behandeling nog benadrukt.1
In verschillende richtlijnen zijn behandelstrategieën voorgesteld die nu als standaardbehandeling voor AECOPD worden beschouwd.3,4,5,6 Deze omvatten het gebruik van corticosteroïden, bronchusverwijdende middelen en, in bepaalde gevallen, antibiotica. Hoewel er duidelijke aanwijzingen zijn voor het gebruik van steroïden en bronchusverwijders bij AECOPD, is er nog steeds discussie over het juiste gebruik van antibiotica bij de behandeling van acute exacerbaties. Er zijn meerdere potentiële factoren die tot AECOPD kunnen leiden, waaronder virussen, bacteriën en veelvoorkomende verontreinigende stoffen; daarom is een behandeling met antibiotica misschien niet geïndiceerd voor alle patiënten die zich met exacerbaties presenteren. Bovendien zijn de risico’s van een behandeling met antibiotica – waaronder bijwerkingen, selectie van resistente bacteriën en de bijbehorende kosten – niet onaanzienlijk.
Bacteriële infecties spelen echter een rol bij ongeveer 50% van de patiënten met AECOPD en voor deze groep kan het gebruik van antibiotica belangrijke voordelen opleveren.7
Interessant is dat een retrospectieve cohortstudie van 84.621 patiënten die waren opgenomen voor AECOPD aantoonde dat 85% van de patiënten op enig moment tijdens de ziekenhuisopname antibiotica kreeg.8
Ondersteuning voor antibiotica
Een aantal gerandomiseerde onderzoeken heeft de klinische uitkomsten vergeleken van patiënten met AECOPD die antibiotica kregen versus patiënten die placebo’s kregen. De meeste daarvan hadden kleine steekproeven en bestudeerden alleen ββ-lactam en tetracycline antibiotica in een poliklinische setting; er zijn beperkte gegevens met betrekking tot intramurale patiënten en nieuwere geneesmiddelen. Een meta-analyse toonde aan dat antibiotica het mislukken van de behandeling met 66% en de ziekenhuismortaliteit met 78% verminderden in de subset van onderzoeken met patiënten die in het ziekenhuis werden opgenomen.8 Een analyse van een groot retrospectief cohort van patiënten die in het ziekenhuis werden opgenomen voor AECOPD liet een significant lager risico op mislukken van de behandeling zien bij met antibiotica behandelde patiënten in vergelijking met onbehandelde patiënten.9 Meer in het bijzonder hadden behandelde patiënten een lager percentage ziekenhuissterfte en heropname voor AECOPD en een kleinere kans dat ze tijdens de indexopname alsnog mechanische beademing nodig hadden.
Data suggereren ook dat behandeling met antibiotica tijdens exacerbaties een gunstige invloed zou kunnen hebben op latere exacerbaties.10 Een retrospectieve studie van 18.928 Nederlandse patiënten met AECOPD vergeleek de resultaten van patiënten die als onderdeel van hun therapie antibiotica hadden gekregen (meestal doxycycline of een penicilline) met patiënten die dat niet hadden gekregen. De auteurs toonden aan dat de mediane tijd tot de volgende exacerbatie aanzienlijk langer was bij de patiënten die antibiotica kregen.10 Verder waren zowel het sterftecijfer als het totale risico op het ontwikkelen van een volgende exacerbatie significant verlaagd in de antibioticagroep, met een mediane follow-up van ongeveer twee jaar.
Indicaties voor antibiotica
Klinische symptomen. In een baanbrekend onderzoek van Anthonisen en collega’s werden drie klinische criteria vastgesteld die in latere onderzoeken en in de klinische praktijk de basis hebben gevormd voor de behandeling van AECOPD met antibiotica.11 Deze worden ook wel de “kardinale symptomen” van AECOPD genoemd en omvatten toegenomen dyspneu, sputumvolume en sputumzuiverheid. In deze studie werden 173 poliklinische patiënten met COPD gerandomiseerd naar een 10-daagse antibioticakuur of placebo bij het begin van een exacerbatie en klinisch gevolgd. De auteurs vonden dat met antibiotica behandelde patiënten significant meer kans hadden dan de placebogroep om behandelingssucces te bereiken, gedefinieerd als resolutie van alle verergerde symptomen binnen 21 dagen (68,1% vs. 55,0%, P<0,01).
Belangrijk is dat behandelde patiënten ook significant minder kans hadden op klinische verslechtering na 72 uur (9,9% vs. 18,9%, P<0,05). Patiënten met type I exacerbaties, gekenmerkt door alle drie de kardinale symptomen, hadden het meeste baat bij antibioticatherapie, gevolgd door patiënten met type II exacerbaties, bij wie slechts twee van de symptomen aanwezig waren. Latere studies hebben gesuggereerd dat purulentie van sputum goed correleert met de aanwezigheid van acute bacteriële infectie en daarom een betrouwbare klinische indicator kan zijn van patiënten die waarschijnlijk baat zullen hebben bij antibiotische therapie.12
Laboratoriumgegevens. Hoewel purulentie van sputum in verband wordt gebracht met bacteriële infectie, is een sputumkweek minder betrouwbaar, aangezien pathogene bacteriën vaak worden geïsoleerd bij patiënten met zowel AECOPD als stabiele COPD. De prevalentie van bacteriële kolonisatie bij matige tot ernstige COPD kan zelfs oplopen tot 50%.13 Daarom wordt een positieve bacteriële sputumkweek, bij afwezigheid van purulentie of andere tekenen van infectie, niet aanbevolen als de enige basis voor het voorschrijven van antibiotica.
Serum biomarkers, met name C-reactief proteïne (CRP) en procalcitonine, zijn onderzocht als een nieuwere benadering om patiënten te identificeren die baat zouden kunnen hebben bij een antibioticatherapie voor AECOPD. Studies hebben een verhoogde CRP-spiegel bij AECOPD aangetoond, vooral bij patiënten met purulent sputum en positieve bacteriële sputumkweken.12 Procalcitonine is bij voorkeur verhoogd bij bacteriële infecties.
Eén gerandomiseerd, placebogecontroleerd onderzoek bij gehospitaliseerde patiënten met AECOPD toonde een aanzienlijke vermindering van het antibioticagebruik aan op basis van lage procalcitoninespiegels, zonder een negatieve invloed te hebben op het klinisch succespercentage, de ziekenhuissterfte, de latere behoefte aan antibiotica, of de tijd tot de volgende exacerbatie.14 Vanwege inconsistent bewijs is het gebruik van deze markers als richtlijn voor het toedienen van antibiotica bij AECOPD echter nog niet definitief vastgesteld.14,15 Bovendien zijn deze laboratoriumuitslagen vaak niet beschikbaar op de plaats van zorg, waardoor hun nut bij de beslissing om antibiotica te initiëren mogelijk beperkt is.
 klik voor grote versie
klik voor grote versie
Tabel 1. Klinische richtlijnen voor het initiëren van antibiotica bij AECOPD
Kwaalte van de ziekte. De ernst van de ziekte is een belangrijke factor bij de beslissing om AECOPD met antibiotica te behandelen. Patiënten met een vergevorderde, onderliggende luchtwegobstructie, zoals gemeten aan de hand van de FEV1, hebben een grotere kans op een bacteriële oorzaak van AECOPD.16 Bovendien verhogen baseline klinische kenmerken, waaronder hoge leeftijd en comorbide aandoeningen, met name hart- en vaatziekten en diabetes, het risico op ernstige exacerbaties.17
Uit een meta-analyse van placebogecontroleerde trials bleek dat patiënten met ernstige exacerbaties waarschijnlijk baat hadden bij antibioticatherapie, terwijl patiënten met milde of matige exacerbaties geen reductie in behandelingsfalen of sterftecijfers hadden.18 Patiënten met acuut ademhalingsfalen die intensieve zorg en/of beademingsondersteuning (niet-invasief of invasief) nodig hebben, blijken ook baat te hebben bij antibiotica.19
De huidige klinische richtlijnen verschillen enigszins in hun aanbevelingen over wanneer antibiotica bij AECOPD moeten worden gegeven (zie tabel 1). Er zijn echter aanwijzingen dat patiënten die zich met twee of drie hoofdsymptomen presenteren, met name patiënten met meer purulent sputum, en patiënten met een ernstige ziekte (d.w.z. reeds bestaande luchtwegobstructie en/of exacerbaties waarvoor mechanische beademing nodig is) het best met antibiotica kunnen worden behandeld. Omgekeerd hebben studies aangetoond dat bij veel patiënten, met name bij patiënten met mildere exacerbaties, de symptomen verdwijnen zonder behandeling met antibiotica.11,18
 klik voor grote versie
klik voor grote versie
Tabel 2. Gerichte antibioticatherapie bij AECOPD
Antibioticakeuze bij AECOPD
Risicostratificatie. Bij patiënten die waarschijnlijk baat zullen hebben bij een antibioticumkuur, is inzicht in de relatie tussen de ernst van COPD, de gastheerrisicofactoren voor slechte resultaten en de microbiologie van het grootste belang om de klinische besluitvorming te kunnen sturen. In het verleden zijn bacteriën als Haemophilus influenzae, Streptococcus pneumoniae en Moraxella catarrhalis betrokken geweest bij de pathogenese van AECOPD.3,7 Bij patiënten met eenvoudige exacerbaties moeten antibiotica worden gebruikt die gericht zijn tegen deze ziekteverwekkers (zie tabel 2).
Patiënten met ernstigere onderliggende luchtwegobstructie (d.w.z. FEV1<50%) en risicofactoren voor slechte resultaten, met name recente ziekenhuisopname (≥2 dagen in de afgelopen 90 dagen), frequente antibioticakuren (>3 kuren in het afgelopen jaar), en ernstige exacerbaties, hebben meer kans op infectie met resistente stammen of gramnegatieve organismen.3,7 Vooral Pseudomonas aeruginosa is een toenemende bron van zorg in deze populatie. Bij patiënten met gecompliceerde exacerbaties moeten meer breed dekkende, empirische antibiotica worden gestart (zie tabel 2).
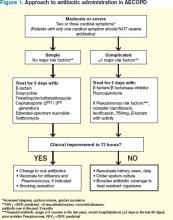
Met dit in gedachten moeten patiënten die voldoen aan de criteria voor behandeling eerst worden gestratificeerd op basis van de ernst van COPD en risicofactoren voor slechte uitkomsten voordat een beslissing over een specifiek antibioticum wordt genomen. Figuur 1 schetst een aanbevolen aanpak voor het toedienen van antibiotica bij AECOPD. Bij de optimale keuze van antibiotica moet rekening worden gehouden met de kosteneffectiviteit, lokale patronen van antibioticaresistentie, weefselpenetratie, therapietrouw van de patiënt en het risico van ongewenste voorvallen zoals diarree.
 klik voor grote versie
klik voor grote versie
Figuur 1. Aanpak van de toediening van antibiotica bij AECOPD
Vergelijkende effectiviteit. De huidige behandelingsrichtlijnen geven geen voorkeur voor het gebruik van een bepaald antibioticum bij eenvoudige AECOPD.3,4,5,6 Aangezien selectieve druk echter heeft geleid tot in vitro resistentie tegen antibiotica die traditioneel als eerstelijns werden beschouwd (bv. doxycycline, trimethoprim/sulfamethoxazol, amoxicilline), is het gebruik van tweedelijnsantibiotica (bv. fluorochinolonen, macroliden, cefalosporinen, β-lactam/ β-lactamaseremmers) toegenomen. Bijgevolg hebben verschillende studies de doeltreffendheid van verschillende antimicrobiële regimes vergeleken.
Een meta-analyse vond dat tweedelijnsantibiotica, in vergelijking met eerstelijnsmiddelen, een grotere klinische verbetering gaven aan patiënten met AECOPD, zonder significante verschillen in mortaliteit, microbiologische eradicatie, of incidentie van bijwerkingen.20 Een andere meta-analyse vergeleek trials die alleen macroliden, chinolonen en amoxicilline-clavulanaat onderzochten en vond geen verschil in termen van klinische effectiviteit op korte termijn; er waren echter zwakke aanwijzingen dat chinolonen geassocieerd waren met een beter microbiologisch succes en minder recidieven van AECOPD.21 Fluorochinolonen hebben de voorkeur bij gecompliceerde gevallen van AECOPD, waarbij het risico op enterobacteriaceae en Pseudomonas-soorten groter is.3,7
Antibioticaduur
De duur van antibioticatherapie bij AECOPD is uitgebreid bestudeerd, waarbij gerandomiseerde gecontroleerde onderzoeken consequent geen extra voordeel aantoonden van kuren die langer duurden dan vijf dagen. Eén meta-analyse van 21 studies vond vergelijkbare klinische en microbiologische genezingspercentages bij patiënten die waren gerandomiseerd naar een antibioticakuur van ≤5 dagen versus >5 dagen.22 Een subgroepanalyse van de trials die verschillende duur van hetzelfde antibioticum evalueerden, toonde ook geen verschil in klinische effectiviteit aan, en deze bevinding werd bevestigd in een aparte meta-analyse.22,23
Voordelen van kortere antibioticakuren zijn onder andere een betere therapietrouw en minder resistentie. De gebruikelijke duur van de antibioticakuur is drie tot zeven dagen, afhankelijk van de respons op de therapie.3
Terug naar de casus
Aangezien de patiënt geen significante comorbiditeiten of risicofactoren heeft, en voldoet aan de criteria voor een eenvoudige Anthonisen type I exacerbatie (toegenomen dyspneu, sputum, en sputum purulentie), wordt bij opname gestart met antibiotische therapie met trimethoprim/sulfamethoxazol, naast de eerder gestarte behandelingen met steroïden en bronchodilatoren. De klinische toestand van de patiënt verbetert en hij wordt op ziekenhuisdag 3 ontslagen met een recept om een vijfdaagse antibioticakuur te voltooien.
Bottom Line
Antibioticatherapie is effectief bij geselecteerde AECOPD-patiënten, met maximale voordelen wanneer de beslissing om te behandelen gebaseerd is op een zorgvuldige overweging van de karakteristieke klinische symptomen en de ernst van de ziekte. De keuze en duur van de antibiotica moeten de waarschijnlijke bacteriële oorzaken en de huidige richtlijnen volgen.
Dr. Cunningham is assistent-professor interne geneeskunde en academisch hospitalist op de afdeling ziekenhuisgeneeskunde aan de Vanderbilt University School of Medicine in Nashville, Tenn. Dr. LaBrin is assistent-professor interne geneeskunde en kindergeneeskunde en academisch ziekenhuisarts aan Vanderbilt. Dr. Markley is klinisch instructeur en academisch hospitalist aan Vanderbilt.
- Donaldson GC, Wedzicha JA. COPD exacerbaties: 1. Epidemiologie. Thorax. 2006;61:164-168.
- National Heart, Lung, and Blood Institute. 2009 NHLBI Morbidity and Mortality Chartbook. Website van het National Heart, Lung, and Blood Institute. Beschikbaar op: http://www.nhlbi.nih.gov/resources/docs/cht-book.htm Accessed Oct. 10, 2011.
- Global Initiative for Chronic Obstructive Lung Disease (GOLD). Wereldwijde strategie voor de diagnose, het beheer en de preventie van chronische obstructieve longaandoeningen. Global Initiative for Chronic Obstructive Lung Disease (GOLD) website. Beschikbaar op: www.goldcopd.org/guidelines-resources.html Accessed Oct. 10, 2011.
- Celli BR, MacNee W, Agusti A, et al. Standards for the diagnosis and treatment of patients with COPD: a summary of the ATS/ERS position paper. Eur Resp J. 2004;23:932-946.
- National Clinical Guideline Centre. Chronic obstructive pulmonary disease: management of chronic obstructive pulmonary disease in adults in primary and secondary care. Website van het National Institute for Health and Clinical Excellence. Beschikbaar op: http://guidance.nice.org.uk/CG101/Guidance/pdf/English. Accessed Oct. 10, 2011.
- O’Donnell DE, Aaron S, Bourbeau J, et al. Canadian Thoracic Society recommendations for management of chronic obstructive pulmonary disease-2007 update. Can Respir J. 2007;14(Suppl B):5B-32B.
- Sethi S, Murphy TF. Infection in the pathogenesis and course of chronic obstructive pulmonary disease. N Engl J Med. 2008;359:2355-2565.
- Quon BS, Qi Gan W, Sin DD. Hedendaagse behandeling van acute exacerbaties van COPD: een systematische review en metaanalyse. Chest. 2008;133:756-766.
- Rothberg MB, Pekow PS, Lahti M, Brody O, Skiest DJ, Lindenauer PK. Antibioticatherapy and treatment failure in patients hospitalized for acute exacerbations of chronic obstructive pulmonary disease. JAMA. 2010;303:2035-2042.
- Roede BM, Bresser P, Bindels PJE, et al. Antibioticabehandeling is geassocieerd met verminderd risico van latere exacerbatie bij obstructieve longziekte: een historische populatiegebaseerde cohortstudie. Thorax. 2008;63:968-973.
- Anthonisen NR, Manfreda J, Warren CP, Hershfield ES, Harding GKM, Nelson NA. Antibioticatherapie bij exacerbaties van chronisch obstructieve longziekte. Ann Intern Med. 1987;106:196-204.
- Stockley RA, O’Brien C, Pye A, Hill SL. Relationship of sputum color to nature and outpatient management of acute exacerbations of COPD. Chest. 2000;117:1638-1645.
- Rosell A, Monso E, Soler N, et al. Microbiologic determinants of exacerbation in chronic obstructive pulmonary disease. Arch Intern Med. 2005; 165:891-897.
- Stolz D, Christ-Crain M, Bingisser R, et al. Antibioticabehandeling van exacerbaties van COPD: a randomized, controlled trial comparing procalcitonin-guidance with standard therapy. Chest. 2007;131:9-19.
- Daniels JMA, Schoorl M, Snijders D, et al. Procalcitonin vs C-reactive protein as predictive markers of response to antibiotic therapy in acute exacerbations of COPD. Chest. 2010;138:1108-1015.
- Miravitlles M, Espinosa C, Fernandez-Laso E, Martos JA, Maldonado JA, Gallego M. Relationship between bacterial flora in sputum and functional impairment in patients with acute exacerbations of COPD. Chest. 1999;116:40-46.
- Patil SP, Krishnan JA, Lechtzin N, Diette GB. In-hospital mortality following acute exacerbations of chronic obstructive pulmonary disease. Arch Intern Med. 2003;163:1180-1186.
- Puhan MA, Vollenweider D, Latshang T, Steurer J, Steurer-Stey C. Exacerbaties van chronisch obstructieve longziekte: wanneer zijn antibiotica geïndiceerd? Een systematisch overzicht. Resp Res. 2007;8:30-40.
- Nouira S, Marghli S, Belghith M, Besbes L, Elatrous S, Abroug F. Once daily ofloxacin in chronic obstructive pulmonary disease exerbation requiring mechanical ventilation: a randomized placebo-controlled trial. Lancet. 2001;358:2020-2025.
- Dimopoulos G, Siempos II, Korbila IP, Manta KG, Falagas ME. Comparison of first-line with second-line antibiotics for acute exacerbations of chronic bronchitis: a metaanalysis of randomized controlled trials. Chest. 2007;132:447-455.
- Siempos II, Dimopoulos G, Korbila IP, Manta KG, Falagas ME. Macroliden, quinolonen en amoxicilline/clavulanaat voor chronische bronchitis: een meta-analyse. Eur Resp J. 2007;29:1127-1137.
- El-Moussaoui, Roede BM, Speelman P, Bresser P, Prins JM, Bossuyt PMM. Short-course antibiotic treatment in acute exacerbations of chronic bronchitis and COPD: a meta-analysis of double-blind studies. Thorax. 2008;63:415-422.
- Falagas ME, Avgeri SG, Matthaiou DK, Dimopoulos G, Siempos II. Short- versus long-duration antimicrobial treatment for exacerbations of chronic bronchitis: a meta-analysis. J Antimicrob Chemother. 2008;62:442-450.
