Dear Editor:
Peritonitis is the principal cause of peritoneal dialysis (PD) catheter loss and the primary reason why patients switch from PD to hemodialysis1. Powoduje zgon u 6% pacjentów, zwłaszcza gdy jest wywołane przez Staphylococcus aureus, drobnoustroje jelitowe i grzyby2.
Krytyczne znaczenie ma szybkie rozpoczęcie podawania antybiotyków, które powinno być rozpoczęte natychmiast po zauważeniu mętnego wypływu, nawet bez potwierdzenia liczby komórek w laboratorium3. Wytyczne zalecają empiryczne leczenie skojarzone wankomycyną lub cefalosporyną z aminoglikozydem lub cefalosporyną trzeciej generacji3.
Chemiczne zapalenie otrzewnej, opisywane jako zapalenie otrzewnej wywołane czynnikiem niezakaźnym (takim jak antybiotyki i roztwory do dializ), jest rzadszym stanem.
Chemiczne zapalenie otrzewnej wywołane wankomycyną opisano po raz pierwszy w 1984 roku4 , a w 80-90 dekadzie odnotowano blisko 90 podobnych przypadków5,6. Od tego czasu nie odnotowano żadnego innego przypadku.
Ikodekstrynowe zapalenie otrzewnej po raz pierwszy opisano w 1999 roku7, ale częstość jego występowania nie jest jasna. W 2002 r. w Europie wystąpiło ognisko epidemiczne, związane z zanieczyszczeniem roztworu8. Zgłoszono niewiele przypadków po ulepszeniu procesu wytwarzania, wszystkie związane z „uczuleniem” w tym okresie lub z innymi zanieczyszczeniami8.
Zgłosiliśmy przypadek chemicznego zapalenia otrzewnej u pacjenta leczonego ikodekstryną i dootrzewnowo wankomycyną, w którym wankomycyna wydaje się być czynnikiem sprawczym.
34-letni mężczyzna, z niewydolnością nerek wtórną do nefropatii cukrzycowej, był w PD od 2006 roku. Ikodekstryna została wprowadzona rok po rozpoczęciu PD. W kolejnych latach nie stwierdzono epizodów zapalenia otrzewnej.
W 2009 roku zgłosił się do szpitala z łagodnym bólem brzucha z czterogodzinną ewolucją. Nie miał innych objawów, w miejscu wyjścia nie było objawów zapalnych, a wypływ był przejrzysty. Analiza płynu ujawniła 26 komórek/µl (tabela 1), radiografia jamy brzusznej i USG były prawidłowe.
Podano dootrzewnowo wankomycynę (2 g co 5 dni) i ceftazydym (1 g co dzień) i wypisano pacjenta, utrzymując ikodekstrynę.
Następnego dnia powrócił z mętnym płynem (tabela 1). Utrzymano to samo leczenie i mętny wypływ ustąpił w ciągu dwóch kolejnych dni.
W piątej dobie pacjent był bezobjawowy i zgłosił się na drugie podanie wankomycyny. Później w tym samym dniu ponownie pojawiły się bóle brzucha i mętny wyciek (tabela 1).
PD zawieszono i rozpoczęto hemodializę. Przełączono wankomycynę i ceftazydym na drogę dożylną i utrzymano dodatkową dobową dawkę ceftazydymu dootrzewnowego (500 mg). Stan chorego stał się bezobjawowy, a mętny wypływ ustąpił w ciągu kolejnych dwóch dni. Wszystkie posiewy, w tym na grzyby i Mycobacterium tuberculosis, były jałowe.
W 9. dobie ponownie zastosowano PD (z ikodekstryną), a w 10. dobie podano dootrzewnowo wankomycynę. Po podaniu wankomycyny ponownie pojawił się mętny wypływ. W 12. dniu był bezobjawowy i odbarczony (tabela 1).
Trzy miesiące później pozostaje bezobjawowy, z zachowaną ultrafiltracją i czystym wypływem.
Pacjenci z zapaleniem otrzewnej zwykle prezentują się z mętnym płynem i bólem brzucha. Leukocyty w wypływie przekraczające 100/ml (z 50% komórek wielojądrzastych) wskazują na obecność stanu zapalnego, którego najbardziej prawdopodobną przyczyną jest infekcyjne zapalenie otrzewnej3. Jednak w krótkim czasie pobytu leukocyty mogą nie osiągać 100/ml3, a zapalenie otrzewnej może objawiać się bólem brzucha i brakiem mętnego wypływu3.
W naszym pacjencie wykluczono inne przyczyny bólu brzucha, takie jak zapalenie żołądka i jelit, zapalenie trzustki, zapalenie wyrostka robaczkowego lub pneumoperitoneum i rozpoczęto leczenie empiryczne infekcyjnego zapalenia otrzewnej. Mętny wypływ obecny w następnym dniu został przyjęty jako późna ekspresja zapalenia otrzewnej w płynie o dłuższym czasie przebywania.
Ból brzucha i mętny wypływ pojawiły się ponownie po drugim podaniu wankomycyny i został on przyjęty z podejrzeniem opornego na leczenie zapalenia otrzewnej. W przypadku potwierdzenia tego podejrzenia należało usunąć cewnik otrzewnowy, a pacjenta przestawić na hemodializę9. U pacjenta nie obserwowano jednak typowego rozwoju opornego na leczenie infekcyjnego zapalenia otrzewnej i wykluczono inne przyczyny mętnego wypływu, takie jak hemoperitoneum, nowotwór złośliwy, wypływ eozynofilowy i chylosomowy10. Chemiczne zapalenie otrzewnej związane z ikodekstryną lub wankomycyną pozostało prawdopodobnym rozpoznaniem5,6.
Ikodekstrynowe zapalenie otrzewnej wydaje się być spowodowane zanieczyszczeniem roztworu peptydoglikanami uwolnionymi z bakterii (Alicylobacillus acidocaldarius) podczas procesu produkcyjnego8. Usprawnienie procesu zmniejszyło częstość występowania z najwyższego poziomu 0,912% w 2002 r. do 0,013% w 2003 r.8.
Pacjenci zgłaszają się z łagodnym bólem brzucha i mętnym wypływem, bez odbicia, gorączki lub wysypki11,12. Ilość leukocytów w wypływie waha się od 100 do 6000/µl11,13, z przewagą jednojądrzastych11. Hodowla jest zawsze jałowa11.
Opóźnienie pomiędzy rozpoczęciem stosowania ikodekstryny a wystąpieniem pierwszych objawów waha się od kilku godzin do kilku lat7,12. Przebieg kliniczny jest pofałdowany, z przerywanym bólem i zmętnieniem dializatu po każdym zamieszkaniu z ikodekstryną, bez odpowiedzi na antybiotyki12. Zaprzestanie podawania ikodekstryny prowadzi do złagodzenia objawów i normalizacji leukocytów w ciągu 24-48 godzin, ale nawrót jest niezmiennie wywoływany po ponownej próbie12.
U naszego pacjenta nie wykryto ani czasowego związku z podawaniem ikodekstryny, ani nie odnotowano nawrotu po ponownej próbie.
Czasowy związek z podawaniem wankomycyny poparł diagnozę chemicznego zapalenia otrzewnej wywołanego wankomycyną.
Kliniczna prezentacja waha się od samego mętnego wypływu do silnego bólu brzucha i gorączki. Zaczyna się 2-12 godzin po podaniu wankomycyny5 i ustępuje w ciągu 3 do 4 dni po zawieszeniu6. Przeważają neutrofile, a liczba eozynofilów waha się od 0-10%5,6.
Zgłoszona częstość występowania zapalenia otrzewnej wywołanego przez wankomycynę (Vancoled®) wynosiła 23%6. Mechanizm leżący u podstaw tego zjawiska jest nieznany5,14. Niektórzy pacjenci doświadczają nawrotu bólu brzucha i (lub) podwyższenia leukocytów w płynie po ponownej ekspozycji na wankomycynę podawaną dootrzewnowo, bez skarg, gdy podawana jest dożylnie lub dootrzewnowo wankomycyna innego producenta5. Wyniki te potwierdzają podejrzenie, że zapalenie nie jest w pełni spowodowane samą wankomycyną, ale innym składnikiem jej preparatu14,15.
Wankomycyna zawiera 5,2-16,7% zanieczyszczeń, w zależności zarówno od marki, jak i partii preparatu14,15. Zróżnicowana ilość zanieczyszczeń obecnych w poszczególnych partiach może decydować o wystąpieniu reakcji zapalnej6.
Nie odnotowano żadnych przypadków śmiertelnych6,7 i nie zaleca się żadnego leczenia, z wyjątkiem wstrzymania podawania środka wywołującego zakażenie7.
Chociaż klinicznie jest to łagodna postać, która ustępuje samoistnie, długoterminowe następstwa są nadal nieznane. Ponadto może być mylona z infekcyjnym zapaleniem otrzewnej i prowadzić do niepotrzebnego przepisywania antybiotyków lub do usunięcia cewnika i zawieszenia PD7.
W ciągu ostatnich 15 lat nie odnotowano żadnego przypadku zapalenia otrzewnej wywołanego wankomycyną, być może z powodu postępującej poprawy oczyszczania. W czasach, gdy coraz częściej stosowane są preparaty generyczne, nasz przypadek może zwrócić uwagę lekarzy na obecność tego zapomnianego działania niepożądanego.
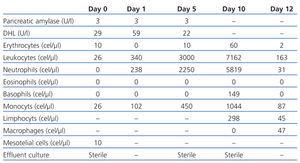
Tabela 1. Ewolucja charakterystyki ścieków
.
