Związki jonowe, kowalencyjne (proste cząsteczkowe i olbrzymie atomowe) i metaliczne mają różne właściwości. Dlatego, aby zaklasyfikować substancję do któregoś z tych związków, należy przeprowadzić serię testów/doświadczeń, aby dowiedzieć się, jakie ma ona właściwości. Zwróć uwagę na poniższą tabelę:
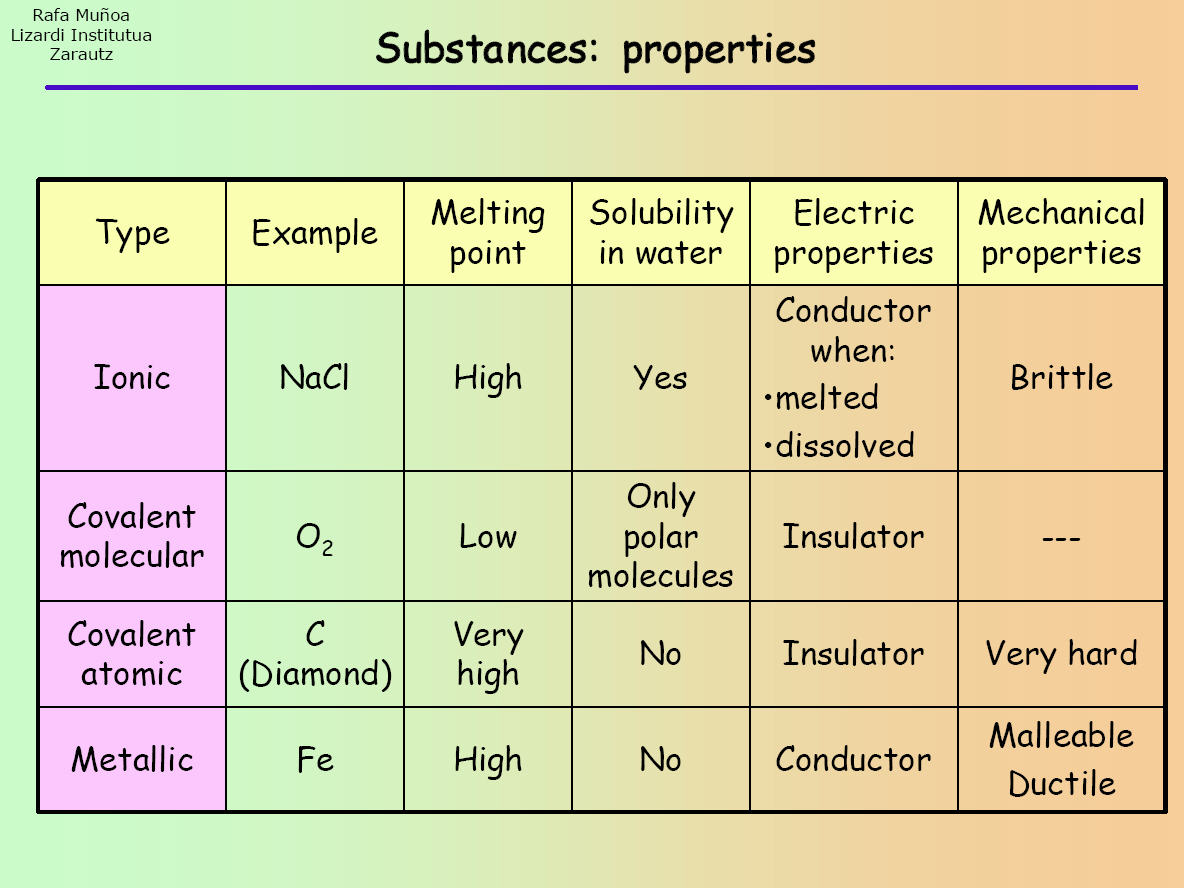
Po przeprowadzeniu eksperymentu, wyniki, które otrzymasz mogą być porównane z tymi w tabeli, aby zidentyfikować jakiego rodzaju związkiem jest dana substancja.
Po pierwsze, próbka nieznanej substancji może być umieszczona w probówce i umieszczona nad płomieniem. Robi się to w celu określenia temperatury topnienia. Jeśli substancja topi się, to prawdopodobnie jest to kowalencyjnie prosta substancja molekularna (jak pokazano w tabeli). Jednakże, jeśli nie występuje topnienie, substancja może być jonowa, kowalencyjna olbrzymia atomowa lub metaliczna.
Właśnie dlatego musimy przeprowadzić więcej niż jedną próbę na nieznanej substancji, ponieważ niektóre kategorie związków mają podobne właściwości (na przykład związki jonowe i związki kowalencyjne mają wysokie temperatury topnienia).
Następnie możesz spróbować rozpuścić trochę substancji w wodzie (lub innym polarnym rozpuszczalniku). Jeśli rozpuszcza się, to może być albo jonowy lub kowalencyjny prosty związek molekularny. Twoje wyniki z poprzedniego testu i następnego pomogą zawęzić wyniki do tylko jednego typu związku.
Następnie możesz podłączyć próbkę do obwodu takiego jak pokazany poniżej, aby sprawdzić, czy przewodzi ona prąd elektryczny.
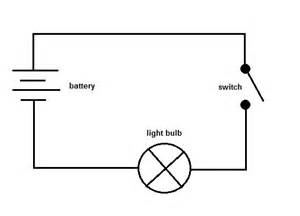
Możesz zastąpić przełącznik próbką. Jeśli żarówka zaświeci, to jest to przewodnik, a jeśli nie, to jest to nieprzewodnik.
Więc, na przykład, na koniec tego doświadczenia, jeśli próbka pozostała nie stopiona, rozpuściła się w wodzie i przewodziła prąd elektryczny, to jest to związek jonowy.
Wszystkie te obserwacje mogą być dalej wyjaśnione przez zbadanie wiązań i międzycząsteczkowych sił przyciągania, które utrzymują składniki związku razem.
.
