Bakteria Gram-ujemna z rodziny Enterobacteriaceae, Serratia marcescens jest organizmem znanym z wywoływania bakteriemii, zapalenia płuc, zakażenia dróg moczowych, zapalenia wsierdzia, zapalenia opon mózgowych i septycznego zapalenia stawów.1 Opisywano również nietypowe przypadki zapalenia tkanki łącznej i martwiczego zapalenia powięzi (NF) wywołane przez S marcescens.2,3 Jednostkę tę opisywano początkowo u pacjentów z obniżoną odpornością i bez niej.4 Opisywano również przypadki zarówno środowiskowe, jak i szpitalne.3
Raport przypadku
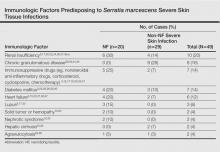
68-letnia chorobliwie otyła kobieta z wysokim ciśnieniem krwi, cukrzycą, przewlekłą niewydolnością nerek, przewlekłą niewydolnością żylną i obrzękiem limfatycznym lewej nogi została skierowana do naszego oddziału ratunkowego. U pacjentki wystąpił ból i rumień obwodowy z licznymi ropniami podudzia lewego trwający od 2 tygodni. W wywiadzie nie odnotowano urazu, owrzodzenia, wstrzyknięcia ani ugryzienia przez zwierzę. W momencie prezentacji pacjentka nie miała gorączki, a parametry życiowe były w normie. Rozpoczęto leczenie empiryczne doustną amoksycyliną (6 g dziennie) i amoksycyliną-klawulanianem (375 mg dziennie). Czterdzieści osiem godzin później stan zapalny, ból i ropień pogorszyły się (ryc. 1A). Badania laboratoryjne wykazały zwiększoną liczbę białych krwinek (15,9×109⁄L z 86% neutrofilów) i zwiększone stężenie białka C-reaktywnego (322 mg/L). Serologia ludzkiego wirusa niedoboru odporności była ujemna. Aspiracja igłowa ropnia dała wynik S marcescens. Druga aspiracja potwierdziła obecność tego samego organizmu, dzikiego typu S marcescens, który był oporny na amoksycylinę i kwas klawulanowy, cefalosporyny pierwszej generacji i tobramycynę, ale wrażliwy na piperacylinę, cefalosporyny trzeciej generacji, amikacynę, cyprofloksacynę i kotrimoksazol. Rozpoczęto dożylne podawanie cefepimu, cefalosporyny III generacji. W ciągu kolejnych 48 godzin u chorego rozwinęła się ciężka sepsa z dezorientacją, ostrą niewydolnością nerek (kreatynina: 231 µmol/L vs 138 µmol/L na poziomie wyjściowym 9,11,35-38,40; ropnie, gumma lub zmiany podobne do pyoderma gangrenosum związane z przewlekłą chorobą ziarniniakową w dzieciństwie 29,44,45; bolesne guzki z wtórnymi ropniami 31-34,46; ostre pęcherzowe zapalenie tkanki łącznej 8,10,30; wtórne zakażenia owrzodzeń 35,40; ropnie u immunokompetentnego pacjenta 41; martwicze owrzodzenie skóry 36). Często dotyczyły kończyn dolnych (NF, n=13; non-NF, n=16). Podłożem immunosupresji było 14 przypadków NF i 17 przypadków non-NF. Predysponujące czynniki immunologiczne zestawiono w tabeli. Miejscowe czynniki ryzyka, w tym przewlekły obrzęk nogi, uraz, rana chirurgiczna, wstrzyknięcie wypełniacza i owrzodzenie, były często opisywane w przypadkach NF i nie-NF,16,20,26-28,31,32,34,35,37,38,40,46 włączając nasz przypadek. Operacja była konieczna w 19 przypadkach NF i w 7 przypadkach non-NF. NF wywołane przez Serratia marcescens prowadziło do większej śmiertelności (n=12) niż przypadki bez NF (n=1). Inne niezbyt ciężkie manifestacje kliniczne zakażenia S marcescens opisywane w literaturze obejmowały rozsiane wykwity grudkowe z zakażeniem ludzkim wirusem niedoboru odporności42 i zapalenie mieszków włosowych pnia.43 U naszego pacjenta występowało wiele czynników ryzyka, w tym przewlekłe obrzęki, cukrzyca, przewlekła niewydolność nerek i przewlekła niewydolność żylna. Potencjalna obecność ropni i tkanki martwiczej utrudnia penetrację antybiotyków w miejscu zakażenia, a w związku z wysoką śmiertelnością S marcescens cellulitis należy systematycznie rozważać jak najwcześniejsze leczenie chirurgiczne.