![]()
Osoby korzystające z technologii wspomagających mogą nie być w stanie uzyskać pełnego dostępu do informacji zawartych w tym pliku. Aby uzyskać pomoc, prosimy o wysłanie wiadomości e-mail na adres: [email protected]. W temacie wiadomości e-mail należy wpisać 508 Accommodation oraz tytuł raportu.
![]() PDF
PDF
The Advisory Committee on Immunization Practices (ACIP) annually reviews the recommended Adult Immunization Schedule to ensure that the schedule reflects current recommendations for the use of licensed vaccines. W czerwcu 2005 roku ACIP zatwierdził schemat szczepień ochronnych dla dorosłych na okres od października 2005 roku do września 2006 roku. Ten schemat został również zatwierdzony przez American Academy of Family Physicians i American College of Obstetricians and Gynecologists.
Zmiany w schemacie na październik 2005–wrzesień 2006
Szablon na lata 2005-2006 różni się od poprzedniego schematu w następujący sposób:
- Szczepionki wymienione w schemacie opartym na wieku (ryc. 1) są wyświetlane w taki sposób, aby można było odróżnić szczepionki zalecane do rutynowego stosowania od szczepionek zalecanych dla osób dorosłych z pewnymi wskaźnikami ryzyka (podobnie jak w schemacie szczepień ochronnych dla dzieci). Ilustruje to zarówno schemat kolorów, jak i linia przerywana.
- Żółte paski („Dla wszystkich osób w tej grupie”) i zielone paski („Dla osób nieposiadających dokumentacji szczepienia lub dowodów choroby”) z poprzedniego schematu zostały połączone w jeden żółty pasek, który teraz brzmi: „Dla wszystkich osób w tej kategorii, które spełniają wymagania wiekowe i którym brakuje dowodów odporności (np,
- Fioletowy pasek został zmieniony z „Dla osób z grupy ryzyka (np. ze wskazaniami medycznymi/ekspozycyjnymi)” na „Zalecane, jeśli występuje jakiś inny czynnik ryzyka (np. na podstawie wskazań medycznych, zawodowych, stylu życia lub innych)”. Dodano fioletowy pasek do kolumn grup wiekowych 50–64 lata i >65 lat dla szczepionki przeciwko odrze, śwince, różyczce (MMR).
- Kolumna „Cukrzyca, choroba serca, przewlekła choroba płuc lub przewlekła choroba wątroby, w tym przewlekły alkoholizm” została zamieniona z kolumną „Wrodzony niedobór odporności, białaczka, chłoniak, uogólniona choroba nowotworowa, terapia środkami alkilującymi, antymetabolitami, wyciek płynu mózgowo-rdzeniowego, napromienianie lub duże ilości kortykosteroidów” na schemacie medycznym/inne wskazania (ryc. 2), tak aby przeciwwskazania do szczepionek MMR i przeciwko ospie wietrznej znajdowały się teraz obok siebie.
- Wiersz dotyczący szczepionki przeciwko ospie wietrznej został przesunięty w górę na obu rycinach (tj, (tzn. bezpośrednio po szczepionce MMR), ponieważ szczepionka ta jest obecnie powszechnie zalecana w niektórych grupach wiekowych.
- Szczepionka przeciwko meningokokom została dodana do schematu postępowania w medycynie/innych wskazaniach (ryc. 2). Zmieniono przypis, aby uwzględnić ostatnio opublikowane zalecenia ACIP dotyczące tej szczepionki (1).
- Przypis dotyczący tężca i błonicy (#1) został przeredagowany.
- Przypis dotyczący ospy wietrznej (#3) został przeredagowany zgodnie z zaleceniami ACIP przyjętymi w czerwcu 2005 roku.
- Przypis dotyczący grypy (#4) zmieniono, dodając najnowszy stan dużego ryzyka: schorzenia nerwowo-mięśniowe upośledzające czynność układu oddechowego (2).
- Dodano 10. przypis dotyczący szczepienia przeciwko Haemophilus influenzae typu b w populacjach dużego ryzyka (tj, osoby z asplenią, białaczką i zakażeniem ludzkim wirusem niedoboru odporności).
Schemat szczepień ochronnych dla dorosłych jest dostępny w języku angielskim i hiszpańskim pod adresem http://www.cdc.gov/nip/recs/adult-schedule.htm. Ogólne informacje na temat szczepień ochronnych dla dorosłych, w tym zalecenia dotyczące szczepień osób zakażonych wirusem HIV i cierpiących na inne schorzenia immunosupresyjne, są dostępne w stanowych i lokalnych departamentach zdrowia oraz w National Immunization Program pod adresem http://www.cdc.gov/nip. Oświadczenia informacyjne dotyczące szczepionek są dostępne pod adresem http://www.cdc.gov/nip/publications/vis. Oświadczenia ACIP dotyczące każdej zalecanej szczepionki można przeglądać, pobierać i drukować ze strony internetowej Krajowego Programu Szczepień Ochronnych (National Immunization Program) pod adresem http://www.cdc.gov/nip/publications/acip-list.htm. Instrukcje dotyczące zgłaszania zdarzeń niepożądanych do Vaccine Adverse Event Reporting System są dostępne pod adresem http://www.vaers.hhs.gov lub telefonicznie, 800-822-7967.
- CDC. Prevention and control of meningococcal disease: recommendations of the Advisory Committee for Immunization Practices (ACIP). MMWR 2005;54(No. RR-7).
- CDC. Prevention and control of influenza: recommendations of the Advisory Committee for Immunization Practices (ACIP). MMWR 2005;54(No. RR-8).
Rysunek 1
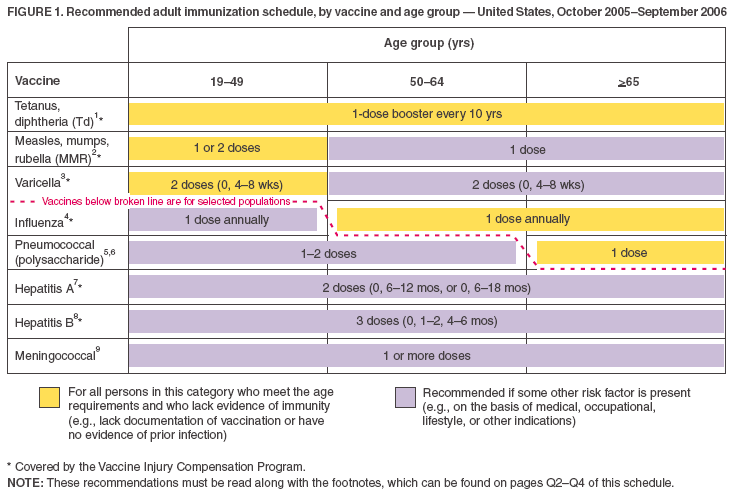
Powrót do góry.
Rysunek 2

Powrót do góry.
1. Szczepienie przeciwko tężcowi i błonicy (Td). Dorośli z niepewnym wywiadem dotyczącym kompletnej serii szczepień podstawowych szczepionkami zawierającymi toksoid błoniczy i tężcowy powinni otrzymać serię podstawową z użyciem skojarzonego toksoidu Td. Pierwsza seria dla dorosłych składa się z 3 dawek; pierwsze 2 dawki podawane są w odstępie co najmniej 4 tygodni, a trzecia dawka 6-12 miesięcy po drugiej. Jeżeli osoba otrzymała serię pierwotną i ostatnie szczepienie otrzymała >10 lat wcześniej, należy podać 1 dawkę. Należy zapoznać się z zaleceniami ACIP dotyczącymi podawania Td jako profilaktyki w leczeniu ran (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). American College of Physicians Task Force on Adult Immunization popiera drugą opcję stosowania Td u dorosłych: pojedyncza dawka przypominająca Td w wieku 50 lat dla osób, które ukończyły pełną serię pediatryczną, w tym dawkę przypominającą dla nastolatków/młodych dorosłych. Nowo zarejestrowana szczepionka przeciwko tężcowi, błonicy i krztuścowi jest dostępna dla dorosłych. Zalecenia ACIP dotyczące jej stosowania zostaną opublikowane.
2. Szczepienie przeciwko ospie wietrznej, śwince i różyczce (MMR). Składowa odry: dorośli urodzeni przed 1957 r. mogą być uznani za odpornych na odrę. Dorośli urodzeni w trakcie lub po 1957 roku powinni otrzymać >1 dawkę MMR, chyba że mają przeciwwskazania lekarskie, dokumentację >1 dawki, wywiad w kierunku odry oparty na rozpoznaniu lekarza lub laboratoryjne dowody odporności. Drugą dawkę MMR zaleca się osobom dorosłym, które: 1) były ostatnio narażone na zachorowanie na odrę lub przebywały w ognisku epidemicznym; 2) były wcześniej szczepione szczepionką zabitą przeciwko odrze; 3) były szczepione szczepionką przeciwko odrze nieznanego typu w latach 1963-1967; 4) są uczniami szkół policealnych; 5) pracują w placówkach służby zdrowia; 6) planują podróż zagraniczną. Nie podawać MMR lub innych szczepionek zawierających odrę osobom zakażonym HIV z ciężką immunosupresją. Komponenta świnki: 1 dawka szczepionki MMR powinna stanowić wystarczającą ochronę dla osób urodzonych w 1957 r. lub później, które nie chorowały na świnkę w wywiadzie na podstawie diagnozy lekarza lub u których brak jest laboratoryjnych dowodów odporności. Komponenta różyczkowa: należy podać 1 dawkę szczepionki MMR kobietom, u których wywiad dotyczący szczepień przeciwko różyczce jest niewiarygodny lub u których brak jest laboratoryjnych dowodów odporności. U kobiet w wieku rozrodczym, niezależnie od roku urodzenia, rutynowo określać odporność na różyczkę i doradzać kobietom w zakresie zespołu różyczki wrodzonej. Nie należy szczepić kobiet, które są w ciąży lub które mogą zajść w ciążę w ciągu 4 tygodni od otrzymania szczepionki. Kobiety, które nie mają dowodów na odporność, powinny otrzymać szczepionkę MMR po zakończeniu lub przerwaniu ciąży i przed wypisem z placówki opieki zdrowotnej.
3. Szczepienie przeciwko ospie wietrznej. Szczepienie przeciwko ospie wietrznej jest zalecane wszystkim dorosłym bez dowodów odporności na ospę wietrzną. Szczególną uwagę należy zwrócić na osoby, które 1) mają bliski kontakt z osobami z grupy dużego ryzyka ciężkiego przebiegu choroby (pracownicy służby zdrowia i osoby z rodzin z obniżoną odpornością) lub 2) są w grupie dużego ryzyka narażenia na zakażenie lub przeniesienia zakażenia (np. nauczyciele małych dzieci, pracownicy placówek opieki nad dziećmi, mieszkańcy i pracownicy instytucji, w tym zakładów poprawczych, studenci szkół wyższych, personel wojskowy, młodzież i dorośli mieszkający w gospodarstwach domowych z dziećmi, kobiety w wieku rozrodczym niebędące w ciąży oraz osoby podróżujące za granicę). Dowody odporności na ospę wietrzną u dorosłych obejmują którekolwiek z poniższych: 1) udokumentowane szczepienie przeciwko ospie wietrznej odpowiednie do wieku (tj. otrzymanie 1 dawki przed ukończeniem 13. roku życia lub otrzymanie 2 dawek po ukończeniu 13. roku życia); 2) urodzenie się w Stanach Zjednoczonych przed 1966 r. lub przebycie choroby wywołanej wirusem ospy wietrznej przed 1966 r. w przypadku osób urodzonych poza Stanami Zjednoczonymi; 3) przebycie choroby wywołanej wirusem ospy wietrznej przed 1966 r. w przypadku osób urodzonych poza Stanami Zjednoczonymi.urodzonych w Stanach Zjednoczonych; 3) przebycie ospy wietrznej w wywiadzie na podstawie rozpoznania przez pracownika służby zdrowia lub zgłoszenia przez rodziców albo przez samego siebie typowego zachorowania na ospę wietrzną dla osób urodzonych w latach 1966-1997 (w przypadku pacjenta zgłaszającego przebycie nietypowego, łagodnego przypadku, pracownicy służby zdrowia powinni poszukiwać powiązania epidemiologicznego z typowym przypadkiem ospy wietrznej lub dowodów potwierdzenia laboratoryjnego, jeżeli zostało ono wykonane w czasie ostrego zachorowania); 4) przebycie półpaśca w wywiadzie na podstawie rozpoznania przez pracownika służby zdrowia; lub 5) laboratoryjne potwierdzenie odporności. Nie należy szczepić kobiet, które są w ciąży lub które mogą zajść w ciążę w ciągu 4 tygodni od podania szczepionki. Nie należy szczepić kobiet w ciąży lub kobiet, które mogą zajść w ciążę w ciągu 4 tygodni od podania szczepionki. Kobiety, u których nie ma dowodów odporności, powinny otrzymać dawkę 1 szczepionki przeciw ospie wietrznej po zakończeniu lub przerwaniu ciąży i przed wypisem z placówki służby zdrowia. Dawka 2 powinna być podana 4–8 tygodni po podaniu dawki 1.
4. Szczepienie przeciwko grypie. Wskazania medyczne: przewlekłe zaburzenia układu sercowo-naczyniowego lub płucnego, w tym astma; przewlekłe choroby metaboliczne, w tym cukrzyca, zaburzenia czynności nerek, hemoglobinopatie lub immunosupresja (w tym immunosupresja spowodowana lekami lub HIV); wszelkie stany (np., zaburzenia funkcji poznawczych, uszkodzenie rdzenia kręgowego, zaburzenia drgawkowe lub inne zaburzenia nerwowo-mięśniowe), które upośledzają czynność układu oddechowego lub przetwarzanie wydzielin z dróg oddechowych, lub które mogą zwiększać ryzyko aspiracji; oraz ciąża w sezonie grypowym. Nie istnieją dane dotyczące ryzyka wystąpienia ciężkiej lub powikłanej choroby grypowej u osób z asplenią, jednak grypa jest czynnikiem ryzyka wtórnych zakażeń bakteryjnych, które mogą powodować ciężką chorobę u osób z asplenią. Wskazania zawodowe: pracownicy służby zdrowia oraz pracownicy placówek opieki długoterminowej i domów pomocy społecznej. Inne wskazania: mieszkańcy domów opieki i innych placówek opieki długoterminowej i wspomaganej; osoby, które mogą przenosić grypę na osoby z grupy wysokiego ryzyka (tj. osoby pozostające w kontakcie domowym i opiekunowie dzieci w wieku 0-23 miesięcy lub osoby w każdym wieku ze schorzeniami wysokiego ryzyka) oraz wszyscy, którzy chcą się zaszczepić. W przypadku zdrowych, nieciężarnych osób w wieku 5–49 lat bez stanów wysokiego ryzyka, które nie są osobami mającymi kontakt z osobami z ciężkimi zaburzeniami odporności przebywającymi w oddziałach specjalnych, zamiast szczepionki inaktywowanej można podać donosowo szczepionkę przeciw grypie (FluMist®).
5. Polisacharydowa szczepionka przeciwko pneumokokom. Wskazania medyczne: przewlekłe zaburzenia układu płucnego (z wyłączeniem astmy); choroby układu krążenia; cukrzyca; przewlekłe choroby wątroby, w tym choroby wątroby w wyniku nadużywania alkoholu (np. marskość wątroby); przewlekła niewydolność nerek lub zespół nerczycowy; czynnościowa lub anatomiczna asplenia (np., choroba sierpowatokrwinkowa lub splenektomia); stany immunosupresyjne (np. wrodzony niedobór odporności, zakażenie wirusem HIV, białaczka, chłoniak, szpiczak mnogi, choroba Hodgkina, uogólniona choroba nowotworowa lub przeszczep narządu lub szpiku kostnego); chemioterapia z zastosowaniem środków alkilujących, antymetabolitów lub długotrwale podawanych kortykosteroidów; implanty ślimakowe. Inne wskazania: Tubylcy Alaski i niektóre populacje Indian amerykańskich; mieszkańcy domów opieki i innych placówek opieki długoterminowej.
6. Ponowne szczepienie polisacharydową szczepionką pneumokokową. Jednorazowe ponowne szczepienie po 5 latach dla osób z przewlekłą niewydolnością nerek lub zespołem nefrytycznym; funkcjonalną lub anatomiczną asplenią (np. choroba sierpowatokrwinkowa lub splenektomia); stanami immunosupresyjnymi (np., wrodzony niedobór odporności, zakażenie wirusem HIV, białaczka, chłoniak, szpiczak mnogi, choroba Hodgkina, uogólniona choroba nowotworowa lub przeszczepienie narządu lub szpiku kostnego); lub chemioterapia środkami alkilującymi, antymetabolitami lub długotrwale stosowanymi kortykosteroidami o działaniu ogólnoustrojowym. Dla osób w wieku >65 lat, jednorazowe ponowne szczepienie, jeżeli były szczepione >5 lat wcześniej i w momencie szczepienia pierwotnego były w wieku <65 lat.
7. Szczepienie przeciwko wirusowemu zapaleniu wątroby typu A. Wskazania medyczne: osoby z zaburzeniami czynnika krzepnięcia lub przewlekłą chorobą wątroby. Wskazania behawioralne: mężczyźni uprawiający seks z mężczyznami lub osoby zażywające nielegalne narkotyki. Wskazania zawodowe: Osoby pracujące z naczelnymi zakażonymi wirusem zapalenia wątroby typu A (HAV) lub z HAV w warunkach laboratorium badawczego. Inne wskazania: osoby podróżujące lub pracujące w krajach o wysokiej lub średniej endemiczności wirusowego zapalenia wątroby typu A (lista krajów, patrzhttp://www.cdc.gov/travel/diseases.htm#hepa), a także wszystkie osoby chcące uzyskać odporność. Aktualne szczepionki powinny być podawane w serii 2-dawkowej w wieku 0 i 6-12 miesięcy lub 0 i 6-18 miesięcy. Jeżeli stosuje się skojarzoną szczepionkę przeciwko WZW typu A i WZW typu B, należy podać 3 dawki w 0, 1 i 6 miesiącu życia.
8. Szczepienie przeciwko WZW typu B. Wskazania medyczne: pacjenci poddawani hemodializie (stosować specjalny preparat lub dwie dawki 20µg/mL) lub pacjenci otrzymujący koncentraty czynników krzepnięcia. Wskazania zawodowe: pracownicy służby zdrowia i pracownicy służb bezpieczeństwa publicznego, którzy są narażeni na kontakt z krwią w miejscu pracy oraz osoby uczące się w szkołach medycznych, stomatologicznych, pielęgniarskich, technikach laboratoryjnych i innych pokrewnych zawodach medycznych. Wskazania behawioralne: osoby przyjmujące narkotyki w zastrzykach; osoby mające więcej niż jednego partnera seksualnego w ciągu ostatnich 6 miesięcy; osoby z niedawno nabytą chorobą przenoszoną drogą płciową (STD); oraz mężczyźni uprawiający seks z mężczyznami. Inne wskazania: kontakty domowe i partnerzy seksualni osób z przewlekłym zakażeniem wirusem zapalenia wątroby typu B (HBV); klienci i członkowie personelu instytucji dla osób z zaburzeniami rozwojowymi; wszyscy klienci klinik STD; więźniowie zakładów karnych; oraz osoby podróżujące za granicę, które będą przebywać w krajach o dużej lub średniej częstości występowania przewlekłego zakażenia HBV przez ponad 6 miesięcy (lista krajów, patrz http://www.cdc.gov/travel/diseases.htm#hepa).
9. Szczepienia przeciwko meningokokom. Wskazania medyczne: dorośli z anatomiczną lub czynnościową asplenią lub terminalnym niedoborem składowych dopełniacza. Inne wskazania: studenci pierwszego roku studiów mieszkający w akademikach; mikrobiolodzy rutynowo narażeni na kontakt z izolatami Neisseria meningitidis; rekruci wojskowi; oraz osoby podróżujące do krajów, w których choroba meningokokowa ma charakter hiperendemiczny lub epidemiczny (np. „pas zapalenia opon mózgowych” w Afryce Subsaharyjskiej w porze suchej), szczególnie jeśli kontakt z miejscową ludnością będzie długotrwały. Szczepienie jest wymagane przez rząd Arabii Saudyjskiej dla wszystkich podróżujących do Mekki podczas corocznego hadżdżu. Szczepionka skoniugowana przeciwko meningokokom jest preferowana u osób dorosłych spełniających którekolwiek z powyższych wskazań, w wieku <55 lat, chociaż polisacharydowa szczepionka przeciwko meningokokom (MPSV4) jest dopuszczalną alternatywą. Ponowne szczepienie po 5 latach może być wskazane u osób dorosłych uprzednio zaszczepionych MPSV4, które pozostają w grupie wysokiego ryzyka zakażenia (np. osoby zamieszkujące obszary, na których choroba ma charakter epidemiczny).
10. Wybrane stany chorobowe, w których może być stosowana szczepionka przeciwko Haemophilus influenzae typu b (Hib). Szczepionki skoniugowane Hib są dopuszczone do stosowania u dzieci w wieku 6–71 miesięcy. Nie ma danych dotyczących skuteczności, na podstawie których można by sformułować zalecenie dotyczące stosowania szczepionki Hib u starszych dzieci i dorosłych z przewlekłymi schorzeniami związanymi ze zwiększonym ryzykiem zachorowania na Hib. Jednak badania sugerują dobrą immunogenność u pacjentów z chorobą sierpowatokrwinkową, białaczką, zakażeniem HIV lub po splenektomii; podawanie szczepionki tym pacjentom nie jest przeciwwskazane.
Zalecany schemat szczepień ochronnych dla dorosłych został zatwierdzony przez Advisory Committee on Immunization Practices, American College of Obstetricians and Gynecologists oraz American Academy of Family Physicians. Standardowy format przypisów MMWR został zmodyfikowany do publikacji tego schematu.
Sugerowane cytowanie: Centers for Disease Control and Prevention. Recommended Adult Immunization Schedule—United States, October 2005–September 2006. MMWR 2005;54:Q1–Q4.
Ten schemat wskazuje zalecane grupy wiekowe i wskazania medyczne do rutynowego podawania obecnie licencjonowanych szczepionek dla osób w wieku >19 lat. Licencjonowane szczepionki skojarzone mogą być stosowane w każdym przypadku, gdy którykolwiek składnik szczepionki skojarzonej jest wskazany i gdy pozostałe składniki szczepionki nie są przeciwwskazane. W celu uzyskania szczegółowych zaleceń należy zapoznać się z ulotkami dołączonymi do opakowań szczepionek przez producentów oraz z pełnymi oświadczeniami ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Zgłaszanie wszystkich istotnych klinicznie odczynów poszczepiennych do systemu zgłaszania niepożądanych odczynów poszczepiennych (Vaccine Adverse Event Reporting System, VAERS). Formularze zgłoszeniowe i instrukcje dotyczące składania raportu VAERS są dostępne pod numerem telefonu 800-822-7967 lub w witrynie internetowej VAERS pod adresem http://www.vaers.hhs.gov.
Informacje dotyczące sposobu składania roszczenia w ramach Vaccine Injury Compensation Program są dostępne pod adresem http://www.hrsa.gov/osp/vicp lub pod numerem telefonu 800-338-2382. Aby złożyć wniosek o odszkodowanie za szkodę wyrządzoną przez szczepionkę, należy skontaktować się z U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, tel. 202-357-6400.
Dodatkowe informacje na temat szczepionek wymienionych powyżej oraz przeciwwskazań do szczepienia są również dostępne pod adresem http://www.cdc.gov/nip lub w Centrum Kontaktowym CDC-INFO pod numerem 800-CDC-INFO (232-4636) w języku angielskim i hiszpańskim, 24 godziny na dobę, 7 dni w tygodniu.
Użycie nazw handlowych i źródeł komercyjnych ma na celu wyłącznie identyfikację i nie oznacza poparcia przez U.S. Department of Health and Human Services.Odniesienia do stron internetowych nie należących do CDC są dostarczane jako usługa dla czytelników MMWR i nie stanowią ani nie implikują poparcia tych organizacji lub ich programów przez CDC lub U.S. Department of Health and Human Services. CDC nie jest odpowiedzialne za treść stron, które można znaleźć na tych stronach. Adresy URL podane w MMWR były aktualne w dniu publikacji.
Zastrzeżenie Wszystkie wersje HTML artykułów MMWR są elektronicznymi konwersjami z tekstu ASCII na HTML. W wyniku tej konwersji mogły powstać błędy w tłumaczeniu znaków lub błędy formatu w wersji HTML. Użytkownicy nie powinni polegać na tym dokumencie HTML, lecz są odsyłani do elektronicznej wersji PDF i/lub oryginalnej wersji papierowej MMWR, gdzie znajdują się oficjalne teksty, ryciny i tabele. Oryginalny egzemplarz papierowy tego wydania można otrzymać od Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371; telefon: (202) 512-1800. W celu uzyskania aktualnych cen należy skontaktować się z GPO.
**Pytania lub wiadomości dotyczące błędów w formatowaniu należy kierować na adres [email protected].
Data ostatniego przeglądu: 10/13/2005
