Autor: Amelie Stahlbuhk
back to Sulfate
Ten artykuł zostanie wkrótce udostępniony.
Abstract
Przedstawione zostaną różne uwodnione formy siarczanu magnezu oraz zachowanie dotyczące rozpuszczalności i higroskopijności.
Formy uwodnione
Kieseryt MgSO4-H2O
Sandryt MgSO4-2H2O
Starkeyit MgSO4-4H2O
Pentahydryt MgSO4-5H2O
Heksahydryt MgSO4-6H2O
Epsomit MgSO4-7H2O
Meridianiit MgSO4-11H2O
Rozpuszczalność
Jak wynika z tabeli 1, różne uwodnione formy siarczanu magnezu są solami łatwo rozpuszczalnymi, co prowadzi do dużej mobilności soli w materiałach porowatych.
| Forma uwodniona | Rozpuszczalność w 20°C |
| Kieseryt | 5.60 |
| Starkeyite | 5.04 |
| Pentahydryt | 4.40 |
| Hexahydryt | 3.61 |
| Epsomit | 2,84 |
Dzięki różnym formom uwodnionym siarczanu magnezu o stabilnych i meta stabilnych stanach równowagi, diagram rozpuszczalności układu MgSO4-H2O zawiera więcej informacji niż diagramy soli z mniejszą ilością form uwodnionych lub również bez form uwodnionych. Dzięki zależności rozpuszczalności od temperatury możliwe jest, że zmianom temperatury towarzyszy hydratacja lub dehydratacja danej fazy.
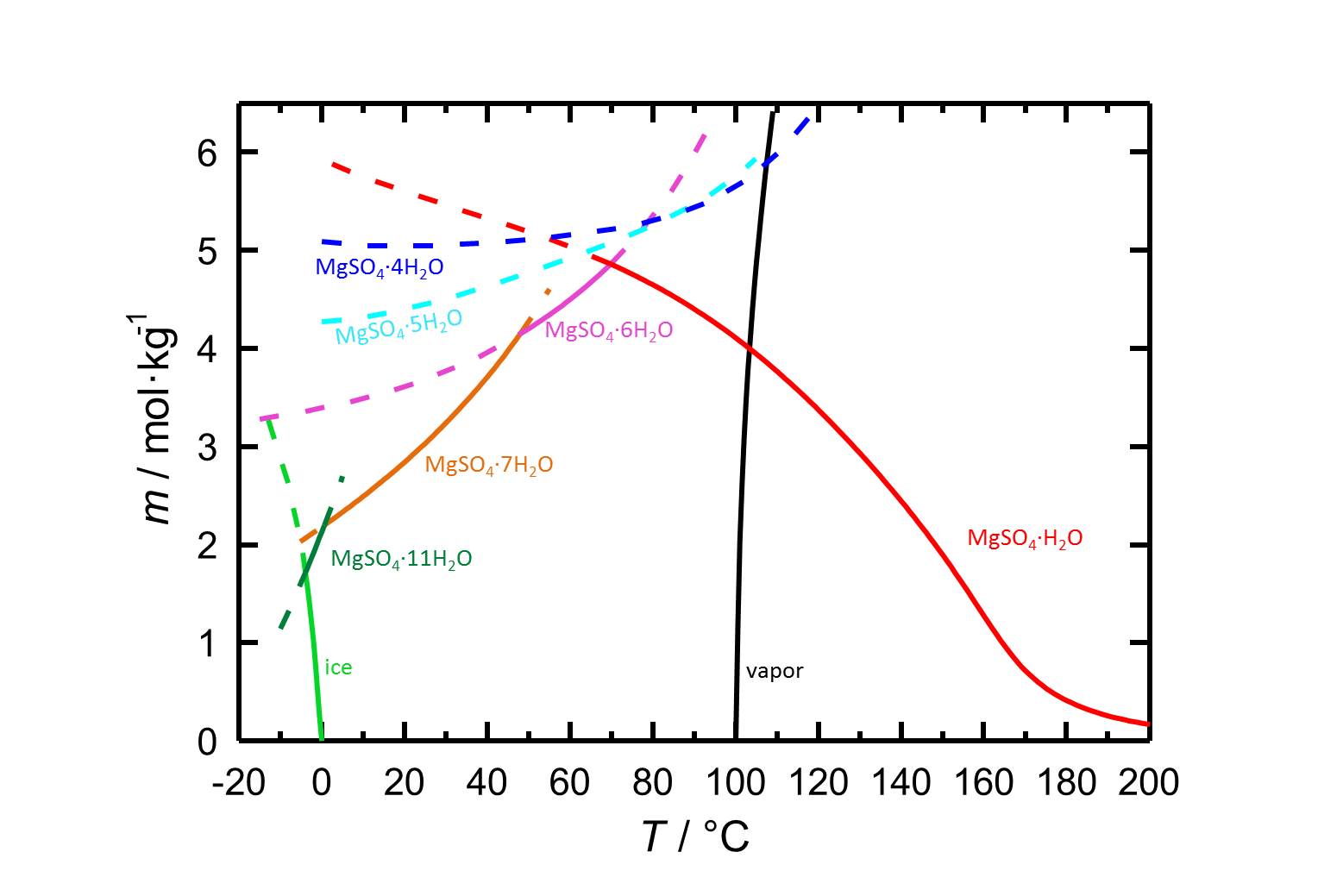
Autor: Steiger, Michael; Linnow, Kirsten; Ehrhardt, Dorothee; Rohde, Mandy
 .
.Hygroskopijność
W układzie MgSO4-H2O zmiany temperatury lub wilgotności względnej mogą prowadzić do procesów hydratacji/dehydratacji lub delikwatacji/krystalizacji. W temperaturze 20 °C epsomit jest obecną fazą krystaliczną, gdy wilgotność względna jest niższa od wilgotności delikatesowej wynoszącej 91,3 %. Gdy wilgotność względna osiąga wartości poniżej 47 %, następuje odwodnienie do niższych poziomów uwodnionych, co przedstawiają krzywe wilgotności równowagowych na rysunku 2.
| Przejście fazowe | Delikwencja lub wilgotność równowagowa w 20°C |
| Roztwór Epsomitu | 91,3 % |
| Epsomit-Heksahydryt | 46.6 % |
| Epsomite-Kieserite | 46.7 % |
| Hexahydrite-Starkeyite | 39.1 % |
z towarzyszącą hydratacją lub dehydratacją danej fazy.
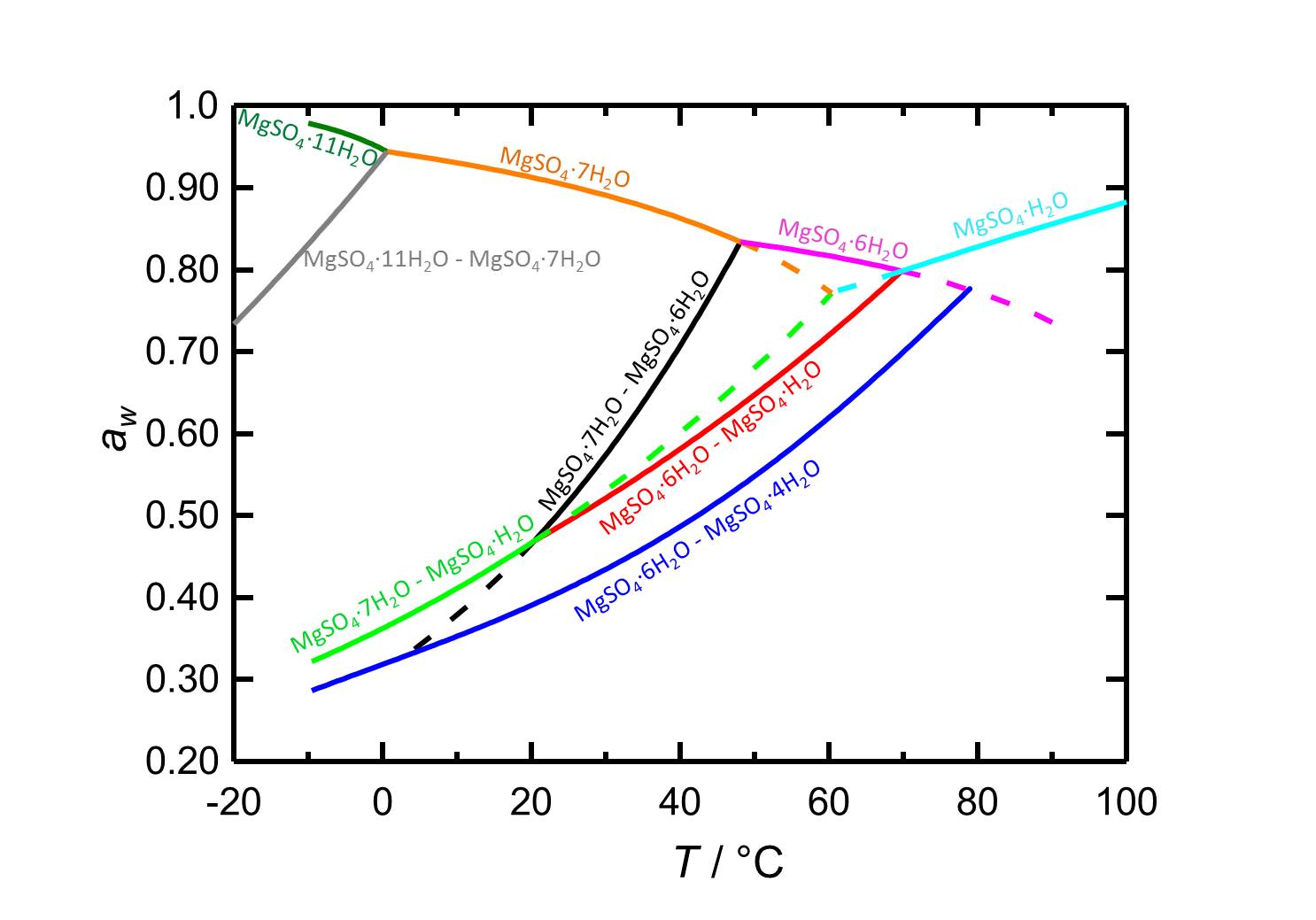
Author: Steiger, Michael; Linnow, Kirsten; Ehrhardt, Dorothee; Rohde, Mandy
 .
.W zakresie temperatur od -10 do 100 °C wilgotności delikatesowe obecnych form uwodnionych (w zależności od temperatury) leżą zawsze powyżej 80 % r.h., sole te nie należą więc do soli higroskopijnych.
Weblinks
Literatura
| Mainusch, Nils (2001): Erstellung einer Materialsammlung zur qualitativen Bestimmung bauschädlicher Salze für Fachleute der Restaurierung, Diplomarbeit, HAWK Hochschule für angewandte Wissenschaft und Kunst Hildesheim/Holzminden/Göttingen, file:Diplomarbeit Nils Mainusch.pdf |   |
|
| Stark, Jochen; Stürmer, Sylvia (1996): Bauschädliche Salze, Bauhaus-Univ. Weimar |  |
|
| Steiger, Michael; Linnow, Kirsten; Ehrhardt, Dorothee; Rohde, Mandy (2011): Decomposition reactions of magnesium sulfate hydrates and phase equilibria in the MgSO4-H2O and Na+-Mg2+-Cl–SO42–H2O systems with implications for Mars. Geochimica et Cosmochimica Act, 75 (12), 3600-3626, 10.1016/j.gca.2011.03.038, |  |
.
