![]()
Persoanele care utilizează tehnologii de asistență s-ar putea să nu poată accesa pe deplin informațiile din acest fișier. Pentru asistență, vă rugăm să trimiteți un e-mail la: [email protected]. Scrieți 508 Cazare și titlul raportului în linia de subiect a e-mailului.
![]() PDF
PDF
Comitetul Consultativ pentru Practici de Imunizare (Advisory Committee on Immunization Practices – ACIP) revizuiește anual calendarul recomandat de imunizare a adulților pentru a se asigura că acesta reflectă recomandările actuale de utilizare a vaccinurilor autorizate. În iunie 2005, ACIP a aprobat Calendarul de imunizare a adulților pentru perioada octombrie 2005-septembrie 2006. Acest calendar a fost aprobat, de asemenea, de Academia Americană a Medicilor de Familie și de Colegiul American al Obstetricienilor și Ginecologilor.
Schimbări în calendarul pentru octombrie 2005–septembrie 2006
Scadenarul 2005–2006 diferă de calendarul anterior după cum urmează:
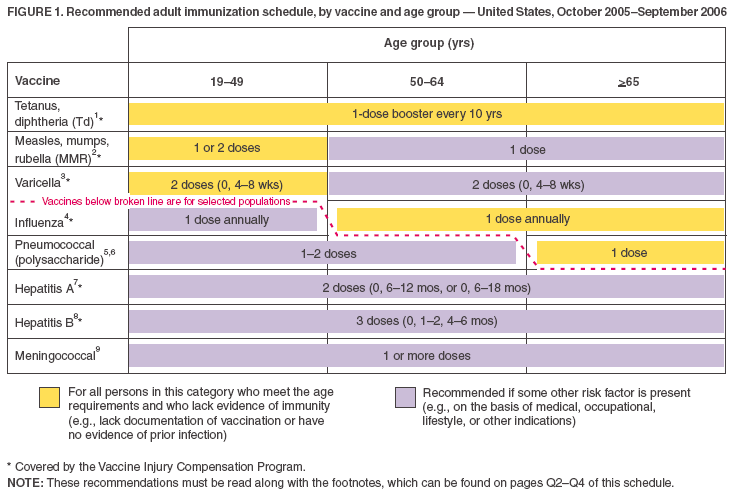
- Vaccinurile enumerate în calendarul bazat pe vârstă (Figura 1) sunt afișate astfel încât vaccinurile recomandate pentru utilizare de rutină să poată fi diferențiate de cele recomandate pentru adulții cu anumiți indicatori de risc (similar cu calendarul de imunizare pentru copii). Acest lucru este ilustrat atât prin schema de culori, cât și prin linia întreruptă.
- Barele galbene („Pentru toate persoanele din această grupă”) și cele verzi („Pentru persoanele care nu au documente de vaccinare sau dovezi de boală”) din calendarul anterior au fost fuzionate într-o singură bară galbenă, care acum sună astfel: „Pentru toate persoanele din această categorie care îndeplinesc cerințele de vârstă și care nu au dovezi de imunitate (de ex, nu au documente de vaccinare sau nu au nicio dovadă de infecție anterioară).”
- Bara mov a fost schimbată din „Pentru persoanele cu risc (de exemplu, cu indicații medicale/de expunere)” în „Recomandat în cazul în care este prezent un alt factor de risc (de exemplu, pe baza unor indicații medicale, profesionale, de stil de viață sau de altă natură)”. Bara mov a fost adăugată la coloanele pentru grupele de vârstă 50–64 ani și >65 ani pentru vaccinul împotriva rujeolei, oreionului, rubeolei (ROR).
- Coloana „Diabet, boală cardiacă, boală pulmonară cronică sau boală hepatică cronică, inclusiv alcoolism cronic” a fost transpusă cu coloana „Imunodeficiență congenitală, leucemie, limfom, malignitate generalizată, terapie cu agenți alchilanți, antimetaboliți, scurgeri de lichid cefalorahidian, radiații sau cantități mari de corticosteroizi” de pe tabelul cu indicații medicale/alte indicații (figura 2), astfel încât contraindicațiile pentru vaccinurile ROR și varicelă sunt acum alăturate.
- Rândul pentru vaccinul împotriva varicelei a fost mutat în sus pe ambele figuri (de ex, la imediat după vaccinul ROR) deoarece vaccinul este acum recomandat universal pentru anumite grupe de vârstă.
- Vaccinul antimeningococic a fost adăugat la schema de indicații medicale/alte indicații (figura 2). Nota de subsol a fost revizuită pentru a încorpora recomandările ACIP recent publicate pentru acest vaccin (1).
- Nota de subsol privind tetanosul și difteria (#1) a fost reformulată.
- Nota de subsol privind varicela (#3) a fost reformulată în conformitate cu recomandările ACIP adoptate în iunie 2005.
- Nota de subsol privind gripa (#4) a fost revizuită pentru a adăuga cea mai nouă afecțiune cu risc ridicat: afecțiuni neuromusculare care compromit funcția respiratorie (2).
- A fost adăugată o a 10-a notă de subsol privind vaccinarea împotriva Haemophilus influenzae tip b pentru populațiile cu risc ridicat (de ex, persoanele cu asplenie, leucemie și infecție cu virusul imunodeficienței umane).
Schema de imunizare pentru adulți este disponibilă în engleză și spaniolă la http://www.cdc.gov/nip/recs/adult-schedule.htm. Informații generale despre imunizarea adulților, inclusiv recomandări privind vaccinarea persoanelor cu HIV și alte afecțiuni imunosupresoare, sunt disponibile la departamentele de sănătate de stat și locale și la Programul Național de Imunizare la http://www.cdc.gov/nip. Declarațiile de informare privind vaccinurile sunt disponibile la http://www.cdc.gov/nip/publications/vis. Declarațiile ACIP pentru fiecare vaccin recomandat pot fi vizualizate, descărcate și tipărite de pe site-ul web al Programului Național de Imunizare la http://www.cdc.gov/nip/publications/acip-list.htm. Instrucțiunile pentru raportarea evenimentelor adverse la Sistemul de raportare a evenimentelor adverse la vaccinuri sunt disponibile la http://www.vaers.hhs.gov sau la numărul de telefon 800-822-7967.
- CDC. Prevenirea și controlul bolii meningococice: recomandări ale Comitetului consultativ pentru practici de imunizare (ACIP). MMWR 2005;54(nr. RR-7).
- CDC. Prevenirea și controlul gripei: recomandări ale Comitetului consultativ pentru practici de imunizare (ACIP). MMWR 2005;54(Nr. RR-8).
Figura 1
Întoarceți la începutul paginii.
Figura 2

Întoarceți la începutul paginii.
Aprobat de Comitetul consultativ privind practicile de imunizare, de Colegiul American de Obstetricieni și Ginecologi și de Academia Americană a Medicilor de Familie
1. Vaccinarea antitetanică și difterică (Td). Adulții cu antecedente incerte ale unei serii complete de vaccinare primară cu vaccinuri care conțin anatoxină difterică și tetanică trebuie să primească o serie primară folosind anatoxina Td combinată. O serie primară pentru adulți este de 3 doze; administrați primele 2 doze la cel puțin 4 săptămâni distanță între ele și a treia doză la 6-12 luni după a doua. Se administrează 1 doză dacă persoana a primit seria primară și dacă ultimul vaccin a fost primit cu >10 ani înainte. Consultați declarația ACIP pentru recomandări privind administrarea de Td ca profilaxie în tratamentul plăgilor (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). Grupul de lucru al Colegiului American al Medicilor pentru imunizarea adulților (American College of Physicians Task Force on Adult Immunization) susține o a doua opțiune pentru utilizarea Td la adulți: un singur rapel Td la vârsta de 50 de ani pentru persoanele care au efectuat seria pediatrică completă, inclusiv rapelul pentru adolescenți/adulți tineri. Un vaccin tetanic-difteric-celular-pertussis, recent autorizat, este disponibil pentru adulți. Recomandările ACIP pentru utilizarea acestuia vor fi publicate.
2. Vaccinarea împotriva rujeolei, oreionului, rubeolei (ROR). Componenta rujeolă: adulții născuți înainte de 1957 pot fi considerați imuni la rujeolă. Adulții născuți în timpul sau după 1957 trebuie să primească >1 doză de ROR, cu excepția cazului în care au o contraindicație medicală, documentația pentru >1 doză, antecedente de rujeolă bazate pe diagnosticul furnizorului de asistență medicală sau dovezi de laborator de imunitate. O a doua doză de ROR este recomandată pentru adulții care: 1) au fost recent expuși la rujeolă sau în cadrul unui focar; 2) au fost vaccinați anterior cu vaccin antirujeolic ucis; 3) au fost vaccinați cu un tip necunoscut de vaccin antirujeolic în perioada 1963–1967; 4) sunt studenți în instituții de învățământ postliceal; 5) lucrează într-o unitate de îngrijire a sănătății; sau 6) intenționează să călătorească la nivel internațional. Refuzați vaccinul ROR sau alte vaccinuri care conțin rujeolă la persoanele infectate cu HIV cu imunosupresie severă. Componenta oreion: 1 doză de vaccin ROR ar trebui să fie adecvată pentru protecția celor născuți în timpul sau după 1957 care nu au antecedente de oreion pe baza diagnosticului furnizorului de asistență medicală sau care nu au dovezi de laborator de imunitate. Componenta rubeolă: administrați 1 doză de vaccin ROR la femeile al căror istoric de vaccinare împotriva rubeolei nu este fiabil sau care nu au dovezi de laborator privind imunitatea. Pentru femeile aflate la vârsta fertilă, indiferent de anul nașterii, determinați în mod curent imunitatea la rubeolă și consiliați femeile cu privire la sindromul rubeolic congenital. Nu vaccinați femeile care sunt însărcinate sau care ar putea rămâne însărcinate în termen de 4 săptămâni de la primirea vaccinului. Femeile care nu au dovezi de imunitate trebuie să primească vaccinul ROR la terminarea sau întreruperea sarcinii și înainte de externarea din unitatea sanitară.
3. Vaccinarea împotriva varicelei. Vaccinarea împotriva varicelei este recomandată pentru toți adulții fără dovezi de imunitate la varicelă. O atenție deosebită trebuie acordată celor care 1) au contacte apropiate cu persoane cu risc ridicat de îmbolnăvire severă (lucrători din domeniul sănătății și contacte familiale ale persoanelor imunocompromise) sau 2) prezintă un risc ridicat de expunere sau de transmitere (de exemplu, profesori de copii mici; angajați din centrele de îngrijire a copiilor; rezidenți și membri ai personalului din medii instituționale, inclusiv instituții corecționale; studenți universitari; personal militar; adolescenți și adulți care locuiesc în gospodării cu copii; femei care nu sunt gravide și sunt de vârstă fertilă; și călători internaționali). Dovada imunității la varicelă la adulți include oricare dintre următoarele: 1) vaccinare antivaricelică documentată corespunzător vârstei (adică primirea unei doze înainte de vârsta de 13 ani sau primirea a 2 doze după vârsta de 13 ani); 2) născut în SUA înainte de 1966 sau antecedente de boală varicelică înainte de 1966 pentru cei care nu sunt din SUAnăscute în SUA înainte de 1966; 3) antecedente de varicelă pe baza diagnosticului furnizorului de asistență medicală sau a declarației părinților sau a autodenunțării bolii tipice de varicelă pentru persoanele născute în perioada 1966-1997 (pentru un pacient care raportează antecedente de un caz atipic, ușor, furnizorii de asistență medicală trebuie să caute fie o legătură epidemiologică cu un caz tipic de varicelă, fie dovada confirmării de laborator, dacă aceasta a fost efectuată în momentul apariției bolii acute); 4) antecedente de herpes zoster pe baza diagnosticului furnizorului de asistență medicală; sau 5) dovada de laborator a imunității. Nu vaccinați femeile care sunt însărcinate sau care ar putea rămâne însărcinate în termen de 4 săptămâni de la administrarea vaccinului. Evaluați femeile gravide pentru dovezi de imunitate la varicelă. Femeile care nu au dovezi de imunitate trebuie să primească doza 1 de vaccin antivaricelicelă la terminarea sau încheierea sarcinii și înainte de externarea din unitatea sanitară. Doza 2 trebuie să fie administrată la 4–8 săptămâni după doza 1.
4. Vaccinarea antigripală. Indicații medicale: afecțiuni cronice ale sistemului cardiovascular sau pulmonar, inclusiv astm; boli metabolice cronice, inclusiv diabet zaharat, disfuncții renale, hemoglobinopatii sau imunosupresie (inclusiv imunosupresie cauzată de medicamente sau HIV); orice afecțiune (de ex, disfuncție cognitivă, leziune a măduvei spinării, tulburare convulsivă sau altă tulburare neuromusculară) care compromite funcția respiratorie sau manipularea secrețiilor respiratorii sau care poate crește riscul de aspirație; și sarcină în timpul sezonului gripal. Nu există date privind riscul de îmbolnăvire de gripă severă sau complicată la persoanele cu asplenie; cu toate acestea, gripa este un factor de risc pentru infecțiile bacteriene secundare care pot provoca boli severe la persoanele cu asplenie. Indicații profesionale: lucrători din domeniul sănătății și angajați ai centrelor de îngrijire pe termen lung și ai locuințelor asistate. Alte indicații: rezidenții căminelor de bătrâni și ai altor centre de îngrijire pe termen lung și de asistență socială; persoanele care pot transmite gripa persoanelor cu risc ridicat (de exemplu, contacții casnici și îngrijitorii de copii cu vârste cuprinse între 0 și 23 de luni sau persoanele de toate vârstele cu afecțiuni cu risc ridicat), precum și orice persoană care dorește să fie vaccinată. Pentru persoanele sănătoase, care nu sunt gravide, cu vârste cuprinse între 5 și 49 de ani, fără afecțiuni cu risc ridicat și care nu sunt contacte ale unor persoane cu imunitate severă în unități de îngrijire specială, vaccinul antigripal administrat pe cale intranazală (FluMist®) poate fi administrat în locul vaccinului inactivat.
5. Vaccinarea pneumococică polizaharidică. Indicații medicale: afecțiuni cronice ale sistemului pulmonar (cu excepția astmului); afecțiuni cardiovasculare; diabet zaharat; afecțiuni hepatice cronice, inclusiv afecțiuni hepatice ca urmare a abuzului de alcool (de exemplu, ciroză); insuficiență renală cronică sau sindrom nefrotic; asplenie funcțională sau anatomică (de ex, siclemie sau splenectomie ); afecțiuni imunosupresoare (de exemplu, imunodeficiență congenitală, infecție HIV , leucemie, limfom, mielom multiplu, boala Hodgkin, malignitate generalizată sau transplant de organe sau de măduvă osoasă); chimioterapie cu agenți alchilanți, antimetaboliți sau corticosteroizi sistemici pe termen lung; și implanturi cohleare. Alte indicații: Nativii din Alaska și anumite populații amerindiene; rezidenți ai căminelor de bătrâni și ai altor unități de îngrijire pe termen lung.
6. Revaccinarea cu vaccin pneumocococic polizaharidic. Revaccinare o singură dată după 5 ani pentru persoanele cu insuficiență renală cronică sau sindrom nefritic; asplenie funcțională sau anatomică (de ex., boala celulelor secerătoare sau splenectomie); afecțiuni imunosupresoare (de ex, imunodeficiență congenitală, infecție HIV, leucemie, limfom, mielom multiplu, boala Hodgkin, malignitate generalizată sau transplant de organe sau de măduvă osoasă); sau chimioterapie cu agenți alchilanți, antimetaboliți sau corticosteroizi sistemici pe termen lung. Pentru persoanele cu vârsta >65 de ani, o singură revaccinare dacă au fost vaccinate >5 ani anterior și aveau vârsta <65 de ani la momentul vaccinării primare.
7. Vaccinarea împotriva hepatitei A. Indicații medicale: persoane cu tulburări ale factorilor de coagulare sau boli hepatice cronice. Indicații comportamentale: bărbați care au relații sexuale cu bărbați sau consumatori de droguri ilegale. Indicații profesionale: Persoane care lucrează cu primate infectate cu virusul hepatitei A (VHA) sau cu VHA în cadrul unui laborator de cercetare. Alte indicații: persoanele care călătoresc sau lucrează în țări cu endemicitate ridicată sau intermediară a hepatitei A (pentru lista țărilor, vezihttp://www.cdc.gov/travel/diseases.htm#hepa), precum și orice persoană care dorește să obțină imunitate. Vaccinurile actuale trebuie administrate într-o serie de 2 doze, fie la 0 și 6–12 luni, fie la 0 și 6–18 luni. Dacă se utilizează vaccinul combinat împotriva hepatitei A și hepatitei B, se administrează 3 doze la 0, 1 și 6 luni.
8. Vaccinarea împotriva hepatitei B. Indicații medicale: pacienți hemodializați (folosiți o formulă specială sau două doze de 20-µg/mL) sau pacienți care primesc concentrați de factor de coagulare. Indicații profesionale: lucrători din domeniul sănătății și lucrători din domeniul siguranței publice care sunt expuși la sânge la locul de muncă și persoane aflate în formare în școlile de medicină, stomatologie, asistență medicală, tehnologie de laborator și alte profesii conexe din domeniul sănătății. Indicații comportamentale: utilizatorii de droguri injectabile; persoanele care au avut mai mult de un partener sexual în ultimele 6 luni; persoanele care au dobândit recent o boală cu transmitere sexuală (BTS); și bărbații care fac sex cu bărbați. Alte indicații: contacții casnici și partenerii sexuali ai persoanelor cu infecție cronică cu virusul hepatitei B (VHB); clienții și membrii personalului instituțiilor pentru persoane cu handicap de dezvoltare; toți clienții clinicilor de boli cu transmitere sexuală; deținuții din penitenciare; și călătorii internaționali care se vor afla în țări cu prevalență ridicată sau intermediară a infecției cronice cu VHB pentru mai mult de 6 luni (pentru lista țărilor, vezi http://www.cdc.gov/travel/diseases.htm#hepa).
9. Vaccinarea meningococică. Indicații medicale: adulți cu asplenie anatomică sau funcțională sau deficiențe terminale ale componentelor complementului. Alte indicații: studenți din primul an de facultate care locuiesc în cămine; microbiologi care sunt expuși în mod obișnuit la izolate de Neisseria meningitidis; recruți militari; și persoanele care călătoresc sau locuiesc în țări în care boala meningococică este hiperendemică sau epidemică (de exemplu, „centura meningitei” din Africa subsahariană în timpul sezonului uscat), în special dacă contactul cu populațiile locale va fi prelungit. Vaccinarea este cerută de guvernul Arabiei Saudite pentru toți călătorii care se deplasează la Mecca în timpul Hajj-ului anual. Vaccinul conjugat meningococic este preferat pentru adulții care îndeplinesc oricare dintre indicațiile de mai sus și care au vârsta <55 de ani, deși vaccinul meningocococic polizaharidic (MPSV4) este o alternativă acceptabilă. Revaccinarea după 5 ani ar putea fi indicată pentru adulții vaccinați anterior cu MPSV4 care rămân la risc ridicat de infectare (de exemplu, persoanele care locuiesc în zone în care boala este epidemică).
10. Condiții selectate pentru care se poate utiliza vaccinul împotriva Haemophilus influenzae tip b (Hib). Vaccinurile conjugate Hib sunt autorizate pentru copiii cu vârsta cuprinsă între 6–71 luni. Nu sunt disponibile date privind eficacitatea pe care să se bazeze o recomandare privind utilizarea vaccinului Hib pentru copiii mai mari și adulții cu afecțiuni cronice asociate cu un risc crescut de îmbolnăvire cu Hib. Cu toate acestea, studiile sugerează o bună imunogenitate la pacienții care au anemie cu celule secerătoare, leucemie sau infecție cu HIV sau care au suferit splenectomii; administrarea vaccinului la acești pacienți nu este contraindicată.
Schema recomandată de imunizare a adulților a fost aprobată de Comitetul consultativ privind practicile de imunizare, de Colegiul American de Obstetricieni și Ginecologi și de Academia Americană a Medicilor de Familie. Formatul standard al notelor de subsol din MMWR a fost modificat pentru publicarea acestui calendar.
Citație sugerată: Centrele pentru Controlul și Prevenirea Bolilor. Calendarul de imunizare recomandat pentru adulți—Statele Unite, octombrie 2005–septembrie 2006. MMWR 2005;54:Q1–Q4.
Acest calendar indică grupele de vârstă și indicațiile medicale recomandate pentru administrarea de rutină a vaccinurilor licențiate în prezent pentru persoanele cu vârsta >19 ani. Vaccinurile combinate licențiate pot fi utilizate ori de câte ori oricare dintre componentele combinației este indicată și când celelalte componente ale vaccinului nu sunt contraindicate. Pentru recomandări detaliate, consultați prospectele producătorilor și declarațiile complete ale ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Raportați toate reacțiile postvaccinare semnificative din punct de vedere clinic la Sistemul de raportare a reacțiilor adverse la vaccinuri (VAERS). Formularele de raportare și instrucțiunile privind depunerea unui raport VAERS sunt disponibile prin telefon, 800-822-7967, sau de pe site-ul VAERS la http://www.vaers.hhs.gov.
Informații privind modul de depunere a unei cereri de despăgubire în cadrul Programului de compensare a leziunilor provocate de vaccinuri sunt disponibile la http://www.hrsa.gov/osp/vicp sau prin telefon, 800-338-2382. Pentru a depune o cerere de despăgubire pentru leziuni provocate de vaccinuri, contactați U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, telefon 202-357-6400.
Informații suplimentare despre vaccinurile enumerate mai sus și contraindicații pentru vaccinare sunt disponibile, de asemenea, la http://www.cdc.gov/nip sau la Centrul de contact CDC-INFO la 800-CDC-INFO (232-4636) în engleză și spaniolă, 24 de ore pe zi, 7 zile pe săptămână.
Utilizarea denumirilor comerciale și a surselor comerciale este doar pentru identificare și nu implică aprobarea de către Departamentul de Sănătate și Servicii Umane al SUA. trimiterile la site-urile non-CDC de pe Internet sunt furnizate ca un serviciu pentru cititorii MMWR și nu constituie sau implică aprobarea acestor organizații sau a programelor lor de către CDC sau Departamentul de Sănătate și Servicii Umane al SUA. CDC nu este responsabil pentru conținutul paginilor găsite pe aceste site-uri. Adresele URL listate în MMWR erau actuale la data publicării.
Disclaimer Toate versiunile HTML ale articolelor din MMWR sunt conversii electronice din text ASCII în HTML. Este posibil ca această conversie să fi dus la erori de traducere a caracterelor sau de format în versiunea HTML. Utilizatorii nu trebuie să se bazeze pe acest document HTML, ci sunt trimiși la versiunea electronică în format PDF și/sau la exemplarul original pe hârtie al MMWR pentru textul, figurile și tabelele oficiale. O copie originală pe hârtie a acestui număr poate fi obținută de la Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371; telefon: (202) 512-1800. Contactați GPO pentru prețurile curente.
**Întrebările sau mesajele referitoare la erori de formatare trebuie adresate la adresa [email protected].
Data ultimei revizuiri: 10/13/2005
