Compușii ionici, covalenți (moleculari simpli și atomici giganți) și metalici au proprietăți diferite. Prin urmare, pentru a clasifica o substanță ca fiind unul dintre acești compuși, trebuie efectuate o serie de teste/experimente pentru a afla ce proprietăți are. Observați tabelul următor:
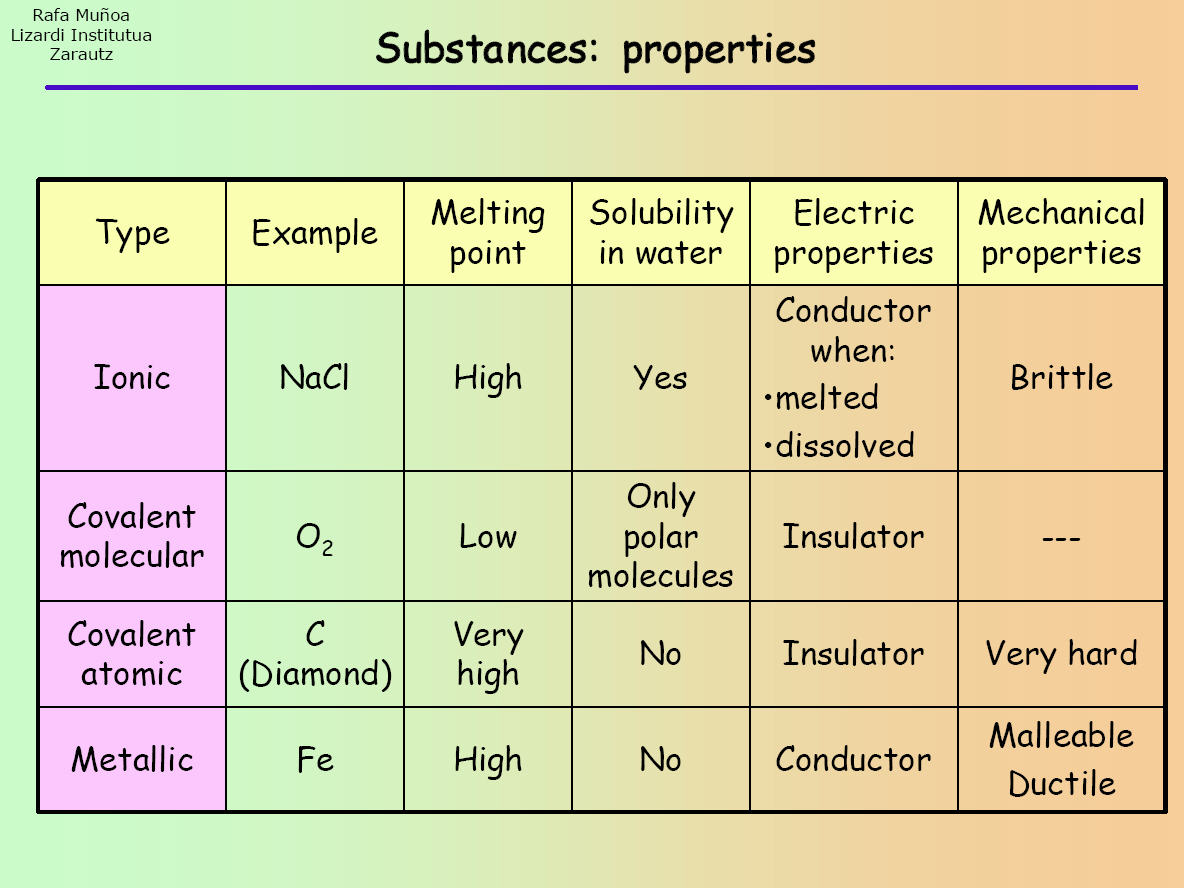
După ce experimentul a fost efectuat, rezultatele pe care le obțineți pot fi comparate cu cele din tabel pentru a identifica ce fel de compus este substanța.
Primul rând, o mostră din substanța necunoscută poate fi plasată într-o eprubetă și pusă deasupra unei flăcări. Acest lucru se face pentru a determina punctul de topire. Dacă substanța se topește, atunci probabil că este o substanță moleculară simplă covalentă (așa cum se arată în tabel). Cu toate acestea, dacă nu are loc nicio topire, substanța poate fi fie ionică, fie atomică gigantică covalentă, fie metalică.
De fapt, acesta este motivul pentru care trebuie să efectuăm mai multe teste asupra substanței necunoscute, deoarece unele categorii de compuși au proprietăți similare (de exemplu, compușii ionici și compușii covalenți au amândoi puncte de topire ridicate).
În continuare, puteți încerca să dizolvați o parte din substanță în apă (sau într-un alt solvent polar). Dacă se dizolvă, atunci poate fi fie un compus molecular simplu ionic, fie unul covalent. Rezultatele dvs. de la testul anterior și de la următorul vă vor ajuta să restrângeți rezultatele la un singur tip de compus.
În continuare, puteți conecta proba la un circuit precum cel prezentat mai jos pentru a vedea dacă aceasta conduce un curent electric.
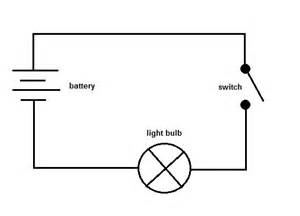
Puteți înlocui întrerupătorul cu proba. Dacă becul se aprinde, atunci este un conductor, iar dacă nu, atunci este un neconductor.
Deci, de exemplu, la sfârșitul acestui experiment, dacă proba a rămas netopită, s-a dizolvat în apă și a condus un curent electric, atunci este un compus ionic.
Toate aceste observații pot fi explicate mai departe prin examinarea legăturilor și a forțelor de atracție intermoleculare care țin împreună componentele unui compus.
.
