Pentru ca moleculele de medicament să ajungă în creier trebuie să treacă bariera defensivă hemato-encefalică. Anthony King investighează modul în care chimiștii se infiltrează în fortăreața creierului
Activitățile obișnuite, cum ar fi exercițiile fizice sau mâncatul, ne pot modifica destul de dramatic compoziția sângelui. Potasiul din sânge poate crește, de exemplu, și pot exista schimbări semnificative în conținutul său de lipide și aminoacizi. Metaboliții toxici pentru celulele nervoase pot intra chiar și în fluxul sanguin.
Bariera hemato-encefalică, din fericire, blochează flotilarea sau jetsam-ul din sângele nostru să traverseze în creierul nostru. Acest lucru este crucial, deoarece semnalizarea neuronilor din creier se bazează pe semnale electrice și pe semnale chimice fine, care necesită un micro-mediu reglat cu precizie, iar acesta poate fi ușor perturbat de moleculele care intră din sânge.
‘Nu vrei ca centrul tău de comunicare să fie perturbat de lucruri care se pot întâmpla în stomac, în intestin sau în alte zone ale corpului. Vrei ca acesta să fie stabil și să funcționeze perfect, fie că dormi, fie că ești urmărit de un tigru”, explică Lester Drewes de la Universitatea Minnesota din Duluth, SUA. Bariera hemato-encefalică, sau BBB, este formată din celulele endoteliale care căptușesc vasele de sânge din creier. Aceste celule-fortăreață sunt lipite foarte strâns între ele și, spre deosebire de alte organe și țesuturi, nu există fisuri între ele pentru ca materialele transportate prin sânge să se scurgă în țesutul cerebral.

Sursa: © HAMISH KIDD
Bariera hemato-encefalică protejează peste 400 de mile de capilare și vase de sânge din creier
Această apărare este o adevărată bătaie de cap pentru tratarea tumorilor cerebrale și a altor afecțiuni neurologice. Medicamentele, tratate ca molecule străine de către BBB, nu reușesc să treacă. De fapt, peste 95 % dintre medicamente nu prezintă o activitate utilă în creier și multe dintre ele prezintă o slabă penetrare a BHE. O proporție mare de medicamente cu molecule mari nu traversează, ceea ce cuprinde toate produsele biotehnologiei: proteine recombinante, anticorpi monoclonali și medicamente cu interferență ARN.
William Pardridge, director al Laboratorului de cercetare a barierei hemato-encefalice de la Universitatea California Los Angeles, SUA, consideră că misiunea de dezvoltare a medicamentelor pentru boala Alzheimer și alte afecțiuni cerebrale a avut de suferit prin concentrarea pe descoperirea medicamentelor pentru sistemul nervos central, în timp ce s-a închis ochii la administrarea medicamentelor. El spune că nicio companie farmaceutică mare din lume nu are în prezent un program de direcționare a medicamentelor către BBB.
Clienți alunecoși
O strategie timpurie pentru traversarea barierei a fost aceea de a face medicamentele mai solubile în lipide; acest lucru le-a permis să pătrundă în celulele endoteliale iubitoare de lipide din creier. Majoritatea drogurilor de abuz, cum ar fi alcoolul, cocaina și heroina, sunt lipofile. Dar există și un dezavantaj: „Dacă faci ceva lipofil, acesta va pătrunde în fiecare organ și celulă din corp și, prin urmare, trebuie să folosești cantități mari. Dacă poate avea un efect secundar negativ asupra unui alt organ sau țesut, acesta va apărea’, spune Drewes.
Câteva medicamente de dimensiuni mici – cum ar fi L-DOPA utilizat pentru tratarea bolii Parkinson – pot fi transportate pe „sisteme naturale de transport al nutrienților”, dar această abordare prezintă complicații în găsirea regimului de dozare corect, deoarece transportatorii pacienților au eficiențe diferite. De asemenea, deși medicamentele liposolubile pot pătrunde în membrana celulelor endoteliale ale creierului, ele pot fi aruncate la fel de repede afară de către transportatorii de eflux.
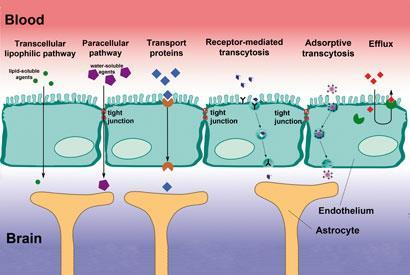
Sursa: © ADAPTED FROM ARMIN K?BELBECK
Există mai multe mecanisme pentru ca moleculele vitale să traverseze bariera, unele pot fi exploatate de medicamente
„Biologia este cu adevărat împotriva administrării de medicamente în creier, așa că sunt necesare strategii inteligente”, spune Joan Abbott, cercetător în neuroștiințe la King’s College London, Marea Britanie. ‘În trecut, marile companii farmaceutice au simplificat lucrurile, limitându-se la molecule mici care aveau chimia potrivită și evitau transportatorii de eflux’. O perspectivă recentă importantă este aceea că o solubilitate lipidică mai mare nu este neapărat mai bună; pentru majoritatea medicamentelor, concentrația „liberă nelegată” în creier este importantă, în timp ce medicamentele lipofile tind să se lipească de alte structuri din creier, inclusiv de membranele lipidice. ‘Chimiștii de medicamente din companii iau acum în considerare acest lucru’, adaugă Abbott.
Cu toate acestea, în zilele noastre, companiile își dau seama că au nevoie de medicamente mult mai inteligente pentru a le face mai specifice și cu mai puține efecte secundare. ‘Acesta este motivul pentru care încearcă să exploreze chimicale noi, vehicule noi de livrare și chiar tehnici pentru a deschide pentru scurt timp BBB și apoi să o închidă din nou după ce un medicament a intrat’, spune Abbott.
Porți temporare
Tumorile care debutează în creier sunt printre cele mai agresive și letale tipuri de cancer, însă opțiunile de tratament sunt limitate de BBB. Vara trecută, cercetătorii din Taiwan au raportat că au reușit să întrerupă bariera cu ajutorul ultrasunetelor focalizate (a se vedea Chemistry World, septembrie 2010, p24). Condus de Kuo-Chen Wei de la Universitatea Chang Gung, grupul a injectat nanoparticule magnetice, acoperite cu un medicament de chimioterapie, în șobolani. Aceștia au folosit ultrasunetele pentru a deschide o mică zonă a BHE și un câmp magnetic pentru a ghida particulele către o locație precisă din creier.1
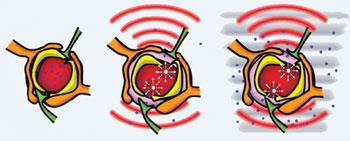
Sursa: Bariera hemato-encefalică: © PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, SUA
Ultrasunele pot întrerupe bariera, permițând ca particulele magnetice să fie ghidate prin ea
Ultrasunele ar putea ajuta, de asemenea, în afecțiuni precum Alzheimer și Parkinson, spune Kullervo Hynynen, de la Școala de Medicină a Universității din Toronto, Canada, care a făcut o muncă similară cu ultrasunete și microbule. Mecanismul fizic și biologic exact al ultrasunetelor nu este cunoscut, subliniază el. ‘Știm că bulele se dilată și se contractă odată cu unda de ultrasunete, iar unele experimente de microscopie rapidă au arătat că vasele mici de sânge – cel puțin in vitro – se dilată și se contractă odată cu bula. Prin urmare, celulele endoteliale sunt întinse’.
Microscopia electronică a susținut această idee de întindere fizică a celulelor de barieră, deși este indus și un anumit transport activ de vacuole prin celulele endoteliale, notează Hynynen. Riscul potențial al oricărei metode de întrerupere a BBB este acela de a lăsa garda jos. Moleculele vor pătrunde în creier în timpul întreruperii, dar acest risc este mic, deoarece este expusă doar o zonă definită a creierului. Dificultățile legate de ultrasunete se referă la lipsa de cunoștințe cu privire la mecanismul prin care funcționează, împreună cu factori legați de siguranță, eficacitate și durată (cum ar fi cât timp este deschisă bariera).
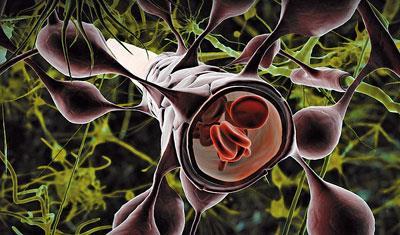
Sursa:
: © BEN BRAHIM MOHAMMED
Celulele endoteliale se înfășoară strâns în jurul vaselor de sânge pentru a exclude
O altă abordare disruptivă constă în injectarea unei soluții hiperosmotice (una care are o concentrație de solut mai mare decât cea a celulelor din jur) în arterele carotide pentru a deschide BBB pentru o perioadă de timp. Această metodă a fost susținută de câțiva ani de Edward Neuwelt de la Oregon Health and Science University din Portland, SUA. ‘Fluidul care curge prin vasele de sânge este hiperosmotic și astfel atrage apa din celulele endoteliale, determinându-le să se micșoreze’, explică Drewes. ‘Acest lucru îndepărtează joncțiunile strânse, formând goluri și spații. Dacă se administrează un medicament antitumoral în fluxul sanguin, acesta se poate difuza în creier și în tumoare”. Celulele se umflă treptat, revenind la dimensiunea lor obișnuită, astfel încât efectul este trecător.
În timp ce cancerele care se dezvoltă în creier sunt relativ rare; de 10 ori mai mulți oameni dezvoltă tumori cerebrale din cancere care încep în altă parte a corpului. BBB împiedică terapiile moderne împotriva cancerului care acționează în altă parte a corpului. Cu toate acestea, cercetătorii americani au dat recent un impuls în acest domeniu, folosind medicamente pentru disfuncția erectilă. Julia Ljubimova de la Cedars-Sinai Medical Centre din Los Angeles și colegii săi au descoperit că Viagra (sildenafil) și
Levitra (vardenafil), care inhibă o enzimă numită fosfodiesterază 5 (PDE5), au crescut permeabilitatea barierei hemato-encefalice. Utilizând un model de șoarece, ei au arătat că aceste medicamente pot crește cantitatea de Herceptin, un anticorp monoclonal de mari dimensiuni utilizat pentru tratarea cancerelor de plămâni și de sân, care traversează BHE și îi sporesc efectul antitumoral în creier.2
Piggy-backing on the BBB
Beverly Davidson, neurolog la Universitatea din Iowa, SUA, a căutat o terapie pentru copiii care suferă de boala de stocare lizozomală, cauzată de absența unei anumite enzime cerebrale . ‘Știm că nu putem pur și simplu să livrăm enzima în sânge și să o facem să acceseze creierul, așa că încercăm să concepem metode pentru a depăși această problemă’, explică ea. Grupul ei a luat celule endoteliale de barieră și le-a modificat pentru a produce enzima lipsă și a o secreta în creier.3 „În esență, transformăm BHE în prietenul nostru și nu în dușmanul nostru”.
ADN-ul recombinant care produce enzima a fost livrat în celulele endoteliale cu ajutorul unui vector viral pe care cercetătorii l-au modificat pentru a se localiza în endoteliile bolnave ale creierului. Davidson speră că noul material genetic va rămâne în endotelii timp de mulți ani. „Nu avem nicio dovadă că aceste celule se divid deloc, cel puțin la rozătoare”, explică ea, astfel încât o singură rundă de terapie genică ar putea dura zeci de ani. Tratamentul a reconstituit activitatea enzimatică în tot creierul unui model de șoarece; următorul pas este de a trece la un model animal mare al bolii.
Compania canadiană AngioChem a dezvoltat o modalitate diferită de a strecura terapii peste barieră – prin valorificarea propriilor receptori de transport. Acești receptori, cum ar fi proteina legată de receptorul de lipoproteine (LRP-1), permit în mod normal substanțelor esențiale precum glucoza, insulina și hormonii de creștere să pătrundă în creier. „Ei văd ceea ce pare a fi primul succes în ceea ce privește livrarea a ceva care va ataca o tumoare”, spune Drewes. ‘Există un oarecare entuziasm în legătură cu acest lucru și ei încearcă să îl dezvolte într-un sistem mai general de administrare a medicamentelor’.
Vehicule de livrare și cai troieni
O altă zonă de creștere reală este cea a construcțiilor artificiale, sau a vehiculelor de livrare proiectate, spune Abbott: ‘În următorii 10 ani mă aștept la o mulțime de astfel de vehicule’. Nanoparticulele și diverși polimeri pot fi proiectați pentru a avea caracteristicile potrivite pentru a se lega de medicamente, dar și pentru a recunoaște receptorii de pe celulele endoteliale ale creierului, astfel încât acestea să fie preluate peste barieră. Un avantaj al polimerilor este că se pot modifica chimic, notează Martin Garnett de la Children’s Brain Tumour Research Centre de la Universitatea din Nottingham, Marea Britanie, care a început să lucreze la nanoparticule de polimeri.
Ljubimova este de părere că nanomedicina va aduce un salt major pentru tratamentul cancerului și va îmbunătăți calitatea vieții pacienților prin reducerea toxicității tratamentelor. ‘Există o mulțime de lucruri în teste clinice, care prezic câștiguri mari „peste cinci până la zece ani”‘, spune ea. Cu toate acestea, Abbott oferă un cuvânt de precauție cu privire la astfel de vehicule medicamentoase. ‘Dificultatea este aceeași ca și în cazul transportatorilor din BHE. Calcularea cantității de medicament care ajunge în creier prin intermediul vehiculelor de administrare este destul de dificilă. Majoritatea dovezilor sugerează că cantitatea care ajunge la ținta corectă este destul de mică, așa că trebuie să optați pentru agenți foarte activi’.

Sursa: © HAMISH KIDD
Un cal troian molecular poate strecura medicamente precum GDNF peste barieră
Metoda calului troian, care leagă agenții terapeutici de moleculele care tranzitează în mod normal bariera, este susținută de Pardridge. El a reproiectat factorul neurotrofic derivat glial (GDNF) ca un cal troian molecular. GDNF este o neurotrofină puternică care poate revigora nervii afectați în modelele animale ale bolii Parkinson; este, de asemenea, o potențială terapie pentru accidentul vascular cerebral și dependența de droguri, dar nu traversează BHE.
Utilizând rezervoare de medicamente implantate și catetere ventriculare – ambele proceduri invazive – cercetătorii au descoperit că GDNF-ul pe care l-au livrat era biologic activ, dar nu avea eficacitate clinică. Problema a fost distribuția; a fost nevoie de o localizare foarte precisă a cateterelor, iar acest lucru nu a fost realizat în toate studiile clinice. Trojanul lui Pardridge este un anticorp monoclonal împotriva receptorului uman de insulină, care poate administra GDNF prin BHE.4 În studiile efectuate pe maimuțe Rhesus, el nu a observat niciun eveniment advers asociat cu administrarea de doze mari de proteină de fuziune anticorp-GDNF.
Scoaterea din laborator
Abbott sugerează că unul dintre motivele pentru care progresul în ceea ce privește administrarea de medicamente în BBB a fost lent este lipsa de finanțare și de interes din partea industriei. Ea explică faptul că marile companii farmaceutice s-au retras în mare parte din aspectele legate de chimia creierului și de administrarea medicamentelor, deoarece au investit mulți bani în programe care s-au dovedit a nu fi productive. Acum sunt mai prudenți, mai pesimiști sau se concentrează pe domenii cu șanse mai mari de succes. Este posibil ca unele companii să considere chiar că nu sunt competente să urmărească ținte cerebrale în care BBB reprezintă o provocare. Chimia sa complexă face ca predictibilitatea să fie mai dificilă.
Sursa: © JULIA LJUBINOV
Tumorile din creier reprezintă o problemă deosebită, deoarece majoritatea medicamentelor obișnuite împotriva cancerului nu pot traversa bariera
Există totuși semne pozitive. Modelele de culturi celulare in vitro ale barierei – necesare pentru testele de permeabilitate a medicamentelor – au fost îmbunătățite în ultimii ani. Tehnicile de imagistică, cum ar fi tomografia cu emisie de pozitroni (PET) și imagistica prin rezonanță magnetică (IRM), ajută să arate ce face BHE și ce medicamente ajung la țintele potrivite în concentrație suficientă.
Acest lucru este esențial, deoarece cercetătorii au ajuns să realizeze că bariera nu este o structură defensivă statică. Este o interfață activă, reglementată și reglată; este modificată la și în jurul locului de leziune după un accident vascular cerebral, de exemplu. Potrivit lui Neuwelt, tumorile cerebrale, epilepsia, boala Alzheimer și boala Parkinson sunt toate asociate cu „perturbări ale BBB normale care contribuie la patologia lor. „5
Informațiile privind starea barierei la un anumit pacient pot fi necesare pentru a concepe și rafina terapiile adecvate. Din ce în ce mai mult în cazul, de exemplu, al leziunilor de stres posttraumatic, se recunoaște că trebuie să știi ce face bariera pentru a ajusta tratamentul, spune Abbott. Este posibil să fie nevoie să ajustați tratamentul pe o perioadă de luni sau săptămâni.
Garnett spune că, până acum, companiile farmaceutice s-au concentrat pe moleculele mici de medicamente mai degrabă decât pe sistemele de eliberare a medicamentelor, dar el crede că acest lucru se schimbă acum. În plus, există o comunitate de cercetare activă în cadrul universităților și al institutelor de cercetare care analizează ultrasunetele, proteinele de fuziune Trojan, construcțiile polimerice și alte mijloace de a depăși bariera și de a face ca terapia să ajungă acolo unde este nevoie de ea.
Abbott concluzionează cu o evaluare optimistă a BBB și a eforturilor de a face ca terapiile să o traverseze: ‘S-au înregistrat multe progrese în ultimii cinci ani. Vedem tot felul de lucruri care sunt acum posibile – deci, în ceea ce privește înțelegerea de bază, cred că lucrurile arată foarte bine. Dar este probabil adevărat că o mare parte din inovație provine de la companii mici; unele dintre acestea au încheiat parteneriate cu companii mai mari sau au fost preluate de acestea. Marile companii farmaceutice tradiționale sunt încă destul de prudente în a încerca noi modalități de a introduce lucruri în creier, deși acest lucru se schimbă.
Anthony King este un scriitor științific independent cu sediul în Dublin, Irlanda
.
