- Metodologie
- Figura1:Imaging pathway
- Abordarea diagnostică și work-up-ul inițial
- Citologia urinară
- Imagistica inițială la pacienții cu risc scăzut
- Figura2:Carcinomul cu celule de tranziție al vezicii urinare (US)
- Figura3:Carcinom renal cu celule de tranziție (US și RPUG)
- Imagistica inițială la pacienții cu risc ridicat
- Figura4:CTC vezical și renal (CTU)
- Figura5:TCC vezical (IRM)
- Figura6:Ureteric TCC (CTU)
- Figura7:Tumoră vezicală (cistoscopie)
- Alte studii imagistice
- Supravegherea clinică
- Tabelul2: Indicații pentru trimitere
Metodologie
O căutare electronică din august-septembrie 2015 în MEDLINE prin PubMed și în baza de date Cochrane Database of Systematic reviews a identificat articole originale relevante, recenzii sistematice și ghiduri bazate pe dovezi din perioada 2008-septembrie 2015, care au fost incluse. Următorii termeni au fost utilizați în combinație în timpul analizei literaturii pentru a produce lista articolelor analizate: „nedureros”, „macroscopic”, „vizibil” ȘI „hematurie”, „rinichi”, „uretere”, „vezică urinară”, „cancer de vezică urinară”, „tract urinar”, „citologie”, „diagnostic imagistic”, „radiografie”, „ultrasonografie”, „ecografie”, „pielografie”, „tomografie computerizată cu raze X” ȘI „urografie”, „rezonanță magnetică” ȘI „urografie”, „intravenoasă” SAU „excretoare” SAU „urografie”, „urologie” SAU „nefrologie” SAU „trimitere” SAU „consultare”, „cistoscopie”, „ghiduri”.
De asemenea, a fost efectuată o căutare manuală pentru a identifica alte publicații relevante din studiile recuperate pentru revizuire. Un total de 84 de articole în text integral au fost preselectate și evaluate pentru eligibilitate. Au fost incluse articolele care descriu studii originale, ghiduri bazate pe dovezi sau revizuiri sistematice, în timp ce studiile pediatrice și pe animale au fost excluse. Articolele care nu erau în limba engleză sau care aveau un text limitat au fost, de asemenea, excluse, urmând ca 59 de articole finale să fie incluse și clasificate în conformitate cu Oxford Centre for Evidence-Based Medicine Levels of Evidence . Căile bazate pe dovezi au fost elaborate și revizuite de către membrii comitetului editorial de experți Diagnostic Imaging Pathways (DIP) în conformitate cu procesele obișnuite DIP (http://www.imagingpathways.health.wa.gov.au/index.php/production/processes-for-creating-and-managing-content), în consultare cu editorul, un urolog și un nefrolog. Algoritmul final (Figura 1), care este, de asemenea, disponibil pe Imaging Pathways (Instrument online de luare a deciziilor clinice: Dulku G. Painless Macroscopic Haematuria. Diagnostic Imaging Pathways; septembrie 2015), oferă îndrumări și recomandări imagistice pentru pacienții adulți cu hematurie inexplicabilă, nedureroasă și vizibilă.
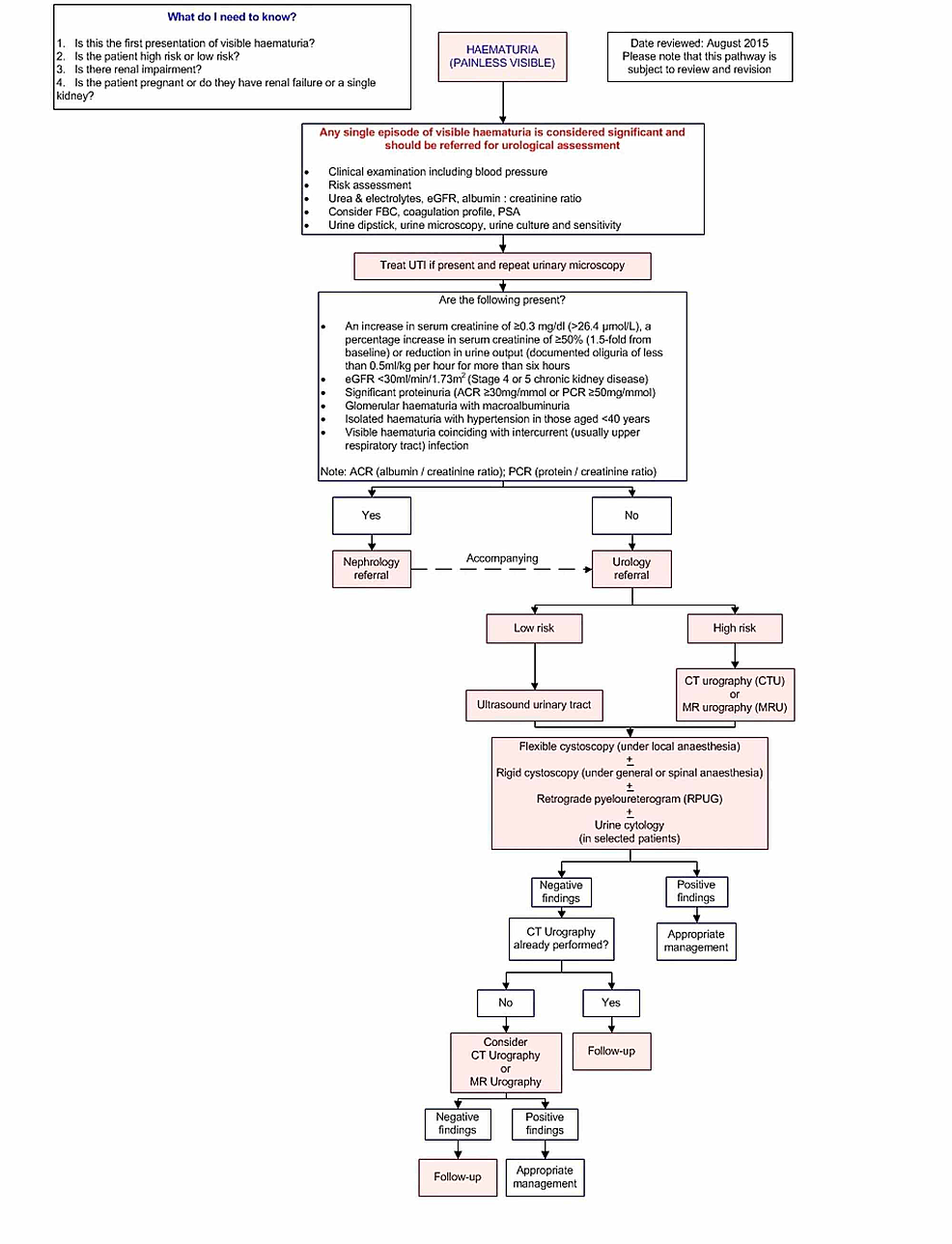
Figura1:Imaging pathway
Acest traseu oferă îndrumări privind imagistica pacienților adulți cu hematurie vizibilă inexplicabilă, nedureroasă și nedureroasă.
eGFR: Rata estimată de filtrare glomerulară; FBC: Hemoleucograma completă; PSA: Antigenul specific prostatic; ACR: Raportul albumină/creatinină; PCR: Raportul proteine/creatinină; ITU: Infecție a tractului urinar.
Revizuirea noastră nu a inclus o analiză a ghidului imagistic pentru detectarea calculilor din tractul urinar ca o cauză a hematuriei, deoarece, de obicei, aceasta este asociată cu durere. Ne-am concentrat în primul rând pe ghidul imagistic și pe literatura de specialitate de sprijin pentru hematuria vizibilă nedureroasă cu tumori urologice maligne ca o cauză potențială.
Abordarea diagnostică și work-up-ul inițial
Consensul Asociației Britanice a Chirurgilor Urologi (BAUS) și al Serviciului Interregional al Șefilor de Urologie (IRCUS), Kaiser Permanente, America a sugerat că orice episod unic de HV este considerat semnificativ și ar trebui să fie referit pentru o evaluare urologică care, în aproape toate cazurile, va include cistoscopia .
Între timp, pot fi efectuate investigații pentru a identifica cauzele tranzitorii, tratabile, și pentru a aranja imagistica primară. Pacienții cu HV și infecție a tractului urinar (ITU) dovedită trebuie totuși investigați pentru depistarea unei tumori maligne concomitente, deoarece tumorile maligne coexistă în mod obișnuit cu o infecție sau acționează ca un nidus din care se propagă o infecție . Infecția tractului urinar trebuie tratată înainte de cistoscopie, deoarece există un risc de uro-sepsis dacă cistoscopia este efectuată în prezența unei ITU active.
Prezența HV nu ar trebui, de asemenea, să fie atribuită terapiei anticoagulante sau antiplachetare și acești pacienți ar trebui, de asemenea, să fie evaluați indiferent de aceste medicamente, deoarece rapoartele de malignitate subiacentă au fost găsite la 24% și 7% din pacienți în două serii separate .
Prin urmare, rolul principal al imagisticii este de a identifica acei pacienți cu o cauză malignă a hematuriei. Cu toate acestea, alegerea modalității imagistice depinde de diverși factori individuali ai pacientului (de exemplu, vârsta, factorii de risc pentru malignitate, funcția renală și sarcina) și de alți factori, cum ar fi politica și practica locală, rentabilitatea și disponibilitatea resurselor .
În mod tradițional, investigațiile de primă linie au inclus radiografia convențională, ecografia renală (US) și/sau pielograma intravenoasă (IVP) în combinație cu cistoscopia. Aceasta din urmă este importantă, deoarece multe leziuni sângerânde ale tractului urinar apar în vezica urinară, iar procedurile imagistice nu s-au dovedit încă în mod concludent a fi la fel de sensibile ca și cistoscopia în diagnosticarea celor mai multe dintre ele .
Investigațiile de a doua linie au inclus urograma prin tomografie computerizată cu mai mulți detectoare (MDCTU) și urografia prin rezonanță magnetică (MRU), deseori efectuate doar dacă testele de primă linie relevă o anomalie.
IRCUS a recomandat ca pentru pacienții cu hematurie semnificativă să se efectueze o CTU modificată sau o IVP cu US renală concomitentă. Nu este nevoie de tomografie renală la urografia intravenoasă (IVU) dacă se efectuează o US renală concomitentă. Această abordare va reduce expunerea la radiații ionizante .
Când recomandă imagistica pentru evaluarea HV, Cowan a sugerat ca tipul de modalitate imagistică utilizată să se bazeze pe un scor de risc, pacienții >40 de ani urmând să fie supuși la urografie CT, în timp ce pacienții <40 de ani să fie supuși la ecografie ca modalitate imagistică de primă linie . Societatea Europeană de Radiologie Urogenitală (ESUR) a sugerat că investigarea pacienților cu risc scăzut necesită ecografie și cistoscopie, iar pacienții cu risc ridicat necesită UCT și cistoscopie pentru o imagistică completă a rinichilor și a tractului urinar .
Citologia urinară
Citologia urinară, deși controversată, este esențială pentru evaluarea carcinomului cu celule uroteliale din tractul urinar superior (UUT-UCC), iar liniile directoare ale Asociației Europene de Urologie (EAU) recomandă ca citologia urinară să fie efectuată ca parte a analizei standard de diagnosticare . Citologia urinară are o sensibilitate de 25%, o specificitate de 91%, o valoare predictivă pozitivă ridicată, dar o valoare predictivă negativă scăzută .
Cu toate acestea, citologia urinară are o rată fals negativă ridicată pentru detectarea malignității și o citologie negativă nu poate exclude niciodată complet prezența unei tumori vezicale, cistoscopia fiind justificată în toate cazurile.
Numeroase teste de urină disponibile în comerț pentru biomarkerii purtați de urină includ BTA TRAK, ImmunoCyt/uCyt+, CxBladder, Nuclear Matrix Protein 22 (NMP-22) și UroVysion (FISH), deși acestea pot rata o proporție semnificativă de pacienți cu cancer de vezică urinară, în special atunci când acuratețea sa este slabă pentru tumorile în stadiu scăzut și de grad scăzut . Din aceste motive, nu s-a ajuns la un consens cu privire la rolul citologiei urinare și/sau al markerilor tumorali vezicali în evaluarea pacienților cu hematurie .
Imagistica inițială la pacienții cu risc scăzut
EUR a sugerat că investigarea pacienților cu risc scăzut necesită US și cistoscopie, iar pacienții cu risc ridicat necesită UCT și cistoscopie pentru o imagistică completă a rinichilor și a tractului urinar . Cu toate acestea, sensibilitatea US nu este suficientă pentru a elimina necesitatea cistoscopiei din cauza lipsei sale de sensibilitate în detectarea tumorilor vezicale mici, în special a celor cu diametrul mai mic de 0,5 cm.
Ultrasonul (US) este important în evaluarea inițială a hematuriei și, pe lângă faptul că este ușor disponibil și ieftin, nu implică expunerea la radiații ionizante și este deosebit de util în cazul populațiilor sensibile la radiații, cum ar fi copiii și femeile însărcinate sau în vârstă fertilă. Ecografia permite, de asemenea, planuri de scanare nelimitate, permițând astfel o bună vizualizare a rinichilor și a vezicii urinare. În plus, studiile Doppler pot oferi informații suplimentare cu privire la vascularizația maselor (Figura 2A, 2B) .
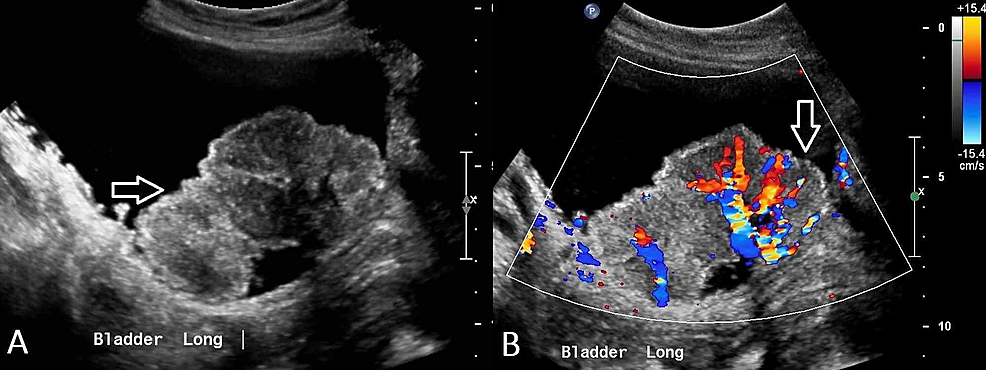
Figura2:Carcinomul cu celule de tranziție al vezicii urinare (US)
(A) Ecografia pelvisului demonstrează o tumoare neregulată, eterogenă în interiorul vezicii urinare, cu multiple leziuni polipoidale mai mici observate adiacente, ceea ce este sugestiv pentru cancerul vezicii urinare. (B) Vascularitatea este demonstrată în cadrul acestei mase.
În detectarea tumorilor UUT, US are o sensibilitate variabilă în detectarea carcinoamelor uroteliale, cu o sensibilitate moderată (82%) pentru detectarea carcinomului cu celule renale și o sensibilitate scăzută (12%) pentru detectarea carcinomului urotelial al ureterului . Cu toate acestea, în comparație cu IVP în detectarea anomaliilor UUT la pacienții care prezintă hematurie, US este mai sensibilă în detectarea tumorilor renale și vezicale , cu o sensibilitate mai mare (96% față de 25%) și, respectiv, o valoare predictivă negativă mai mare (98% față de 91%) .
În plus, US este, de asemenea, utilă pentru a detecta hidronefroza și/sau hidroureterul care pot fi o sechelă a tumorilor vezicale care obstrucționează joncțiunea vezico-ureterică (figura 3). Cu toate acestea, în comparație cu imagistica de secțiune transversală, cum ar fi MDCTU sau MRU, US are o sensibilitate mai mică în detectarea anomaliilor tractului urinar.
Ecografia este excelentă în a determina dacă o masă este chistică sau nu și dacă o leziune chistică este un chist simplu sau minim complicat sau complicat. Leziunile care nu sunt chisturi simple necesită un bilanț suplimentar cu CT sau RMN. US cu substanță de contrast (CEUS) este o alternativă promițătoare în evaluarea inițială a maselor renale. Performanța raportată a CEUS în evaluarea maselor chistice solide sau complexe suspectate sugerează o valoare similară a CEUS în comparație cu CT. CEUS are avantajul lipsei de nefrotoxicitate, al lipsei de radiații ionizante și al capacității de a evalua în timp real tiparul de evidențiere – iar acest lucru poate fi realizat la prima vizită a pacientului la US. Cu toate acestea, locul CEUS în algoritmul de diagnosticare necesită clarificări suplimentare.
Prin urmare, utilizarea US ca modalitate imagistică de primă linie în evaluarea hematuriei pare să fie justificată . Având în vedere că ultrasunetele singure pot rata potențial leziunile ureterale și uroteliale, este necesară o evaluare suplimentară cu cistoscopia, în timp ce pielo-ureterografia retrogradă este un adjuvant util (figura 3) .
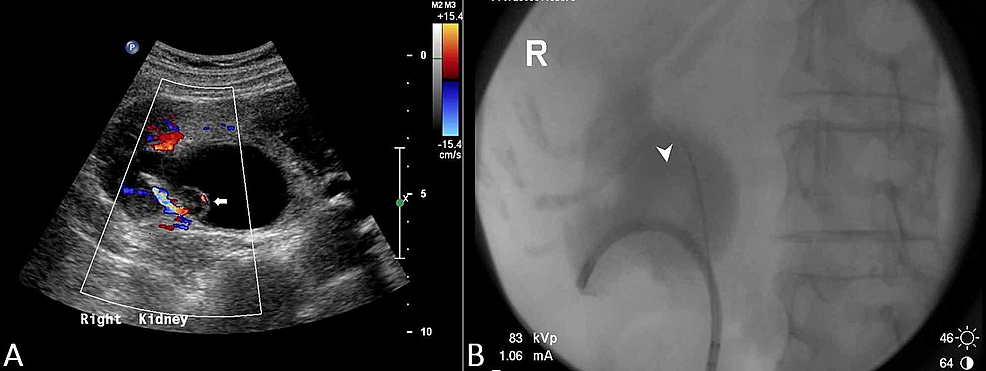
Figura3:Carcinom renal cu celule de tranziție (US și RPUG)
(A) Ecografia pelvisului demonstrează un ureter drept proximal difuz îngroșat, cu o leziune papilară (săgeată) observată în cadrul pelvisului renal drept și hidronefroza dreaptă rezultată. (B) Acest lucru corespunde constatărilor pielo-ureterogramei retrograde (RPUG) (cap de săgeată), ceea ce sugerează un carcinom cu celule tranziționale al tractului urinar superior drept obstructiv.
Imagistica inițială la pacienții cu risc ridicat
Urografia CT
Urografia CT (denumită și CT IVP, deși CTU este termenul preferabil) depășește US, IVU, și radiografia în evaluarea maselor parenchimatoase renale și a calculilor din tractul urinar, cu o sensibilitate și o specificitate pentru tumorile maligne uroteliale din tractul superior de 67-100% și, respectiv, 93-99% .
Strategia diagnostică optimă pentru investigarea pacienților cu risc ridicat după excluderea ITU este o strategie combinată care utilizează UCT și cistoscopia flexibilă . Pacienții’ cu leziuni compatibile cu cancerul de vezică urinară la UCT ar trebui să fie referiți direct pentru cistoscopie rigidă și să evite astfel cistoscopia flexibilă, cu un avantaj de reducere cu 17% a numărului de cistoscopii flexibile efectuate .
Pentru toate celelalte categorii de pacienți, inclusiv pacienții mai tineri și pacienții cu indicații mai benigne și cu probabilități mai mici de cancer înainte de testare, US este modalitatea imagistică de primă linie . Modificări ale tehnicii de examinare a urografiei CT, constând în protocoale limitate și combinații de faze de scanare, ar putea fi utilizate alternativ sau complementar cu celelalte teste imagistice .
Protocolul de scanare ar trebui să includă: scanare fără contrast, nefrografie (90-100 de secunde după bolusul de contrast) și faza excretorie (sau pielografică) (5-15 minute după administrarea contrastului) . O fază cortico-medulară este utilă în cazuri selectate, de exemplu, dacă se suspectează un pseudoanevrism sau un pseudotumor. Achiziția de rutină în timpul acestei faze poate să nu fie justificată . Imaginile fără contrast sunt utile pentru a detecta calculul renal. Faza nefrografică are cea mai mare sensibilitate în detectarea maselor renale, iar corelația cu imaginile fără contrast este necesară pentru a arăta un accesoriu fără echivoc. Faza pielografică/excretorie este utilizată pentru a evalua sistemul colector, ureterele și vezica urinară, cu utilizarea tehnicilor de distensie ureterică, cum ar fi compresia, bolusul salin intravenos și diureticele, toate acestea demonstrând rezultate variabile. Urografia CT poate detecta, de asemenea, boala extra-urinară .
În comparație cu tumorile uroteliale, mulți pacienți cu malignitate renală rămân asimptomatici până în stadiile tardive ale bolii, având în vedere că marea majoritate a cancerelor renale sunt mici și detectate întâmplător. În plus, masele renale invadează rareori în sistemul colector. În consecință, triada clasică de durere în flanc, hematurie și o masă renală abdominală palpabilă a carcinomului cu celule renale (CCR) apare la cel mult 6-9% dintre pacienți și, atunci când este prezentă, sugerează în mod clar o boală local avansată și un prognostic slab. În acest caz, CT și IRM sunt recomandate fiecare pentru bilanț și sunt considerate egale pentru stadializare și diagnostic (figurile 4, 5) . Cu toate acestea, sunt așteptate studii comparative între CT și IRM de câmp înalt. Între timp, IRM poate fi utilizat în cazuri selectate pentru rezolvarea problemelor. IRM cu ponderare de difuzie (DWI) poate fi, de asemenea, utilă pentru detectarea și caracterizarea leziunilor, dar analizele sistematice indică doar o acuratețe moderată .
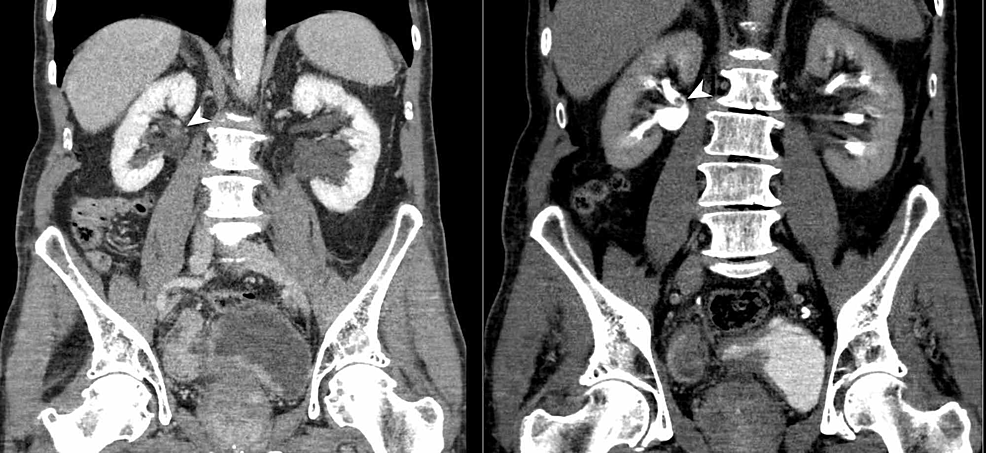
Figura4:CTC vezical și renal (CTU)
Urografia CT (reformat coronal) demonstrează îngroșarea neregulată a peretelui vezicii urinare și, de asemenea, un defect de umplere polipoidă sesilă în fața posterioară a pelvisului renal drept (capete de săgeată). Rezultatele sunt sugestive pentru un carcinom cu celule tranziționale (TCC) multifocal al tractului urinar.
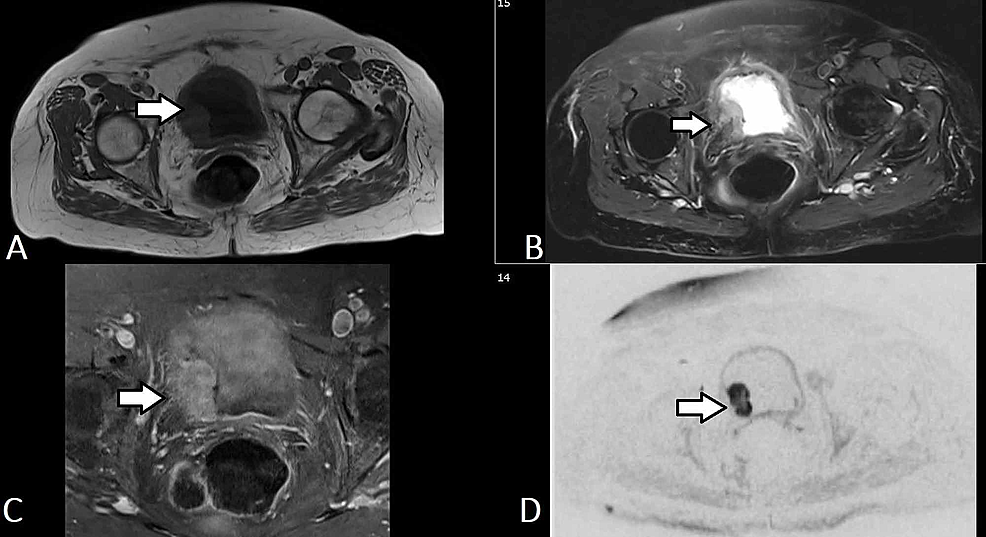
Figura5:TCC vezical (IRM)
(A-D) Imaginile axiale selectate de urografie RM ale aceluiași pacient demonstrează o masă lobulată (săgeată) care provine din peretele lateral drept al vezicii urinare, care se extinde până la trigon și invadează peretele vezicii urinare pentru a implica stratul extern fără a se extinde în grăsimea perivesicală. Masa are o intensitate a semnalului T1 scăzută și T2 ridicată. Masa prezintă o amplificare de contrast relativ omogenă, difuză și o restricție de difuzie proeminentă (b50/400/800). Constelația de constatări reflectă o tumoare vezicală care este probabil stadializată ca T2b No Mx.
TCC: Carcinom cu celule de tranziție
Clasificarea Bosniak a maselor chistice renale se bazează pe caracteristicile imagistice ale tomografiei computerizate cu substanță de contrast și este utilă pentru a prezice riscul de malignizare și pentru a oferi îndrumare în management. Riscul de malignizare pentru leziunile chistice Bosniak 1, 2, 2F, 3 și 4 este de 0%, 0%, 25%, 54% și, respectiv, 100% .
Urografia CT poate fi, de asemenea, eficientă în diagnosticarea tumorilor vezicale. Cu toate acestea, rezultatele pot diferi în funcție de populația specifică studiată. În grupul cu risc ridicat, rezultatele fără echivoc ale UCT au avut o sensibilitate de 93% și o specificitate de 99% pentru detectarea cancerului de vezică urinară, cu o valoare predictivă negativă (NPV) globală de 95%. VNA ridicată a CTU poate evita cistoscopia la acești pacienți selectați, deși cistoscopia rămâne standardul de aur în detectarea tractului urinar inferior, inclusiv a tumorilor uroteliale vezicale, deoarece nici IVP sau MDCTU nu au în mod constant sensibilități suficient de semnificative pentru a exclude anomaliile mucoasei vezicale .
Dozele de radiații reprezintă o preocupare în cazul MDCTU și aceasta poate fi redusă prin limitarea numărului de faze imagistice prin utilizarea CT cu dublă energie (DECT) sau a tehnicii split-bolus . În plus, (25) omiterea achiziției neîmbogățite duce la reducerea expunerii la radiații cu aproape 50% .
DECT oferă informații despre modul în care se comportă substanțele la energii diferite, capacitatea de a genera seturi de date virtuale neîmbogățite și o mai bună detectare a substanțelor care conțin iod pe imaginile cu energie scăzută . Alte avantaje ale DECT includ o bună înregistrare temporală și spațială și o bună separare spectrală între scanările cu energie înaltă și joasă ușor de egalizat doza și zgomotul . Un studiu prospectiv a demonstrat că urografia DECT monofazată cu intensificarea sincronă a fazei nefrografice-excretoare reprezintă o abordare precisă „all-in-one” cu o economie de până la 45% a dozei de radiații în comparație cu un protocol standard cu două faze cu opacizare bună în 86 .9% din cazuri și imagini virtuale neîmbunătățite (VUE) excelente sau bune în 83,3% din cazuri .
Pe de altă parte, MDCTU split-bolus asigură opacifierea de cel puțin 50% a majorității segmentelor UUT cu o sensibilitate ridicată (88.9-100%), specificitate (99-99,5%) și acuratețe (98,5-99,5%) pentru detectarea tumorilor tractului urinar superior (figura 6) .
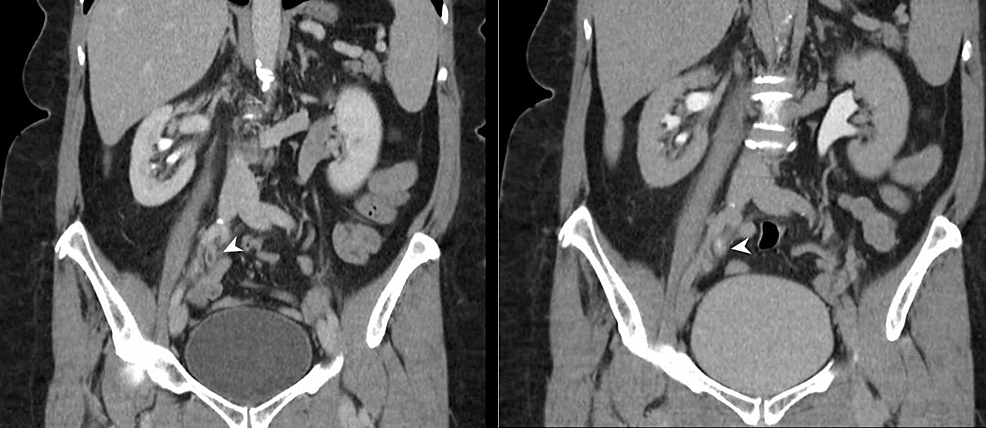
Figura6:Ureteric TCC (CTU)
Urografia CT (reformate coronale) demonstrează un segment de 4 cm de îngroșare urotelială circumferențială la joncțiunea ureterului mijlociu și distal-dreapta (capete de săgeată) cu evidențiere urotelială anormală. Există o obstrucție secundară a sistemului colector drept cu punctul de tranziție observat la nivelul îngroșării uroteliale anormale, ceea ce este foarte suspect pentru un TCC urotelial drept.
TCC: Carcinom cu celule de tranziție
Urografia prin rezonanță magnetică
Urografia prin rezonanță magnetică este utilă în diagnosticarea și stadializarea afecțiunilor maligne ale rinichilor, vezicii urinare și prostatei și în evaluarea funcției renale. Servește ca o tehnică imagistică alternativă pentru populația sensibilă la radiații, inclusiv copiii și femeile însărcinate; cei care necesită examinări repetate ale tractului urinar și cei cu contraindicație la mijloacele de contrast iodate.
Se poate utiliza un protocol MRU complet pentru imagistica tuturor componentelor rinichilor și a sistemului colector urinar într-o singură sesiune de imagistică. Urografia prin rezonanță magnetică se realizează prin două metode principale: urografia statico-fluidală cu secvențe ultra-rapide ponderate în T2, similare cu cele utilizate pentru colangiopancreatografia prin rezonanță magnetică (MRCP), și secvențe ponderate în T1 de urografie excretorie după administrarea de contrast IV cu gadoliniu .
MRU static-fluid este preferată față de MRU excretor în imagistica pacienților cu funcție renală deficitară, a pacienților gravide și a pacienților cu obstrucție ureterală, în special atunci când există un risc rezonabil de fibroză sistemică nefrogenă . Cu toate acestea, având în vedere că secvențele ponderate în T2 sunt efectuate fără administrarea de contrast IV, sunt adesea necesare modificări imagistice pentru a optimiza imagistica ureterală.
Imagistica ureterală poate fi, de asemenea, îmbunătățită în special la MRU excretor, în urma administrării de substanță de contrast IV, soluție salină și un diuretic pentru a obține o distribuție mai uniformă a contrastului . Deși dovezile relevă că DWI demonstrează doar o acuratețe moderată pentru predicția malignității renale, performanța sa ca test independent este încă netestată . Adăugarea DWI la imagistica ponderată în T1 și T2 crește sensibilitatea în identificarea cancerului UUT cu o concordanță inter-observator excelentă. În special, combinația T2WI+DWI demonstrează sensibilități între 92-98% pentru diagnosticarea tumorilor vezicale (figura 5).
Dezvantajele MRU includ costul, disponibilitatea, timpul de achiziție mai lung, degradarea imaginii din cauza artefactelor de mișcare, rezoluția spațială și încrederea diagnostică mai scăzută în detectarea malignității uroteliale în comparație cu UCT. Cu toate acestea, se așteaptă ca dezvoltarea unor secvențe mai rapide și optimizarea protocoalelor RMN 3-T să rezolve aceste probleme .
Cistoscopia
Cistoscopia este încă metoda de alegere pentru evaluarea vezicii urinare și nu ar trebui să fie înlocuită de nicio tehnică de imagistică excretorie . Orientările recente ale EAU recomandă, de asemenea, ca cistoscopia să fie efectuată pentru a exclude tumora vezicală concomitentă (figura 7) atunci când este diagnosticat cancerul UUT, în special atunci când autorii au demonstrat rezultate fals-pozitive și fals-negative notabile la CTU și MRU în detectarea tumorilor vezicale în comparație cu histopatologia la pacienții cu hematurie vizibilă . Ar trebui efectuată o cistoscopie la aproape toți pacienții cu hematurie vizibilă nedureroasă .
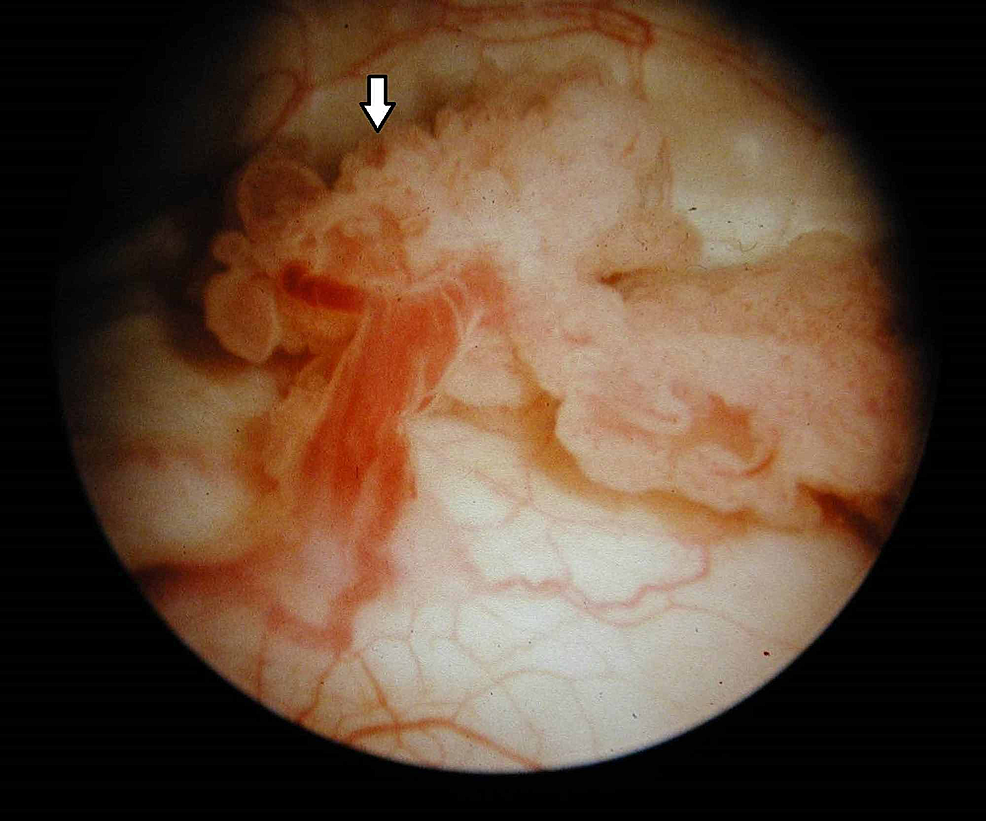
Figura7:Tumoră vezicală (cistoscopie)
Cistoscopia evidențiază o excrescență exofilă, asemănătoare unei conopide, cu frunzulițe delicate și zone de ulcerații în concordanță cu o tumoare malignă a vezicii urinare (săgeată).
Cistoscopia flexibilă este o procedură simplă, rapidă și sigură, efectuată sub anestezie locală ca un caz de o zi, cu o reasigurare fiabilă și permițând pacienților operați să fie diagnosticați și pregătiți pentru intervenția chirurgicală în aceeași vizită .
Pe de altă parte, cistoscopia rigidă este efectuată sub anestezie generală sau spinală, în special atunci când sunt anticipate proceduri suplimentare mai complexe. O pielo-ureterogramă retrogradă (RPUG) poate fi efectuată în momentul cistoscopiei rigide pentru a vizualiza căile superioare dacă nu s-a efectuat deja CTU .
Alte studii imagistice
Pielo-ureterografia retrogradă
Urograma CT s-a dovedit a avea o acuratețe diagnostică mai mare decât RPUG pentru detectarea leziunii uroteliale . Prin urmare, se justifică faptul că UCT ar trebui să fie utilizată înainte de RP, ca un test unic, neinvaziv și cuprinzător, care permite diagnosticarea și/sau stadializarea simultană.
Pielografia retrogradă poate fi în continuare utilizată ca investigație de linia a doua pentru a caracteriza mai bine defectele de umplere detectate la alte modalități, la UCT non-diagnostice, sau la pacienții cu insuficiență renală sau în cazurile de alergie la substanța de contrast. Pielo-ureterografia retrogradă poate arăta doar lumenul ureterului și nu poate descrie în mod direct anomalii extrinseci (figura 3) .
Radiografia simplă a rinichilor, ureterelor și vezicii urinare (Plain X-ray KUB)
Radiografia simplă KUB are în prezent o valoare redusă în investigarea pacienților cu hematurie nedureroasă și nu este utilizată ca modalitate de imagine de primă linie .
Urografia excretorie/Urografia intravenoasă (IVU)
Urografia intravenoasă este o alegere bună în evaluarea bolii uroteliale și intraluminale, dar nu este suficient de sensibilă pentru detectarea maselor renale de dimensiuni <2-3 cm și a fost înlocuită în prezent de UCT pentru imagistica UUT . Investigarea hematuriei la pacienții cu risc ridicat doar cu IVU nu mai este recomandată .
Principalul său avantaj este că IVU imaginează întreaga UUT cu un grad ridicat de rezoluție spațială și oferă, de asemenea, informații structurale, precum și date funcționale limitate. Este adesea testul cel mai eficient din punct de vedere al costurilor în multe centre .
Cu toate acestea, dezavantajele IVU includ un timp de achiziție îndelungat, potențiale reacții de contrast periculoase, necesitând pregătirea intestinului și expunerea la o încărcătură de radiații apreciabilă. Inexactitatea sa relativă este principalul său neajuns și va fi în curând depășită .
Supravegherea clinică
Există un risc ca 1-3% dintre pacienții cu un bilanț negativ să dezvolte malignitate în decurs de trei ani dacă nu sunt controlați . Cel mai bun panel de politici al Asociației Urologice Americane (AUA) recomandă ca medicii de îngrijire primară să verifice dacă există HV, simptome urinare noi și citologie pozitivă la fiecare șase luni timp de trei ani, iar dacă rezultatele sunt în mod constant negative până atunci, urmărirea poate fi întreruptă . BAUS recomandă re-referirea la urologie este necesară în cazul în care există o dezvoltare a HV sau a hematuriei invizibile simptomatice (HNV) în timpul urmăririi de îngrijire primară, a cărei durată nu a fost clar definită . Best Practice Advocacy Centre din Noua Zeelandă a recomandat monitorizarea anuală a cauzelor nefrologice cu ajutorul probei de urină, a tensiunii arteriale, a eGFR și a raportului albumină-creatinină/proteină-creatinină (ACR/PCR) în timp ce persistă hematuria, și anual timp de doi ani pentru cauzele urologice cu ajutorul probei de urină, a eGFR, a ACR/PCR și a citologiei urinare. Această inițiativă permite urmărirea în asistența medicală primară pentru a oferi reasigurare pacienților care se confruntă cu preocupări legate de hematuria continuă, care poate fi intermitentă, dar persistentă în ciuda unui bilanț negativ. Indicația pentru trimiterea la nefrologie și urologie este rezumată în tabelul 2 .
Sesizare la nefrologie
O creștere a creatininei serice de ≥0.3 mg/dl (>26,4 µmol/L), o creștere procentuală a creatininei serice de ≥50% (de 1,5 ori față de valoarea inițială) sau o reducere a debitului urinar (oligurie documentată de mai puțin de 0.5 ml/kg pe oră timp de mai mult de șase ore
Proteinuria semnificativă (ACR ≥30 mg/mmol sau PCR ≥50 mg/mmol) în plus față de hematurie ridică suspiciunea de boală renală intrinsecă
Hematurie glomerulară cu macroalbuminurie
Hematurie izolată (i.e, în absența proteinuriei semnificative) cu hipertensiune arterială la cei cu vârsta <40 de ani
Hematurie vizibilă care coincide cu o infecție intercurentă (de obicei a tractului respirator superior)
Sesizare la urologie
Hematurie vizibilă la toți pacienții (indiferent de vârstă)
Pacienți cu orice infecție simptomatică non-vizibilă simptomatică în absența unei infecții urinare sau a altor cauze tranzitorii (indiferent de vârstă)
Pacienți de sex masculin cu hematurie nonvizibilă asimptomatică
Toți pacienții cu hematurie nonvizibilă asimptomatică și alți factori de risc
Tabelul2: Indicații pentru trimitere
† Prezența globulelor roșii dismorfice, a proteinuriei, a mulajelor celulare și/sau a insuficienței renale sau a oricărui alt indicator clinic suspect pentru boala parenchimatoasă renală justifică efectuarea concomitentă a unui bilanț nefrologic, dar nu exclude necesitatea unei evaluări urologice.
‡ Femeile cu hematurie asimptomatică non-vizibilă cu vârsta <40 de ani nu necesită trimitere la urologie.
.
