INLEDNING
Grundläggande och klinisk forskning som utförts under de senaste åren har fastställt att det finns ett direkt dubbelriktat samband mellan kronisk njursjukdom och kardiovaskulär sjukdom.1,2 I den dagliga kliniska praktiken används vanligen serumkreatininkoncentrationer och den glomerulära filtrationshastigheten uppskattad med Cockcroft-Gault3 formeln eller Modification of Diet in Renal Disease (MDRD)4 ekvationen för att uppskatta njurfunktionen. Plasmakreatininkoncentrationer kan dock påverkas av ett antal faktorer, t.ex. patientens ålder, kön, muskelmassa, fysisk aktivitet, kost och medicinering.5
Cystatin C är en proteinhämmare av cysteinkreatininproteas som syntetiseras i en stabil takt av alla cellkärnor. På grund av sin låga molekylvikt och höga isoelektriska punkt kan det elimineras nästan uteslutande genom glomerulär filtration. Cystatin C-koncentrationerna påverkas inte av ålder, kön eller proteinintag, och de är känsliga för små förändringar i glomerulär filtration. På grund av dessa egenskaper anses plasmakoncentrationen av cystatin C vara en av de bästa markörerna för glomerulär filtrationsstatus.6-9 Nyligen har flera studier rapporterat ett samband mellan förhöjda cystatin C-värden och utvecklingen av kardiovaskulära komplikationer hos patienter med kranskärlssjukdom. Man vet för närvarande inte om detta samband beror på att cystatin C är en bättre markör för njurfunktionen än serumkreatinin eller om det finns andra faktorer än glomerulär filtration som påverkar koncentrationen av detta protein och som dessutom är relaterade till kardiovaskulär risk10 .
Syftet med den här studien var att bedöma det prognostiska värdet av plasmakoncentrationen av cystatin C hos patienter som lagts in på sjukhus för akut koronart syndrom (ACS) med hög risk, och att undersöka förhållandet mellan cystatin C och andra markörer för njurfunktion och inflammation.
METODER
Detta är en prospektiv observationsstudie som utfördes mellan maj 2006 och juli 2007. Totalt 203 patienter som var äldre än 18 år och som konsekutivt hade lagts in på hjärtintensivvårdsavdelningen (ICU) vid vårt center med diagnosen högrisk-ACS inkluderades.
De diagnostiska kriterierna för högrisk-ACS omfattade minst två av följande faktorer: smärta med ischemiska kännetecken, elektrokardiografiska förändringar som är förenliga med ischemi och/eller förhöjda markörer för myokardienekros. Den behandling som gavs och de ytterligare tester som utfördes under patientens sjukhusvistelse baserades på den behandlande läkarens kliniska beslut. Hos de flesta patienter användes en invasiv strategi som innebar akut koronarangiografi (för hjärtinfarkt med ST-segmenthöjning eller vänster grenblock) eller tidig planerad koronarangiografi under de första 24 till 72 timmarna efter sjukhusvistelsen.
Kliniska egenskaper
Följande uppgifter registrerades från patienternas kliniska journaler: demografisk information, förekomst av klassiska kardiovaskulära riskfaktorer (diabetes mellitus, systemisk hypertoni, dyslipidemi och rökning) och anamnes på känd kärlsjukdom (ischemisk hjärtsjukdom, cerebrovaskulär sjukdom, perifer artärsjukdom och tidigare myokardiell revaskulariseringsbehandling). De övriga kliniska variabler som analyserades omfattade typ av ACS, Killip-klass vid tidpunkten för sjukhusvistelsen, systoliska och diastoliska tryckvärden, pulstryck (uppskattat som skillnaden mellan systoliskt och diastoliskt arteriellt tryck) och hjärtfrekvens.
Alla patienter genomgick ekokardiografi, där den vänstra ventrikulära ejektionsfraktionen skattades med Simpson-metoden med hjälp av en 4-kammarmetod; medelvärdet av 3 bestämningar beräknades hos patienter med sinusrytm och medelvärdet av 5 bestämningar hos dem med förmaksflimmer.
I 95 % av patienterna utfördes koronarangiografi, och allvarlighetsgraden av kranskärlslesionerna utvärderades med en poäng baserad på antalet drabbade epikardiella kranskärl.
Analytiska data
Baslinjevärden för hemoglobin, hematokrit, leukocyter, glukos och kreatinin registrerades i de första laboratorieanalyserna som utfördes på vårt center vid tidpunkten för sjukhusvistelsen. Koncentrationer av totalkolesterol, högdensitetslipoproteinkolesterol (HDL-C), lågdensitetslipoproteinkolesterol (LDL-C), glukos, högkänsligt C-reaktivt protein och cystatin C registrerades under de första 24 timmarna, tillsammans med den högsta nivån av troponin I (TpI).
Cystatin C mättes med ett automatiserat homogent immunoassay med hjälp av en Dade-Behring BN ProSpec nefelometer. Reagenset för analysen bestod av polystyrenpartiklar belagda med antikroppar mot proteinet som agglutinerar när de blandas med prover som innehåller cystatin C och sprider ljus med en intensitet som är proportionell mot koncentrationen av analyten.
Referensintervallet för serumkoncentrationen av cystatin C hos vuxna med den använda nefelometriska metoden är 0,51 till 0,95 mg/L. Koncentrationer av högkänsligt C-reaktivt protein bestämdes också genom immunoassay. Den glomerulära filtrationshastigheten uppskattades med MDRD-ekvationen.
Episoder som analyserades
De kardiovaskulära komplikationer som analyserades omfattade dödlighet på sjukhus, dödlighet av alla orsaker under uppföljning, utveckling av en ny hjärtinfarkt, definierad som bröstsmärta eller likvärdig ångestsmärta med EKG-förändringar, eller förhöjda tumörnekrosmarkörer under de första 24 timmarna efter sjukhusvistelse (patienter med förhöjda markörer efter kranskärlsinterventionella ingrepp exkluderades), och utveckling av hjärtsvikt under sjukhusvistelse eller uppföljning.
Klinisk uppföljning
Den genomsnittliga uppföljningen var 186 (SD, 110; median, 156) dagar, under vilken tid alla patienternas kliniska händelser registrerades. Uppföljningen utfördes genom telefonkontakt, på öppenvårdskliniker och genom granskning av patienternas sjukhusjournaler.
Statistisk analys
Alla uppgifter registrerades prospektivt i en databas som skapades med Microsoft Office Access 2003 SP2. De statistiska analyserna utfördes med SPSS (Statistical Package for the Social Sciences), version 12.0. De kategoriska eller dikotoma variablerna uttrycks som absoluta värden och procentandelar och jämfördes med Pearson χ2-testet. De kontinuerliga variablerna med normalfördelning beskrivs som medelvärde (SD), och Student t-testet användes för jämförelser mellan grupper. Variabler som inte uppvisade en gaussisk fördelning jämfördes med Mann-Whitney U-testet.
Spearmans korrelationskoefficient användes för att utvärdera korrelationerna mellan cystatin C-koncentrationen och högkänsligt C-reaktivt protein och glomerulär filtrationshastighet. En logistisk regressionsanalys användes för att bedöma den oberoende rollen av kliniska och laboratoriefaktorer med avseende på cystatin C för att förutsäga utvecklingen av kardiovaskulära komplikationer under sjukhusvistelse, inklusive de signifikanta variablerna i den univariata analysen. De justerade oddskvoterna och 95 % konfidensintervallen (CI) presenteras. Kaplan-Meier överlevnadskurvor under uppföljningen konstruerades och jämfördes med hjälp av long-rank-testet.
För att genomföra en deskriptiv analys av den studerade populationen kategoriserades vissa kvantitativa variabler i intervall: den glomerulära filtrationshastigheten (>90, 90-60, 55 % och 0,95 och
Ett P-värde mindre än 0,05 ansågs vara statistiskt signifikant.
RESULTAT
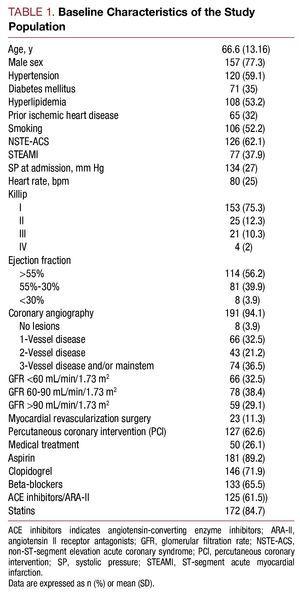
Från maj 2006 till juli 2007 ingick 203 patienter som lagts in på sjukhus med diagnosen högrisk-ACS i studien. Medelåldern var 66,6 (13,16) år. Av de totala patienterna uppvisade 62,1 % (n=126) ACS utan ST-segmenthöjning och 37,9 % (n=77) ACS med ST-segmenthöjning. Studiepopulationens baslinjegenskaper beskrivs i tabell 1.
Mediankoncentrationen av cystatin C var 1,01 (intervall, 0,83-1,35) mg/L, plasmakreatinin vid den första analysen som utfördes var 1 (0.9-1,3) mg/L, glomerulär filtrationshastighet var 72,4 (49,12-93,73) mL/min/1,73 m2 och högkänsligt C-reaktivt protein var 1,37 (0,46-5,02) mg/L. Glomerulär filtration vid tidpunkten för sjukhusvistelsen var 2 hos 32,5 % av patienterna och serumcystatin C var >0,95 mg/L hos 113 (55,7 %) patienter.
Patienter med högre cystatin C-värden uppvisade en sämre klinisk profil, var äldre, hade en hög prevalens av hypertoni, sämre Killip-klass vid tidpunkten för sjukhusvistelsen, allvarligare kranskärlssjukdom vid koronarangiografi och högre värden för plasmakreatinin och C-reaktivt protein (tabell 2).
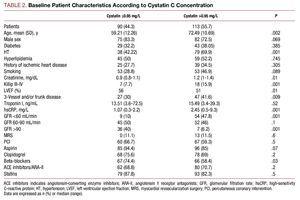
Det fanns inga signifikanta skillnader mellan de 2 cystatin C-grupperna när det gällde den utförda koronarinterventionen; det slutliga angiografiska resultatet gav en liknande framgångsfrekvens och inga signifikanta komplikationer (3,27 % för patienter med cystatin C ≤0,95 och 4,09 % i den andra gruppen). Analysen av den farmakologiska behandlingen visade en betydligt högre användning av betablockerare och aspirin i gruppen med cystatin C ≤0,95 (tabell 2).
Serumvärden för cystatin C visade en högre korrelation med uppskattad glomerulär filtrationshastighet (r=-0,655; P=,001) (figur 1) än med mikroalbuminuri (r=0,302, P=,01) och en lägre korrelation med C-reaktivt protein (r=0,29; P=,01).
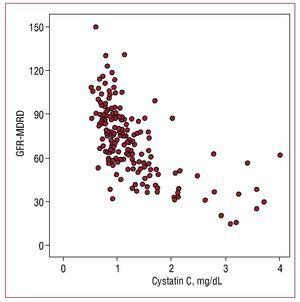
Figur 1. Korrelation mellan cystatin C-värden och glomerulär filtrationshastighet uppskattad med MDRD-formeln (GFR-MDRD).
I gruppen patienter med cystatin C-värden >0,95 uppvisade 6,5 % normala glomerulära filtrationshastigheter och 46 %, glomerulära filtrationshastigheter mellan 60 och 90 mL/min/1,73 m2. Dessutom hade 10 % av de patienter som hade njurdysfunktion med en filtrationshastighet på 2 cystatin C-värden
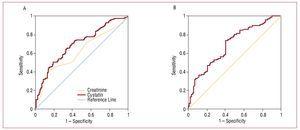
Figur 2. A, ROC för cystatin C och kreatinin i förhållande till utvecklingen av kardiovaskulära komplikationer (hjärtsvikt, infarkt och kardiovaskulär död). B, ROC-kurva för glomerulär filtrationshastighet uppskattad med MDRD i förhållande till utvecklingen av kardiovaskulära komplikationer (hjärtsvikt, infarkt och kardiovaskulär död).
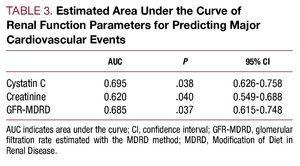
Sjukhusvistelsen varade i median 9 (6-19) dagar. Från intagningstillfället till slutförandet av studieuppföljningen hade 56 (27,58 %) patienter från det totala urvalet utvecklat hjärtsvikt, de flesta av dem i gruppen med förhöjda cystatin C-värden (45 patienter). Dödligheten på sjukhus var betydligt högre i gruppen med förhöjda cystatin C-värden (17,6 % jämfört med 3,3 %; P=.001), och dessa skillnader kvarstod under uppföljningen (figur 3, tabell 4).
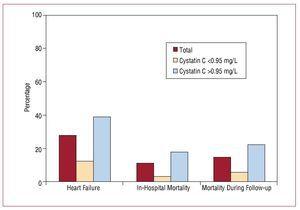
Figur 3. Samband mellan cystatin C 0,95 mg/L och utveckling av kardiovaskulära händelser på sjukhus.

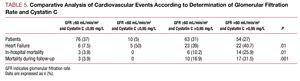
I den univariata analysen observerades inget samband mellan kardiovaskulära komplikationer och typen av ACS, hyperlipidemi eller toppkoncentrationen av TpI, men ett samband hittades med de återstående kardiovaskulära riskfaktorerna: antal drabbade kärl, ejektionsfraktion, njurfunktionsmarkörer, cystatin C och högkänsligt C-reaktivt protein. När resultaten från patienter med en glomerulär filtrationshastighet på >60 ml/min/1,73 m2 analyserades fann vi att patienter med cystatin C >0.95 mg/L uppvisade en signifikant högre frekvens av kardiovaskulära komplikationer än patienter med glomerulär filtration >60 och cystatin C 60 och cystatin C
Skattad händelselös överlevnad (dvs. ingen hjärtsvikt, hjärtinfarkt eller död) efter en genomsnittlig uppföljning på 186 dagar var signifikant högre i gruppen av patienter med cystatinvärden ≤0.95 mg/L: 75 % jämfört med 44 % (P=.02) (figur 4).

Figur 4. Kaplan-Meier-kurvor för att uppskatta sannolikheten för överlevnad utan större kardiovaskulära händelser, beroende på cystatin C-värde.
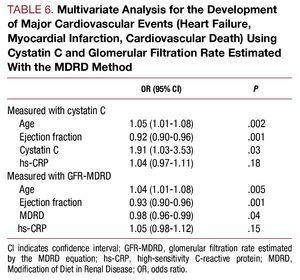
Den multivariata analysen identifierade ålder, ejektionsfraktion och cystatin C-koncentration som oberoende prediktiva faktorer för kardiovaskulära komplikationer under sjukhusvistelse (tabell 6).
DISKUSSION
Resultaten av den här studien visar att förhöjda cystatin C-värden förutspår utvecklingen av hjärtsvikt, hjärtinfarkt och kardiovaskulär död under sjukhus hos patienter med högrisk-ACS, oberoende av andra klassiska riskfaktorer. Dessutom kan plasma cystatin C värde ha en större förmåga att stratifiera patienter med hög risk för kardiovaskulära komplikationer under sjukhusvistelse än andra metoder för att bedöma njurfunktionen. Vi fann att förhöjt cystatin C var förknippat med en sämre kardiovaskulär prognos även i gruppen av patienter med normal glomerulär filtration. Såvitt vi vet är detta den första rapporten om detta samband, vilket vi tror kan få konsekvenser för riskstratifiering i denna patientpopulation.
Under de senaste åren har flera artiklar beskrivit ett nära samband mellan njurdysfunktion och kardiovaskulära komplikationer vid uppföljning av patienter med akut och kronisk ischemisk hjärtsjukdom samt andra kliniska presentationer av kardiovaskulära sjukdomar, i synnerhet hjärtsvikt.1,10-12 En minskning av den glomerulära filtrationen till under 60 ml/min är relaterad till en signifikant ökning av risken för dödsfall, hjärtinfarkt och stroke, både hos patienter med eller utan tidigare kardiovaskulär sjukdom.13 Specifikt har detta samband beskrivits hos ACS-patienter med ST-segmenthöjning och patienter utan.10,13-15 I VALIANT-studien16 (patienter med ventrikeldysfunktion och hjärtsvikt efter ST-segmenthöjning av hjärtinfarkt) var försämring av njurfunktionen (bedömd med den glomerulära filtrationshastigheten) förknippad med en ökning av dödlighet och kardiovaskulära komplikationer under uppföljningen. Liknande resultat har rapporterats för de patientpopulationer som ingår i studierna SAVE (ventrikeldysfunktion efter infarkt), HOPE (patienter med hög kardiovaskulär risk, majoriteten med kronisk ischemisk hjärtsjukdom) och PEACE (patienter med kronisk ischemisk hjärtsjukdom). I dessa studier observerades sambandet mellan njurdysfunktion och prognos för minskad glomerulär filtrationshastighet och för albuminutsöndring i urinen.16-19
Som nämnts ovan har ett direkt dubbelriktat samband beskrivits mellan njurdysfunktion och kardiovaskulär sjukdom. Kronisk njursvikt gynnar utvecklingen av hypertoni och dyslipidemi och främjar aktivering av renin-angiotensinaldosteronsystemet. Dessa faktorer, tillsammans med ökningen av inflammatoriska mediatorer, verkar bidra till en högre produktion av fria radikaler, som påverkar den aterosklerotiska processen och kardiovaskulära skador. Dessutom gynnar förändringar i mineralmetabolismen (ökning av främjare och minskning av hämmare av förkalkning) kalkavlagringar i kranskärlen.20,21 Slutligen har man beskrivit en mindre intensiv användning av terapeutiska interventioner med erkända kliniska och prognostiska fördelar hos patienter med njurdysfunktion. Särskilt hos dem med ACS kan mindre aggressiv behandling och längre fördröjning av interventionella kranskärlsprocedurer samt lägre användning av IIb/IIIa, blockerare av reninangiotensin-aldosteron-axeln, betablockerare, statiner och trombocythämmare bidra till den sämre prognos som beskrivits i denna patientpopulation.22
I den dagliga kliniska praktiken baseras bedömningen av njurfunktionen vanligtvis på serumkreatininbestämningar och uppskattningar av den glomerulära filtrationshastigheten med hjälp av Cockcroft-Gault- eller MDRD-formlerna. Båda dessa metoder har flera begränsningar, varav många härrör från faktorer som påverkar kreatininproduktionen, t.ex. ålder, kvinnligt kön, rasrelaterade egenskaper, kost och förlopp av kroniska sjukdomar.
Dessa ekvationer utvärderades nyligen hos patienter med hjärtsvikt och jämfördes med NT-proBNP, en prognostisk markör. Den prognostiska information som NT-proBNP ger visade sig vara överlägsen den prognostiska informationen från njurfunktionen som uppskattas med MDRD-formeln.23
Cystatin C har molekylära och metaboliska egenskaper som gör plasmakoncentrationerna av detta protein till en bra biologisk markör för uppskattning av njurfunktionen; små funktionsförändringar upptäcks med högre känslighet än de konventionella parametrar som används för detta ändamål.24 Detta kan motivera det faktum att i gruppen av patienter med serumkoncentrationer av cystatin C över den övre normalgränsen uppvisade 15 % en normal glomerulär filtrationshastighet; bestämning av cystatin C kan vara användbart för att identifiera patienter med ett prekliniskt tillstånd av njursjukdom.6
De resultat som erhållits i den aktuella studien stämmer i viss mån överens med de rapporterade resultat som visar att cystatin C är en oberoende prediktor för kardiovaskulära komplikationer hos patienter med kranskärlssjukdom.25-27 Dessutom kan våra data utvidga detta koncept till att omfatta patienter med normal glomerulär filtrationshastighet. Jernberg et al26 analyserade förhållandet mellan plasmavärden av cystatin C och prognos i en grupp patienter som lagts in på sjukhus för ACS utan ST-segmentelevation och rapporterade ett signifikant samband mellan cystatin C-värden och mortalitet. Det har också beskrivits att förhöjda cystatin C-koncentrationer är förknippade med en ökad risk för död, kardiovaskulära komplikationer och förekomsten av hjärtsvikt hos polikliniska patienter med kronisk kranskärlssjukdom.24 Hos äldre personer utan manifest njursjukdom är cystatin C en riskmarkör för död, kardiovaskulära sjukdomar och kronisk njursjukdom.6 I den aktuella studien fann vi att patienter med förhöjda cystatin C-nivåer hade en sämre riskprofil; den relativt låga nivån av C-reaktivt protein var dock överraskande. Vi tror att detta kan förklaras av proteinets kinetik, som har ett specifikt, karakteriserat spektrum där värdet beror på den tidpunkt då provet tas (toppen inträffar 49 timmar efter symtomdebut, och en mer fördröjd topp ses vid akut hjärtinfarkt med ST-segmenthöjning); i vår studie togs proverna inom de första 24 timmarna efter sjukhusvistelsen28. De kardiovaskulära komplikationer som drabbade patienterna i vår studie skiljer sig från dem som publicerats i nyligen publicerade register,29 och detta kan bero på att patienter med mycket hög risk och med högre förekomst av komplikationer inkluderades. I det nyligen publicerade MASCARA-registret hade endast 50 % av de inkluderade patienterna initialt lagts in på en intensivvårdsavdelning eller hjärtintensivvårdsavdelning, medan alla våra patienter kom från en hjärtintensivvårdsavdelning, ett faktum som utan tvekan innebär en viss selektionsbias. Icke desto mindre bestod patientgruppen med förhöjt cystatin C av en population med en betydligt högre riskprofil och antal kardiovaskulära komplikationer än de övriga patienterna. Den aktuella studien bidrar till att etablera större precision i dessa associationer genom att ge den första rapporten om att förhöjda cystatin C-nivåer under de första timmarna av sjukhusvistelse för högrisk-ACS är en oberoende prediktor för kardiovaskulära komplikationer under sjukhusvistelse. Dessutom är sambandet mellan cystatin C och en risk för kardiovaskulära komplikationer högre än för andra allmänt använda parametrar för att uppskatta njurfunktionen, och bibehålls även i gruppen av patienter med normal glomerulär filtration. För närvarande vet man inte exakt om förmågan att förutsäga en högre risk för komplikationer beror på att cystatin C är en bättre markör för njurfunktionen än andra vanliga parametrar (serumkreatinin och glomerulär filtrationshastighet), eller om det finns andra faktorer förutom glomerulär filtration som påverkar cystatin C-koncentrationen och som skulle kunna vara direkt relaterade till kardiovaskulär risk. I denna linje har man beskrivit en positiv korrelation mellan plasmavärden av C-reaktivt protein och fibrinogen med förhöjda cystatin C-koncentrationer och förekomsten av kardiovaskulär sjukdom.30 I PRIME-studien (Prospective Epidemiological Study of Myocardial Infarction) undersöktes sambandet mellan cystatin C och utveckling av akut hjärtinfarkt hjärtdöd och angina pectoris hos patienter utan kranskärlssjukdom. Efter justering för de vanliga kardiovaskulära riskfaktorerna var plasmanivån av cystatin C signifikant förknippad med utvecklingen av den första koronarkomplikationen av ischemiskt ursprung. Författarna ansåg att den minskade glomerulära filtrationshastigheten inte skulle rättfärdiga de högre cystatin C-värden som fallen uppvisade i förhållande till kontrollerna, och de föreslog att inflammation skulle kunna ligga till grund för sambandet mellan cystatin C och risken för kardiovaskulär sjukdom31,32 . I linje med dessa uppgifter visade våra resultat en positiv korrelation mellan cystatin C och högkänsligt C-reaktivt protein (r=0,2), som också är en oberoende prediktor för kardiovaskulära komplikationer, och ger ytterligare bevis för att motivera förekomsten av direkta samband mellan njursjukdom, inflammation och kardiovaskulära sjukdomar.
Enligt de viktigaste begränsningarna i den presenterade studien bör vi påpeka att resultaten endast avser patienter med ACS med hög risk som lagts in på en hjärtintensivvårdsavdelning, varav majoriteten behandlades aggressivt med tidig koronarangiografi. Å andra sidan bör dessa egenskaper lyftas fram, eftersom det finns lite information om denna specifika population, där cystatin C mättes vid sjukhusintag. I nästan alla publicerade studier anges inte tidpunkten för bestämningarna, och åtminstone hos patienter med ACS kan plasmakoncentrationerna av cystatin C påverkas av den tid som förflutit sedan händelsen och de diagnostiska och terapeutiska ingrepp som utförts. Begränsningen i form av en kort uppföljning gör det omöjligt att utvidga våra observationer till att gälla på medellång eller lång sikt. Icke desto mindre erbjuder våra resultat en möjlighet att förbättra riskstratifieringen hos patienter som lagts in på sjukhus för ACS med hög risk, vilket kommer att vara användbart för att besluta om terapi samt för att fastställa diagnosen.
SLUTSATSER
Cystatin C-bestämning vid sjukhusvistelse hos patienter med ACS med hög risk kan vara ett bra kliniskt verktyg för stratifiering av kardiovaskulär risk. Bestämning av detta protein skulle komplettera den information som ges av andra metoder för att bedöma njurfunktionen och skulle, förutom de diagnostiska implikationerna, kunna vara användbar för att identifiera gruppen med högst risk. Det kan vara nödvändigt att ägna särskild uppmärksamhet åt att uppfylla rekommendationerna i riktlinjerna för klinisk praxis i denna population. Dessutom kan cystatin C bidra med viktig information för att stratifiera patienter med hög risk för ACS och bevarad njurfunktion. Ytterligare studier med längre uppföljning kan behövas för att definiera cystatin C:s roll vid ACS med större precision.
AVKORTNINGAR
ACS: akut koronart syndrom
MDRD: Modification of Diet in Renal Disease
TpI: troponin I
.
