![]()
Personer som använder hjälpmedel kanske inte har full tillgång till informationen i denna fil. För hjälp, skicka e-post till: [email protected]. Skriv 508 Accommodation och rapportens titel i e-postens ämnesrad.
![]() PDF
PDF
Den rådgivande kommittén för vaccinationspraxis (Advisory Committee on Immunization Practices, ACIP) ser årligen över det rekommenderade vaccinationsschemat för vuxna för att se till att schemat återspeglar aktuella rekommendationer för användning av licensierade vacciner. I juni 2005 godkände ACIP vaccinationsschemat för vuxna för oktober 2005-september 2006. Detta schema har också godkänts av American Academy of Family Physicians och American College of Obstetricians and Gynecologists.
Förändringar i schemat för oktober 2005-september 2006
Schemat för 2005-2006 skiljer sig från det tidigare schemat på följande sätt:
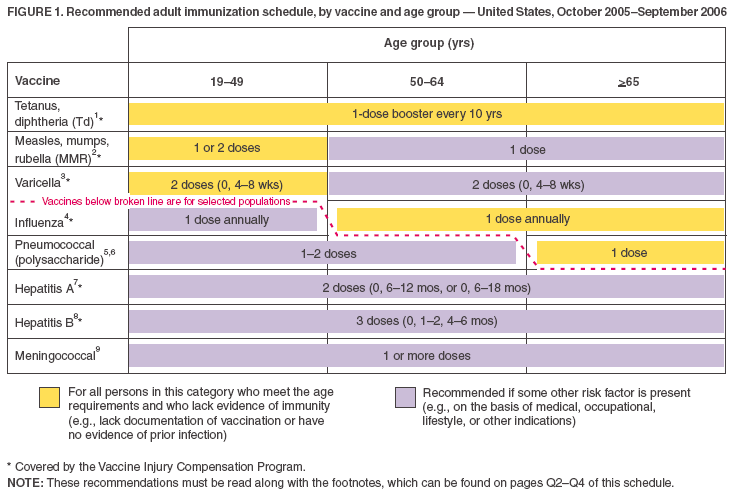
- Vacciner som anges i det åldersbaserade schemat (figur 1) visas så att de vacciner som rekommenderas för rutinanvändning kan särskiljas från dem som rekommenderas för vuxna med vissa riskindikatorer (i likhet med vaccinationsschemat för barn). Detta illustreras både av färgschemat och av den streckade linjen.
- De gula staplarna (”För alla personer i denna grupp”) och de gröna staplarna (”För personer som saknar dokumentation av vaccination eller bevis på sjukdom”) från det tidigare schemat har slagits samman till en gul stapel, som nu lyder: ”För alla personer i denna kategori som uppfyller ålderskraven och som saknar bevis på immunitet (t.ex, saknar dokumentation om vaccination eller saknar bevis på tidigare infektion).”
- Den lila stapeln har ändrats från ”För personer i riskzonen (t.ex. med medicinska indikationer/exponeringsindikationer)” till ”Rekommenderas om någon annan riskfaktor föreligger (t.ex. på grundval av medicinska, yrkesmässiga, livsstilsrelaterade eller andra indikationer)”. Det lila strecket har lagts till i kolumnerna för åldersgrupperna 50–64 år och >65 år för vaccin mot mässling, påssjuka och röda hund (MMR).
- Kolumnen ”Diabetes, hjärtsjukdom, kronisk lungsjukdom eller kronisk leversjukdom inklusive kronisk alkoholism” har flyttats om med kolumnen ”Medfödd immunbrist, leukemi, lymfom, generaliserad malignitet, behandling med alkylerande medel, antimetaboliter, läckage av cerebrospinalvätska, strålning eller stora mängder kortikosteroider” på schemat för medicinska/annan indikationer (figur 2) så att kontraindikationerna för MMR- och varicellavaccinationer nu står sida vid sida.
- Raden för varicellavaccin har flyttats upp på båda figurerna (dvs, till omedelbart efter MMR-vaccinet) eftersom vaccinet nu rekommenderas allmänt för vissa åldersgrupper.
- Meningokockvaccin har lagts till i schemat för medicinska/andra indikationer (figur 2). Fotnoten har reviderats för att införliva de nyligen publicerade ACIP-rekommendationerna för detta vaccin (1).
- Fotnoten om stelkramp och difteri (#1) har omformulerats.
- Fotnoten om varicella (#3) har omformulerats i enlighet med de ACIP-rekommendationer som antogs i juni 2005.
- Fotnoten om influensa (#4) har omarbetats för att lägga till det nyaste högrisktillståndet: neuromuskulära tillstånd som äventyrar andningsfunktionen (2).
- En tionde fotnot har lagts till om vaccination mot Haemophilus influenzae typ b för befolkningsgrupper med hög risk (dvs, personer med aspleni, leukemi och infektion med humant immunbristvirus).
Vuxenvaccinationsplanen finns på engelska och spanska på http://www.cdc.gov/nip/recs/adult-schedule.htm. Allmän information om vaccinering av vuxna, inklusive rekommendationer om vaccination av personer med hiv och andra immunosuppressiva tillstånd, finns tillgänglig från delstatliga och lokala hälsovårdsmyndigheter och från det nationella vaccinationsprogrammet på http://www.cdc.gov/nip. Vaccininformationsmeddelanden finns tillgängliga på http://www.cdc.gov/nip/publications/vis. ACIP-utlåtanden för varje rekommenderat vaccin kan ses, laddas ner och skrivas ut från National Immunization Programs webbplats på http://www.cdc.gov/nip/publications/acip-list.htm. Instruktioner för rapportering av biverkningar till Vaccine Adverse Event Reporting System finns på http://www.vaers.hhs.gov eller per telefon, 800-822-7967.
- CDC. Förebyggande och kontroll av meningokocksjukdomar: rekommendationer från rådgivande kommittén för immuniseringspraxis (ACIP). MMWR 2005;54(nr RR-7).
- CDC. Förebyggande och kontroll av influensa: rekommendationer från rådgivande kommittén för immuniseringspraxis (ACIP). MMWR 2005;54(nr RR-8).
Figur 1
Return to top.
Figur 2

Return to top.
Godkänd av Advisory Committee on Immunization Practices, American College of Obstetricians and Gynecologists och American Academy of Family Physicians
1. Vaccination mot stelkramp och difteri (Td). Vuxna med osäkra historier av en fullständig primärvaccinationsserie med difteri och tetanustoxoid-innehållande vacciner bör få en primär serie med kombinerad Td-toxoid. En primär serie för vuxna består av tre doser; de två första doserna ges med minst fyra veckors mellanrum och den tredje dosen ges 6-12 månader efter den andra. Administrera 1 dos om personen har fått den primära serien och om den senaste vaccineringen gjordes >10 år tidigare. Se ACIP-utlåtandet för rekommendationer för administrering av Td som profylax vid sårbehandling (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). American College of Physicians Task Force on Adult Immunization stöder ett andra alternativ för användning av Td hos vuxna: en enda Td-booster vid 50 års ålder för personer som har genomgått hela den pediatriska serien, inklusive boostern för tonåringar/unga vuxna. Ett nyligen godkänt vaccin mot tetanus, difteri och cellulär kikhosta finns tillgängligt för vuxna. ACIP:s rekommendationer för dess användning kommer att publiceras.
2. Vaccination mot mässling, påssjuka och röda hund (MMR). Mässlingskomponent: Vuxna som är födda före 1957 kan anses vara immuna mot mässling. Vuxna som är födda under eller efter 1957 bör få >1 dos MMR om de inte har en medicinsk kontraindikation, dokumentation av >1 dos, anamnes på mässling baserat på vårdgivarens diagnos eller laboratoriebevis på immunitet. En andra dos MMR rekommenderas för vuxna som 1) nyligen exponerats för mässling eller i samband med ett utbrott, 2) tidigare vaccinerats med avdödat mässlingsvaccin, 3) vaccinerats med en okänd typ av mässlingsvaccin under 1963–1967, 4) studerar vid postsekundära utbildningsinstitutioner, 5) arbetar vid en sjukvårdsinrättning eller 6) planerar att resa internationellt. Avstå från MMR-vaccin eller andra vaccin som innehåller mässling från hiv-infekterade personer med allvarlig immunosuppression. Mumps-komponent: 1 dos MMR-vaccin bör vara tillräckligt skydd för personer som är födda under eller efter 1957 och som inte har en historia av påssjuka baserad på en diagnos från hälso- och sjukvårdspersonal eller som saknar laboratoriebevis för immunitet. Rubellakomponent: 1 dos MMR-vaccin ska administreras till kvinnor vars vaccinationshistorik mot rubella är otillförlitlig eller som saknar laboratoriebevis för immunitet. För kvinnor i fertil ålder, oavsett födelseår, ska man rutinmässigt fastställa immunitet mot röda hund och ge kvinnor råd om medfött röda hund-syndrom. Vaccinera inte kvinnor som är gravida eller som kan bli gravida inom 4 veckor efter att ha fått vaccinet. Kvinnor som inte har bevis på immunitet bör få MMR-vaccin vid avslutad eller avslutad graviditet och innan de skrivs ut från vårdinrättningen.
3. Vaccination mot vattkoppor. Vaccination mot varicella rekommenderas för alla vuxna utan bevis på immunitet mot varicella. Särskild hänsyn bör tas till dem som 1) har nära kontakt med personer med hög risk för allvarlig sjukdom (hälso- och sjukvårdspersonal och familjekontakter till personer med nedsatt immunförsvar) eller 2) löper hög risk att utsättas för exponering eller överföring (t.ex. lärare som undervisar små barn, barnomsorgspersonal, boende och personal i institutionella miljöer, inklusive kriminalvårdsanstalter, högskolestudenter, militärpersonal, ungdomar och vuxna som bor i hushåll med barn, icke-gravida kvinnor i fertil ålder och internationella resenärer). Bevis på immunitet mot varicella hos vuxna omfattar något av följande: 1) Dokumenterad åldersanpassad varicellavaccination (dvs. 1 dos före 13 års ålder eller 2 doser efter 13 års ålder). 2) Född i USA före 1966 eller anamnes på varicella före 1966 för personer som inte är födda i USA.3) anamnes på varicella baserat på en diagnos från hälso- och sjukvårdspersonal eller föräldrarnas eller egen anmälan om typisk varicellasjukdom för personer födda 1966-1997 (för en patient som rapporterar en anamnes på ett atypiskt, lindrigt fall bör hälso- och sjukvårdspersonal söka antingen en epidemiologisk koppling till ett typiskt varicellafall eller bevis på laboratoriebekräftelse, om den utfördes vid tiden för den akuta sjukdomen), 4) anamnes på herpes zoster baserat på en diagnos från hälso- och sjukvårdspersonal eller 5) laboratoriebekräftelse på immunitet. Vaccinera inte kvinnor som är gravida eller som kan bli gravida inom 4 veckor efter att ha fått vaccinet. Bedöm gravida kvinnor för bevis på varicellaimmunitet. Kvinnor som inte har bevis på immunitet ska få dos 1 av varicellavaccin när graviditeten avslutas eller avslutas och innan de skrivs ut från vårdinrättningen. Dos 2 ska ges 4-8 veckor efter dos 1.
4. Influensavaccination. Medicinska indikationer: kroniska sjukdomar i det kardiovaskulära eller pulmonella systemet, inklusive astma; kroniska metaboliska sjukdomar, inklusive diabetes mellitus, njurdysfunktion, hemoglobinopatier eller immunosuppression (inklusive immunosuppression orsakad av läkemedel eller hiv); alla tillstånd (t.ex, kognitiv dysfunktion, ryggmärgsskada, krampsjukdom eller annan neuromuskulär sjukdom) som försämrar andningsfunktionen eller hanteringen av andningssekret eller som kan öka risken för aspiration, samt graviditet under influensasäsongen. Det finns inga uppgifter om risken för allvarlig eller komplicerad influensasjukdom hos personer med aspleni, men influensa är en riskfaktor för sekundära bakterieinfektioner som kan orsaka allvarlig sjukdom hos personer med aspleni. Yrkesindikationer: Hälso- och sjukvårdspersonal och anställda vid anläggningar för långtidsvård och vårdboende. Andra indikationer: Invånare på vårdhem och andra anläggningar för långtidsvård och stödboende, personer som sannolikt kan överföra influensa till personer med hög risk (dvs. hushållskontakter i hemmet och vårdare av barn i åldern 0-23 månader eller personer i alla åldrar med högrisktillstånd) och alla som vill bli vaccinerade. För friska, icke-gravida personer i åldern 5-49 år utan högrisktillstånd som inte är kontaktpersoner till allvarligt immunsupprimerade personer på specialavdelningar kan intranasalt administrerat influensavaccin (FluMist®) administreras i stället för inaktiverat vaccin.
5. Vaccination mot pneumokockpolysackarid. Medicinska indikationer: kroniska sjukdomar i lungsystemet (utom astma), hjärt- och kärlsjukdomar, diabetes mellitus, kroniska leversjukdomar, inklusive leversjukdom till följd av alkoholmissbruk (t.ex. cirros), kronisk njursvikt eller nefrotiskt syndrom, funktionell eller anatomisk aspleni (t.ex, sicklecellsjukdom eller splenektomi), immunosuppressiva tillstånd (t.ex. medfödd immunbrist, hiv-infektion, leukemi, lymfom, multipelt myelom, Hodgkins sjukdom, generaliserad malignitet eller organ- eller benmärgstransplantation), kemoterapi med alkylerande medel, antimetaboliter eller långvariga systemiska kortikosteroider, och cochleaimplantat. Andra indikationer: Andra indikationer: Alaska Natives och vissa indianpopulationer, boende på vårdhem och andra långtidsvårdsinrättningar.
6. Revaccination med pneumokockpolysackaridvaccin. Engångsrevaccination efter 5 år för personer med kronisk njursvikt eller nefritiskt syndrom; funktionell eller anatomisk aspleni (t.ex. sicklecellsjukdom eller splenektomi); immunosuppressiva tillstånd (t.ex, medfödd immunbrist, hiv-infektion, leukemi, lymfom, multipelt myelom, Hodgkins sjukdom, generaliserad malignitet eller organ- eller benmärgstransplantation) eller kemoterapi med alkylerande medel, antimetaboliter eller långvariga systemiska kortikosteroider. För personer i åldern >65 år, engångsrevaccination om de vaccinerades >5 år tidigare och var i åldern <65 år vid tidpunkten för primärvaccinationen.
7. Hepatit A-vaccination. Medicinska indikationer: Personer med koagulationsfaktorsjukdomar eller kronisk leversjukdom. Beteendeindikationer: Män som har sex med män eller användare av illegala droger. Yrkesmässiga indikationer: Personer som arbetar med hepatit A-virus (HAV)-infekterade primater eller med HAV i forskningslaboratorier. Andra indikationer: Personer som reser till eller arbetar i länder med hög eller medelhög endemicitet för hepatit A (för en förteckning över länder, se http://www.cdc.gov/travel/diseases.htm#hepa) samt personer som önskar erhålla immunitet. De nuvarande vaccinerna bör administreras i en tvådosserie vid antingen 0 och 6–12 månader eller 0 och 6–18 månader. Om det kombinerade hepatit A- och hepatit B-vaccinet används ska 3 doser administreras vid 0, 1 och 6 månader.
8. Vaccination mot hepatit B. Medicinska indikationer: Hemodialyspatienter (använd särskild formulering eller två doser på 20 µg/mL) eller patienter som får koagulationsfaktorkoncentrat. Yrkesindikationer: Hälso- och sjukvårdspersonal och personal inom den offentliga säkerheten som exponeras för blod på arbetsplatsen samt personer som utbildar sig inom läkar-, tandläkar-, sjuksköterske-, laboratorieteknik- och andra närliggande hälsovårdsyrken. Beteendeindikationer: Injektionsmissbrukare, personer med mer än en sexpartner under de senaste sex månaderna, personer med en nyligen förvärvad sexuellt överförbar sjukdom (STD) och män som har sex med män. Andra indikationer: hushållskontakter och sexpartners till personer med kronisk infektion med hepatit B-virus (HBV), klienter och personal på institutioner för utvecklingsstörda personer, alla klienter på STD-kliniker, intagna i kriminalvårdsanstalter och internationella resenärer som kommer att vistas i länder med hög eller medelhög förekomst av kronisk HBV-infektion i mer än 6 månader (för en förteckning över länder, se http://www.cdc.gov/travel/diseases.htm#hepa).
9. Meningokockvaccination. Medicinska indikationer: Vuxna med anatomisk eller funktionell aspleni eller terminal komplementkomponentbrist. Andra indikationer: Förstaårsstudenter som bor i studenthem, mikrobiologer som rutinmässigt utsätts för isolat av Neisseria meningitidis, militära rekryter; och personer som reser till eller är bosatta i länder där meningokocksjukdom är hyperendemisk eller epidemisk (t.ex. ”meningitbältet” i Afrika söder om Sahara under torrperioden), särskilt om kontakten med lokalbefolkningen kommer att vara långvarig. Vaccination krävs av Saudiarabiens regering för alla resenärer till Mecka under den årliga Hajj. Meningokockkonjugatvaccin är att föredra för vuxna som uppfyller någon av ovanstående indikationer och som är <55 år, även om meningokockpolysackaridvaccin (MPSV4) är ett godtagbart alternativ. Revaccination efter 5 år kan vara indicerat för vuxna som tidigare vaccinerats med MPSV4 och som fortfarande löper hög risk för infektion (t.ex. personer som bor i områden där sjukdomen är epidemisk).
10. Utvalda tillstånd för vilka vaccin mot Haemophilus influenzae typ b (Hib) kan användas. Hib-konjugatvaccin är godkänt för barn i åldern 6–71 månader. Det finns inga uppgifter om effekt som kan ligga till grund för en rekommendation om användning av Hib-vaccin för äldre barn och vuxna med kroniska sjukdomar som är förknippade med en ökad risk för Hib-sjukdom. Studier tyder dock på god immunogenicitet hos patienter som har sicklecellsjukdom, leukemi eller HIV-infektion eller som har genomgått splenektomi; administrering av vaccin till dessa patienter är inte kontraindicerat.
Det rekommenderade vaccinationsschemat för vuxna har godkänts av Advisory Committee on Immunization Practices, American College of Obstetricians and Gynecologists och American Academy of Family Physicians. MMWR:s standardformat för fotnoter har ändrats för publicering av detta schema.
Föreslagna citat: Centers for Disease Control and Prevention. Recommended Adult Immunization Schedule—United States, October 2005–September 2006. MMWR 2005;54:Q1–Q4.
Detta schema anger de rekommenderade åldersgrupperna och medicinska indikationerna för rutinmässig administrering av för närvarande licensierade vacciner för personer i åldern >19 år. Licensierade kombinationsvacciner kan användas när någon av kombinationens komponenter är indicerad och när vaccinets övriga komponenter inte är kontraindicerade. För detaljerade rekommendationer, se tillverkarnas bipacksedlar och de fullständiga uttalandena från ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Rapportera alla kliniskt betydelsefulla reaktioner efter vaccination till Vaccine Adverse Event Reporting System (VAERS). Rapporteringsformulär och instruktioner om hur man lämnar in en VAERS-rapport finns tillgängliga på telefon, 800-822-7967, eller på VAERS webbplats på http://www.vaers.hhs.gov.
Information om hur man lämnar in en ansökan om ersättning från Vaccine Injury Compensation Program finns på http://www.hrsa.gov/osp/vicp eller på telefon, 800-338-2382. För att lämna in en ansökan om ersättning för vaccinskada, kontakta U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, telefon 202-357-6400.
Den ytterligare informationen om de vacciner som anges ovan och kontraindikationer för vaccination finns också på http://www.cdc.gov/nip eller från CDC-INFO Contact Center på 800-CDC-INFO (232-4636) på engelska och spanska, 24 timmar om dygnet, 7 dagar i veckan.
Användning av handelsnamn och kommersiella källor är endast för identifiering och innebär inte att det amerikanska hälsoministeriet godkänner dem.Hänvisningar till webbplatser på Internet som inte tillhör CDC tillhandahålls som en service till MMWR:s läsare och innebär inte att CDC eller det amerikanska hälsoministeriet godkänner eller innebär att CDC eller det amerikanska hälsoministeriet godkänner dessa organisationer eller deras program. CDC ansvarar inte för innehållet på de sidor som finns på dessa webbplatser. De URL-adresser som anges i MMWR var aktuella vid publiceringsdatumet.
Disclaimer Alla MMWR:s HTML-versioner av artiklar är elektroniska konverteringar från ASCII-text till HTML. Denna konvertering kan ha resulterat i teckenöversättning eller formatfel i HTML-versionen. Användarna bör inte förlita sig på detta HTML-dokument, utan hänvisas till den elektroniska PDF-versionen och/eller MMWR:s ursprungliga papperskopia för den officiella texten, figurerna och tabellerna. En papperskopia av detta nummer kan erhållas från Superintendent of Documents, U.S. Government Printing Office (GPO), Washington, DC 20402-9371, telefon: (202) 512-1800. Kontakta GPO för aktuella priser.
**Frågor eller meddelanden om fel i formateringen ska ställas till [email protected].
Datum för den senaste översynen: 10/13/2005
