![]()
Pessoas que utilizam tecnologia de assistência podem não conseguir aceder totalmente às informações deste ficheiro. Para assistência, por favor envie um e-mail para: [email protected]. Type 508 Accommodation and the title of the report in the subject line of e-mail.
![]() PDF
PDF
The Advisory Committee on Immunization Practices (ACIP) reviews annually the recommended Adult Immunization Schedule to ensure that the schedule reflects the current recommendations for the use of licensed vaccines. Em junho de 2005, a ACIP aprovou a Programação de Imunização de Adultos para outubro de 2005-setembro de 2006. Esta programação também foi aprovada pela Academia Americana de Médicos de Família e pelo Colégio Americano de Médicos Obstetras e Ginecologistas.
Alterações na programação para outubro de 2005–Setembro de 2006
A programação para 2005–2006 difere da programação anterior da seguinte forma:
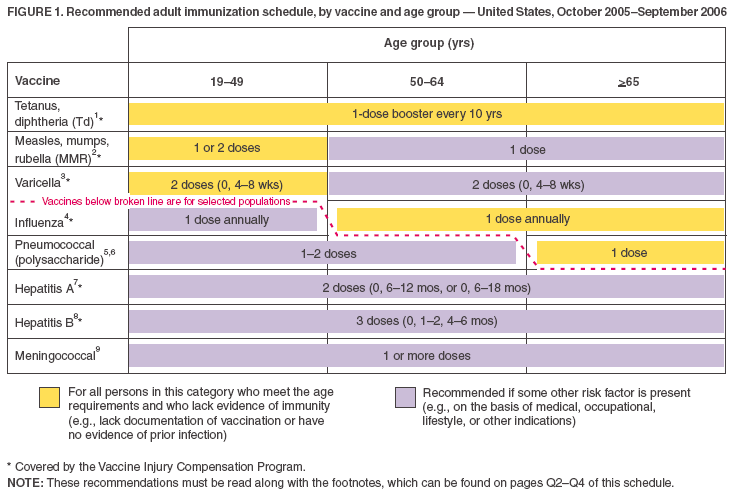
- As vacinas listadas na programação baseada na idade (Figura 1) são exibidas para que as vacinas recomendadas para uso rotineiro possam ser diferenciadas das recomendadas para adultos com determinados indicadores de risco (semelhante à programação de imunização infantil). Isto é ilustrado tanto pelo esquema de cores quanto pela linha quebrada.
- As barras amarelas (“Para todas as pessoas deste grupo”) e as barras verdes (“Para pessoas sem documentação de vacinação ou evidência de doença”) do cronograma anterior foram fundidas em uma barra amarela, que agora diz: “Para todas as pessoas nesta categoria que atendem aos requisitos de idade e que não possuem evidência de imunidade (por exemplo falta documentação da vacinação ou não tem evidência de infecção anterior)”
- A barra roxa foi alterada de “Para pessoas em risco (por exemplo, com indicações médicas/de exposição)” para “Recomendado se algum outro fator de risco estiver presente (por exemplo, com base em indicações médicas, profissionais, estilo de vida ou outras indicações)”. A barra roxa foi adicionada às colunas dos grupos de idade 50–64 anos e >65 anos para a vacina contra sarampo, papeira, rubéola (MMR).
- A coluna, “Diabetes, doença cardíaca, doença pulmonar crônica, ou doença hepática crônica incluindo alcoolismo crônico” foi transposta com a coluna, “Imunodeficiência congênita, leucemia, linfoma, malignidade generalizada, terapia com agentes alquilantes, antimetabolitos, vazamento de líquido cefalorraquidiano, radiação, ou grandes quantidades de corticosteróides” no cronograma de indicações médicas/outras (Figura 2) de modo que as contra-indicações para as vacinas contra MMR e varicela estão agora lado a lado.
- A fila para a vacina contra varicela foi movida para cima em ambas as figuras (i.e, para imediatamente após a vacina MMR) porque a vacina é agora universalmente recomendada para certos grupos etários.
- A vacinaeningocócica foi adicionada ao calendário de indicações médicas/outras (Figura 2). A nota de rodapé foi revista para incorporar as recomendações ACIP recentemente publicadas para esta vacina (1).
- A nota de rodapé do tétano e da difteria (#1) foi reformulada.
- A nota de rodapé da varicela (#3) foi reformulada de acordo com as recomendações ACIP adoptadas em Junho de 2005.
- A nota de rodapé influenza (#4) foi revisada para adicionar a mais nova condição de alto risco: condições neuromusculares que comprometem a função respiratória (2).
- A nota de rodapé 10 foi adicionada com relação à vacinação contra Haemophilus influenzae tipo b para populações de alto risco (i.e, pessoas com asplenia, leucemia e infecção pelo vírus da imunodeficiência humana).
O programa de imunização de adultos está disponível em inglês e espanhol em http://www.cdc.gov/nip/recs/adult-schedule.htm. Informações gerais sobre imunização de adultos, incluindo recomendações sobre vacinação de pessoas com HIV e outras condições imunossupressoras, estão disponíveis nos departamentos de saúde estaduais e locais e no Programa Nacional de Imunização em http://www.cdc.gov/nip. As informações sobre vacinação estão disponíveis em http://www.cdc.gov/nip/publicações/vis. As declarações do ACIP para cada vacina recomendada podem ser visualizadas, descarregadas e impressas a partir do website do Programa Nacional de Imunização em http://www.cdc.gov/nip/publications/acip-list.htm. Instruções para a notificação de eventos adversos ao Sistema de Notificação de Eventos Adversos da Vacina estão disponíveis em http://www.vaers.hhs.gov ou por telefone, 800-822-7967.
- CDC. Prevenção e controle da doença meningocócica: recomendações do Comitê Consultivo para Práticas de Imunização (ACIP). MMWR 2005;54(No. RR-7).
- CDC. Prevenção e controle da influenza: recomendações da Comissão Consultiva de Práticas de Imunização (ACIP). MMWR 2005;54(No. RR-8).
Figure 1
Volta ao topo.
Figure 2

Volta ao topo.
Aprovado pelo Comitê Consultivo de Práticas de Imunização, pelo Colégio Americano de Obstetras e Ginecologistas, e pela Academia Americana de Médicos de Família
>
1. Vacinação contra o tétano e difteria (Td). Adultos com história incerta de uma série completa de vacinação primária com difteria e tétano com toxoides devem receber uma série primária usando toxoides Td combinados. Uma série primária para adultos é de 3 doses; administrar as primeiras 2 doses com pelo menos 4 semanas de intervalo e a terceira dose 6–12 meses após a segunda. Administre 1 dose se a pessoa recebeu a série primária e se a última vacinação foi recebida >10 anos antes. Consulte a declaração da ACIP para recomendações sobre a administração de Td como profilaxia no tratamento de feridas (http://www.cdc.gov/mmwr/preview/mmwrhtml/00041645.htm). A Força Tarefa sobre Imunização de Adultos do Colégio Americano de Médicos apoia uma segunda opção para o uso de Td em adultos: um único reforço de Td aos 50 anos de idade para pessoas que tenham completado a série pediátrica completa, incluindo o reforço de adolescentes/jovens adultos. Uma vacina recentemente licenciada contra o tétano difteria-acelular-pertussis está disponível para adultos. Serão publicadas recomendações ACIP para o seu uso.
2. Vacinação contra sarampo, papeira, rubéola (MMR). Componente do sarampo: adultos nascidos antes de 1957 podem ser considerados imunes ao sarampo. Adultos nascidos durante ou após 1957 devem receber >1 dose de MMR a menos que tenham uma contra-indicação médica, documentação de >1 dose, histórico de sarampo baseado no diagnóstico do prestador de cuidados de saúde, ou evidência laboratorial de imunidade. Uma segunda dose de MMR é recomendada para adultos que 1) foram recentemente expostos ao sarampo ou em um ambiente de surto; 2) foram previamente vacinados com a vacina contra sarampo morto; 3) foram vacinados com um tipo desconhecido de vacina contra sarampo durante 1963-1967; 4) são estudantes em instituições de ensino pós-secundário; 5) trabalham em uma instituição de saúde; ou 6) planejam viajar internacionalmente. Não vacinar pessoas infectadas pelo sarampo com imunossupressão grave. Componente da caxumba: 1 dose de vacina contra MMR deve ser adequada para proteção das pessoas nascidas durante ou após 1957 que não tenham histórico de caxumba com base no diagnóstico do prestador de serviços de saúde ou que não tenham provas laboratoriais de imunidade. Componente da rubéola: administrar 1 dose da vacina MMR a mulheres cujo histórico de vacinação contra a rubéola não seja confiável ou que careçam de evidência laboratorial de imunidade. Para mulheres em idade fértil, independentemente do ano de nascimento, determine rotineiramente a imunidade à rubéola e aconselhe as mulheres sobre a síndrome da rubéola congênita. Não vacine mulheres que estejam grávidas ou que possam engravidar dentro de 4 semanas após o recebimento da vacina. Mulheres que não têm evidência de imunidade devem receber a vacina MMR ao completar ou interromper a gravidez e antes da alta do serviço de saúde.
3. Vacinação contra varicela. A vacinação contra a varicela é recomendada para todos os adultos sem evidência de imunidade à varicela. Consideração especial deve ser dada àqueles que 1) têm contato próximo com pessoas em alto risco de doenças graves (trabalhadores de saúde e contatos familiares de pessoas imunocomprometidas) ou 2) estão em alto risco de exposição ou transmissão (por exemplo, professores de crianças pequenas; funcionários de creches; residentes e funcionários de instituições, incluindo instituições correcionais; estudantes universitários; militares; adolescentes e adultos vivendo em lares com crianças; mulheres não grávidas em idade fértil; e viajantes internacionais). A evidência de imunidade à varicela em adultos inclui qualquer uma das seguintes: 1) vacina contra a varicela apropriada para a idade (isto é, recebimento de 1 dose antes dos 13 anos de idade ou recebimento de 2 doses após os 13 anos de idade); 2) nascido nos EUA antes de 1966 ou histórico de doença de varicela antes de 1966 para não-americanos.3) história de varicela baseada no diagnóstico do prestador de cuidados de saúde ou no relato dos pais ou auto-relato da doença típica da varicela para pessoas nascidas durante 1966–1997 (para um paciente que relata uma história de um caso atípico e leve, os prestadores de cuidados de saúde devem procurar ou uma ligação epidemiológica com um caso típico de varicela ou evidência de confirmação laboratorial, se esta foi realizada no momento da doença aguda); 4) história de herpes zoster baseada no diagnóstico do prestador de cuidados de saúde; ou 5) evidência laboratorial de imunidade. Não vacine mulheres que estejam grávidas ou que possam engravidar dentro de 4 semanas após o recebimento da vacina. Avaliar as mulheres grávidas quanto à evidência de imunidade à varicela. As mulheres que não têm evidência de imunidade devem receber a dose 1 de vacina contra varicela ao completar ou interromper a gravidez e antes da alta da instituição de saúde. A dose 2 deve ser administrada 4 a 8 semanas após a dose 1.
4. Vacinação contra a gripe. Indicações médicas: doenças crónicas dos sistemas cardiovascular ou pulmonar, incluindo asma; doenças metabólicas crónicas, incluindo diabetes mellitus, disfunção renal, hemoglobinopatias, ou imunossupressão (incluindo imunossupressão causada por medicamentos ou VIH); qualquer condição (por exemplo disfunção cognitiva, lesão medular, distúrbio convulsivo ou outro distúrbio neuromuscular) que comprometa a função respiratória ou a manipulação de secreções respiratórias ou que possa aumentar o risco de aspiração; e gravidez durante a época da gripe. Não existem dados sobre o risco de doença influenza grave ou complicada entre pessoas com asplenia; entretanto, a influenza é um fator de risco para infecções bacterianas secundárias que podem causar doença grave entre pessoas com asplenia. Indicações ocupacionais: trabalhadores de saúde e empregados de instalações de cuidados de longa duração e de vida assistida. Outras indicações: residentes de lares e outras instalações de cuidados de longa duração e de vida assistida; pessoas com probabilidade de transmitir a gripe a pessoas de alto risco (ou seja, contatos domiciliares e cuidadores de crianças de 0 a 23 meses ou pessoas de todas as idades com condições de alto risco), e qualquer pessoa que deseje ser vacinada. Para pessoas saudáveis, não grávidas de 5 a 49 anos sem condições de alto risco, que não estejam em contato com pessoas gravemente imunocomprometidas em unidades de cuidados especiais, a vacina contra influenza (FluMist®) pode ser administrada por via intranasal em vez da vacina inativada.
5. Vacina contra polissacarídeos pneumocócicos. Indicações médicas: doenças crônicas do sistema pulmonar (excluindo asma); doenças cardiovasculares; diabetes mellitus; doenças hepáticas crônicas, incluindo doenças hepáticas como resultado do abuso de álcool (por exemplo, cirrose); insuficiência renal crônica ou síndrome nefrótica; asplenia funcional ou anatômica (por exemplo doença falciforme ou esplenectomia); condições imunossupressoras (por exemplo, imunodeficiência congênita, infecção por HIV, leucemia, linfoma, mieloma múltiplo, doença de Hodgkin, malignidade generalizada ou transplante de órgãos ou medula óssea); quimioterapia com agentes alquilantes, antimetabolitos ou corticosteróides sistêmicos a longo prazo; e implantes cocleares. Outras indicações: Nativos do Alasca e certas populações indígenas americanas; residentes de lares e outras instalações de cuidados de longo prazo.
6. Revacinação com vacina pneumocócica de polissacarídeos. Revacinação única após 5 anos para pessoas com insuficiência renal crônica ou síndrome nefrítica; asplenia funcional ou anatômica (por exemplo, doença falciforme ou esplenectomia); condições imunossupressoras (por exemplo imunodeficiência congênita, infecção por HIV, leucemia, linfoma, mieloma múltiplo, doença de Hodgkin, malignidade generalizada, ou transplante de órgãos ou medula óssea); ou quimioterapia com agentes alquilantes, antimetabolitos, ou corticosteróides sistêmicos a longo prazo. Para pessoas com idade >65 anos, revacinação única se foram vacinadas >5 anos antes e tinham idade <65 anos no momento da vacinação primária.
7. Vacinação contra a hepatite A. Indicações médicas: pessoas com distúrbios do fator de coagulação ou doença hepática crônica. Indicações comportamentais: homens que fazem sexo com homens ou usuários de drogas ilegais. Indicações ocupacionais: Pessoas que trabalham com o vírus da hepatite A (VHA) – primatas infectados ou com o VHA em um ambiente de laboratório de pesquisa. Outras indicações: pessoas que viajam ou trabalham em países com endemicidade alta ou intermediária da hepatite A (para lista de países, verhttp://www.cdc.gov/travel/diseases.htm#hepa), assim como qualquer pessoa que deseje obter imunidade. As vacinas atuais devem ser administradas em séries de 2 doses com 0 e 6–12 meses, ou 0 e 6–18 meses. Se a vacina combinada contra a hepatite A e a hepatite B for utilizada, administrar 3 doses a 0, 1 e 6 meses.
8. Vacinação contra a hepatite B. Indicações médicas: pacientes em hemodiálise (usar formulação especial ou duas doses de 20-µg/mL) ou pacientes que recebem concentrados de fator de coagulação. Indicações profissionais: profissionais de saúde e de segurança pública que tenham exposição ao sangue no local de trabalho e pessoas em formação nas escolas de medicina, odontologia, enfermagem, tecnologia laboratorial e outras profissões de saúde aliadas. Indicações comportamentais: usuários de drogas injetáveis; pessoas com mais de um parceiro sexual durante os 6 meses anteriores; pessoas com uma doença sexualmente transmissível (DST) adquirida recentemente; e homens que fazem sexo com homens. Outras indicações: contactos domésticos e parceiros sexuais de pessoas com infecção crónica pelo vírus da hepatite B (VHB); clientes e funcionários de instituições para pessoas com deficiência de desenvolvimento; todos os clientes de clínicas de DST; reclusos de estabelecimentos prisionais; e viajantes internacionais que estarão em países com prevalência elevada ou intermédia de infecção crónica pelo VHB durante mais de 6 meses (para lista de países, ver http://www.cdc.gov/travel/diseases.htm#hepa).
9. Vacinação meningocócica. Indicações médicas: adultos com asplenia anatômica ou funcional ou deficiências de componentes do complemento terminal. Outras indicações: estudantes universitários do primeiro ano que vivem em dormitórios; microbiologistas expostos rotineiramente a isolados de Neisseria meningitidis; recrutas militares; e pessoas que viajam ou residem em países nos quais a doença meningocócica é hiperendémica ou epidémica (por exemplo, a “cintura de meningite” da África subsariana durante a estação seca), particularmente se o contacto com as populações locais for prolongado. O governo da Arábia Saudita exige vacinação para todos os viajantes a Meca durante o Hajj anual. A vacina conjugada meningocócica é preferida para os adultos que se encontrem com qualquer uma das indicações acima, com idade <55 anos, embora a vacina polissacarídeo meningocócica (MPSV4) seja uma alternativa aceitável. A revacinação após 5 anos pode ser indicada para adultos previamente vacinados com MPSV4 que permanecem em alto risco de infecção (por exemplo, pessoas que residem em áreas onde a doença é epidêmica).
10. Condições selecionadas para as quais a vacina Haemophilus influenzae tipo b (Hib) pode ser usada. As vacinas conjugadas do Hib são licenciadas para crianças de 6 a 71 meses de idade. Não há dados de eficácia disponíveis nos quais se possa basear uma recomendação sobre o uso da vacina contra o Hib para crianças maiores e adultos com condições crônicas associadas a um risco aumentado para a doença do Hib. Entretanto, estudos sugerem boa imunogenicidade em pacientes com doença falciforme, leucemia ou infecção por HIV ou que tenham tido esplenectomias; administrar a vacina a esses pacientes não é contra-indicado.
O Programa Recomendado de Imunização de Adultos foi aprovado pelo Comitê Consultivo de Práticas de Imunização, pelo Colégio Americano de Obstetras e Ginecologistas e pela Academia Americana de Médicos de Família. O formato padrão da nota de rodapé MMWR foi modificado para publicação desta programação.
Citação de citação: Centros de Controle e Prevenção de Doenças. Cronograma Recomendado de Imunização de Adultos — Estados Unidos, Outubro 2005–Setembro 2006. MMWR 2005;54:Q1–Q4.
Esta programação indica os grupos etários recomendados e as indicações médicas para a administração rotineira das vacinas atualmente licenciadas para pessoas com idade >19 anos. As vacinas combinadas licenciadas podem ser usadas sempre que quaisquer componentes da combinação forem indicados e quando os outros componentes da vacina não estiverem contra-indicados. Para recomendações detalhadas, consulte os folhetos informativos dos fabricantes e as declarações completas da ACIP (http://www.cdc.gov/nip/publications/acip-list.htm).
Relatar todas as reacções clinicamente significativas pós-vacinação ao Sistema de Notificação de Eventos Adversos da Vacina (VAERS). Formulários de notificação e instruções sobre como apresentar um relatório VAERS estão disponíveis por telefone, 800-822-7967, ou no website do VAERS em http://www.vaers.hhs.gov.
Informações sobre como apresentar uma reclamação do Programa de Indenização de Danos da Vacina estão disponíveis em http://www.hrsa.gov/osp/vicp ou por telefone, 800-338-2382. Para apresentar um pedido de indemnização por danos causados por vacinas, contacte o U.S. Court of Federal Claims, 717 Madison Place, N.W., Washington, DC 20005, telefone 202-357-6400.
Informações adicionais sobre as vacinas listadas acima e contra-indicações para vacinação também estão disponíveis em http://www.cdc.gov/nip ou pelo CDC-INFO Contact Center no 800-CDC-INFO (232-4636) em inglês e espanhol, 24 horas por dia, 7 dias por semana.1769
Disclaimer Todas as versões HTML do MMWR dos artigos são conversões eletrônicas do texto ASCII para HTML. Esta conversão pode ter resultado em tradução de caracteres ou erros de formatação na versão HTML. Os usuários não devem confiar neste documento HTML, mas são referidos à versão eletrônica em PDF e/ou à cópia original em papel do MMWR para o texto oficial, figuras e tabelas. Uma cópia original em papel deste número pode ser obtida junto ao Superintendente de Documentos, U.S. Government Printing Office (GPO), Washington, DC 20402-9371; telefone: (202) 512-1800. Contacte o GPO para preços correntes.
**Questões ou mensagens relativas a erros de formatação devem ser enviadas para [email protected].
Data da última revisão: 10/13/2005
