Introdução
Doença diverticular do cólon representa a doença mais comum que afecta o intestino grosso no mundo ocidental. A prevalência da doença diverticular tem aumentado no último século em todo o mundo, provavelmente devido a mudanças no estilo de vida, como fumar, excesso de peso, e sobre toda a inactividade física e dieta pobre em fibras. A prevalência aumenta com a idade, variando de aproximadamente 5% em adultos com menos de 40 anos até 50-70% entre aqueles com 80 anos de idade ou mais; 80% dos pacientes que apresentam diverticulite têm 50 anos ou mais. As diverticulas podem apresentar-se em número desde solitárias a centenas, têm tipicamente 5-10mm de diâmetro, mas podem ultrapassar os 2cm de tamanho. A diverticulosidade ocorre principalmente no cólon sigmóide e descendente em mais de 90% dos pacientes, mas pode ser prevalente em graus variados no restante do cólon.1
Existem vários termos relacionados à diverticulite que serão usados nesta revisão. A presença de diverticula no cólon na ausência de inflamação explícita é chamada diverticula ou doença diverticular descomplicada (DUD). Pode ser sintomática ou assintomática. O termo “diverticulite aguda do cólon” (DCD) é usado para descrever a inflamação da diverticula, que pode ou não progredir para complicações (DCD complicado). Há também diverticulite crônica, devido a diverticulite recorrente ou devido ao desenvolvimento de uma colite segmentar associada à diverticula. Resumidamente, o espectro clínico da doença diverticular é amplo.
Estudos sobre a história natural da doença apontam que a grande maioria dos pacientes com diverticula (cerca de 80%) permanecerá assintomática durante toda a sua vida. Dos 15-20% que desenvolvem sintomas, aproximadamente 1/4 eventualmente terá um episódio de doença diverticular dolorosa sintomática sem inflamação, e até 10-25% terá um episódio de TCA. Cerca de 1-2% necessitarão de hospitalização e 0,5% de cirurgia. A diverticula é responsável pela maioria (24-42%) dos episódios de sangramento gastrointestinal inferior.2-4
Fisiopatologia e desenvolvimento de sintomas
Um divertículo colônico é uma hérnia de mucosa e submucosa, correspondendo a um ponto fraco onde a vasa rectila penetra a túnica muscular. Os mecanismos patogênicos da doença diverticular ainda são pouco compreendidos, porém é geralmente reconhecido que estes estão provavelmente relacionados a complexas interações entre dieta, microbiota colônica, fatores genéticos, motilidade colônica e estrutura que resultam em sua formação de diverticula colônica ao longo do tempo.5 Ver Fig. 1. Em 1971, Painter e Burkitt publicaram sua famosa hipótese de que a doença diverticular era causada pelo excesso de pressão no cólon devido à segmentação baseada na ingestão insuficiente de fibra alimentar. Em resposta ao aumento da pressão intraluminal, os outpouchings podem desenvolver-se e sobressair em áreas de fraqueza potencial.6 A estase ou obstrução no divertículo de pescoço estreito pode levar ao crescimento excessivo de bactérias e à isquemia do tecido local, levando à perfuração.7 Desde então, numerosos estudos observacionais tentaram demonstrar o possível efeito da fibra na prevenção da doença diverticular. A maioria deles concluiu que o risco de DUD estava inversamente associado à ingestão de fibras alimentares.8-10 Com base nessas evidências, uma dieta rica em fibras é recomendada para prevenir a doença diverticular na maioria das diretrizes e posições atuais.11-15 Entretanto, essa hipótese tem sido questionada recentemente desde: (1) a associação inversa entre ingestão de fibras e diverticulose tem sido questionada em alguns estudos epidemiológicos recentes16,17 e (2) novas hipóteses patogênicas, como a neuropática e a miopática, estão surgindo.18-22 Outros fatores que têm sido associados a um risco aumentado de doença diverticular incluem inatividade física, constipação intestinal, obesidade e tabagismo.23-27
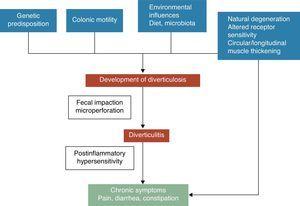
O desenvolvimento de sintomas na doença diverticular está provavelmente relacionado a interações complexas entre características genéticas, estrutura do cólon, inflamação de baixo grau de motilidade intestinal e hipersensibilidade pós-inflamatória.
A associação entre a doença diverticular não complicada (DRU) e os sintomas é incerta. Há algumas evidências que sugerem que a doença diverticular dolorosa pode ser uma condição relacionada à inflamação e seus efeitos na função neuromuscular no cólon.22-28 A presença de uma inflamação intestinal crônica de baixo grau induziria uma disfunção sensório-motora, levando ao desenvolvimento e/ou persistência dos sintomas. Alterações na microflora intestinal poderiam ser um dos mecanismos putativos responsáveis pela inflamação de baixo grau. O crescimento excessivo de bactérias auxiliado pela estase fecal dentro da diverticula poderia contribuir para uma inflamação crônica de baixo grau que sensibilizaria tanto os eferentes primários intrínsecos quanto os neurônios aferentes primários extrínsecos. Essas alterações poderiam levar à hipertrofia muscular lisa, e aumento da sensibilidade à distensão abdominal e, finalmente, ao desenvolvimento de sintomas.3,22 Ver Fig. 1.
Como mencionamos acima, a maioria das pessoas com diverticula colônica permanece assintomática, mas eventualmente pode desenvolver complicações como DAC ou sangramento da diverticula. Neste artigo nós focalizamos o TCA. A manifestação clínica deste evento dependerá de uma série de fatores, incluindo o tamanho da perfuração, o nível de contaminação extracolônica e a habilidade do corpo em conter esta contaminação.29,30
Gerenciamento da doença diverticularGerenciamento da doença diverticular não complicada (DUD)
Em pacientes com DUD assintomática,2 uma dieta rica em fibras pode ser recomendada devido ao seu possível benefício profilático na prevenção da DUD sintomática e complicações. Não há evidências de que outros medicamentos sejam úteis nesses pacientes.
Existem mais evidências sobre o benefício do tratamento na DEU sintomática. O sintoma mais freqüente é a dor abdominal, que pode ser exacerbada pela alimentação e aliviada pela defecação ou pela passagem de flatus. Outros sintomas são náusea, diarréia, constipação e inchaço. Mais de 61% dos pacientes com DRU sintomática que não estão tomando nenhuma medida terapêutica para prevenir a recorrência dos sintomas tornar-se-ão sintomáticos dentro de 1 ano, e cerca de 4% desenvolverão complicações.31
Cinco agentes foram propostos para tratamento (ver Fig. 2):

Tratamento de doença diverticular descomplicada. Mecanismos de ação.
A) Dieta com alto teor de fibras ou agentes de volume
Estudos controlados controlados controladoseversais (ECR) e outros estudos intervencionistas avaliam o efeito das fibras em UDD sintomáticas, mas com resultados inconsistentes.32-37 De qualquer forma, a fibra é recomendada na prevenção e tratamento da DUD sintomática, bem como na prevenção da DDA pela maioria das diretrizes e posicionamentos atuais.11-15
B) Terapia antibiótica
A fundamentação para o uso de antibióticos na DUD sintomática não está claramente estabelecida. Estudos recentes sugerem que alterações na microbiota intestinal (crescimento excessivo de bactérias intestinais) poderiam contribuir para o desenvolvimento de sintomas devido à produção excessiva de gás intestinal através da fermentação de carboidratos. A fim de evitar efeitos sistemáticos, os antibióticos pouco absorvidos que actuam contra os agentes patogénicos entéricos mas que apresentam um risco mínimo de toxicidade sistemática ou efeitos secundários parecem ser os antibióticos mais apropriados. Rifaximin foi proposto.
Rifaximin
Rifaximin é uma rifamicina análoga não sistemática com um largo espectro de actividade in vitro. A rifaximina pode diminuir a actividade metabólica da flora intestinal, aumentando a massa fecal, e pode também erradicar o crescimento excessivo de bactérias. Este antibiótico tem um perfil de alta segurança e tolerabilidade.33,38 O nível plasmático da rifaximina é mínimo, portanto os patogénios não envenenados não são expostos à pressão selectiva e o risco de resistência bacteriana é baixo.39 Três RCTs abertas e duas duplas cegas40-44 examinaram a eficácia da administração cíclica da rifaximina e da fibra na redução dos sintomas em comparação com a fibra isolada. Uma revisão sistemática e duas metanálises analisaram estes ensaios.44-46 Concluíram que o tratamento combinado é eficaz na obtenção de alívio dos sintomas a 1 ano em doentes com DRU. 35% dos pacientes tratados com fibras isoladas eram assintomáticos em comparação com 64% nos grupos de tratamento combinado. O número necessário para o tratamento foi de três para rifaximina vs. placebo para aliviar os sintomas e nove para evitar complicações. Em resumo, os melhores resultados foram obtidos utilizando uma combinação de fibra solúvel, como o glucomanano e a rifaximina 1 semana por mês.
C) Probióticos
Probióticos são microorganismos vivos que podem restaurar a flora intestinal comensal que pode ter sido alterada na doença diverticular devido à estase e à redução do tempo de trânsito do cólon.47 Infelizmente, há poucos dados disponíveis sobre o seu uso em UDD sintomática e a maioria dos estudos são pequenos e descontrolados. A maioria deles apresenta melhora dos sintomas.48-50
Probióticos também estudaram em combinação com 5-aminosalicilato (5-ASA). Tursi e colegas realizaram três TCRs comparando 5-ASA sozinho, probiótico sozinho ou terapia combinada.51-53 Tanto o 5-ASA como os probióticos pareceram ser eficazes para a prevenção da DUD sintomática, mas sua combinação foi melhor. Um RCT recente de dupla ligação publicado por este mesmo grupo científico concluiu que tanto a mesalazina cíclica quanto o DG Lactobacillus casei subsp, particularmente em combinação, parecem ser melhores que o placebo para manter a remissão da DUD sintomática.54 Mas, em resumo, os desenhos pobres do estudo e o tamanho pequeno deles não permitem conclusões definitivas.
D) 5-ASA: mesalazina
Mesalazina tem efeitos anti-inflamatórios e antioxidantes. Em 2010, Gatta et al.,55 publicaram uma revisão sistemática da Cochrane que avaliou o papel da 5-ASA em pacientes com doença diverticular. Os autores concluíram que a 5-ASA pode ser eficaz no tratamento desta doença e que a mesalazina era melhor que a administração cíclica para evitar recaídas. São necessárias TCRs de alta qualidade e bem projetadas para confirmar suas observações. De fato, o primeiro ensaio duplo-cego controlado por placebo encontrou mesalazina eficaz na obtenção de alívio da dor em pacientes com DRU aguda.56 Além disso, há dois TCR interessantes que mostraram um benefício para a mesalazina em comparação com a rifaximina em termos de prevenção de recidiva sintomática e sucesso similar na manutenção da remissão a longo prazo em comparação com o probiótico Lactobacillus casei.53,57
E) Agentes anticolinérgicos/antiespasmódicos
A hipermotilidade do cólon na diverticulose sugere que agentes antiespasmódicos como a diciclomina e a hiosciamina podem melhorar os sintomas diminuindo a contração muscular. Mas, não há TTRs que confirmem este benefício.
F) Evitar o tratamento com AINE
Estudos controlados severamente mostraram que os AINE são um fator de risco para o desenvolvimento de sintomas, TCA, perfuração e sangramento.7,58-60 Os usuários de AINE têm mais risco de desenvolver doenças diverticulares sintomáticas do que os não usuários (RR: 1,5, IC 95%: 1,1-2,1).58 E em pacientes com doenças diverticulares complicadas houve um maior uso de AINE em comparação com os controles sem doença. Postulou-se que este risco aumentado era devido a danos na mucosa, resultando em comprometimento da função de barreira da mucosa cólica, permitindo a translocação de bactérias, que provocam inflamação.
G) Níveis de vitamina D
Parece que a incidência de ACD tem sido associada a variações geográficas e sazonais. Por causa disso, Maguire et al. conduziram dois interessantes estudos observacionais que mostraram que níveis mais baixos de vitamina D e baixa exposição à luz UV (a exposição UV determina o status da vitamina D) estão associados a um risco significativamente maior de TCA. Mais estudos de alta qualidade são necessários antes de fazer uma recomendação.61,62
Tratamento da diverticulite aguda do cólon (DCA)
Embora a maioria das pessoas com diverticulose permaneça assintomática, estima-se que cerca de 10-25% delas desenvolverão um episódio de DCA esquerdo.63 Geralmente, o diagnóstico clínico não é suficientemente preciso e as técnicas radiológicas são indicadas. Em pacientes com sintomas leves (a maioria) e sem sinais de TCA complicado, a combinação de dor no baixo abdome esquerdo, a ausência de vômitos e uma proteína C reativa >50mg/l, pode ser suficiente para o diagnóstico.64,65 Se a imagem for indicada, provavelmente, uma estratégia condicional com ultra-som como técnica de primeira linha e seguida de tomografia computadorizada (TC), se o ultra-som for inconclusivo ou duvidoso, pode representar a abordagem mais eficaz. O número de exames de tomografia computadorizada pode ser reduzido em 50%. Em 1978, Hinchey et al. propuseram uma classificação da TCA, que foi modificada posteriormente.66,67 Ela distingue cinco estágios da TCA; estágio 0, diverticulite clinicamente leve, estágio I (a: inflamação pericólica e b: abcesso
cm na proximidade da inflamação primária), estágio II, abcesso intraabdominal, pélvico ou retroperitoneal ou abcesso distante da inflamação primária, estágio III, peritonite purulenta generalizada e estágio IV, peritonite fecal. Ver Fig. 3.

Algoritmo para o manejo da diverticulite cólica aguda.
Tratamento do DCA sem complicações (Hinchey stage 0 ou Ia)
A maioria do DCA sem complicações pode ser tratada com segurança de forma conservadora com uma taxa de sucesso entre 70% e 100%.14 O tratamento ambulatorial pode permitir uma importante economia de custos para os sistemas de saúde. Em casos de TCA sem complicações, os critérios para o tratamento hospitalar são inflamação significativa (incluem presença de febre ou peritonite), intolerância a fluidos orais, idade superior a 80-85 anos, imunossupressão, ou comorbidades graves. Na maioria dos casos, uma baixa permanência hospitalar será suficiente. Não há evidências de que as restrições alimentares influenciaram os resultados do tratamento, embora a maioria dos médicos geralmente recomende dieta líquida clara.
Uma das maiores mudanças recentes no manejo do TCA sem complicações é a diminuição do uso de antibióticos. Uma recente revisão da Cochrane, apenas uma abordagem qualitativa (sem meta-análise), descobriu que os melhores dados disponíveis não suportam o seu uso rotineiro.68 Os antibióticos não aceleram a recuperação nem previnem complicações ou recidivas. Portanto, o uso de antibióticos, neste caso, é questionável. Provavelmente, eles seriam apropriados em pacientes com sinais de infecção generalizada, sinais de septicemia ou bacteremia e em pacientes imunocomprometidos. Os regimes recomendados são baseados em consensos clínicos. Vários antibióticos podem ser utilizados, desde ampicilina até cefalosporinas de terceira geração, desde que sejam eficazes contra bactérias gram positivas, gram negativas e anaeróbias. A combinação de ciprofloxacina e metronidazol é provavelmente o tratamento oral mais prescrito. Se esta combinação for mal tolerada, a ampicilina-sulfactam pode ser uma boa escolha. Por outro lado, dados recentes têm mostrado que não há vantagens do tratamento intravenoso sobre os antibióticos orais e do tratamento intravenoso de 4 dias em 7 dias.69-71 Normalmente, a melhora clínica é observada dentro de 3-4 dias após o tratamento. Finalmente, a admissão ao hospital com antibiótico intravenoso é recomendada quando o paciente é incapaz de ingerir alimentos oralmente, é afetado por comorbidade grave ou não melhora com tratamento ambulatorial.
Tratamento do TCA complicado (Hinchey stage Ib a IV)TCA Hinchey Ib ou II: abcesso
Aproximadamente 15% dos pacientes com TCA desenvolverão um abscesso.67 Não há evidências de alta qualidade sobre o manejo mais otimizado do TCA com formação de abscesso. A hospitalização é indicada. O tamanho é um determinante importante para o sucesso do tratamento. Em abscessos menores (
cm) é recomendado um tratamento conservador com antibióticos de amplo espectro. Será bem sucedido em até 70%.72 Quando o tratamento conservador falha ou em abscessos maiores, a drenagem percutânea deve ser realizada. É bem sucedida em até 80%.73 A cirurgia será um tratamento de resgate quando os tratamentos mencionados anteriormente falharem.ACD Hinchey III ou IV: peritonite purulenta ou fecal
Peritonite é a complicação mais grave, com uma mortalidade de 14%. Embora não haja evidências, a cirurgia precoce é considerada a terapia padrão para estes pacientes. A escolha da operação é influenciada pelas condições do paciente, pelos achados operatórios e pela experiência do cirurgião. Em pacientes críticos com instabilidade hemodinâmica, recomenda-se o procedimento de Hartmann. Entretanto, em pacientes hemodinamicamente estáveis, a anastomose primária com ou sem desvio fecal proximal deve ser considerada uma escolha preferível.14,74
Tradicionalmente, as diretrizes internacionais recomendam o uso da endoscopia após um episódio de TCA para excluir o câncer colorretal. Esta recomendação é baseada apenas em opiniões de especialistas. Estudos retrospectivos recentes e uma revisão sistemática75-80 mostram que a taxa de câncer nestes pacientes é bastante baixa. Com base nesta evidência recente, a estratégia mais eficaz pode ser a de referir-se à colonoscopia apenas aos pacientes com sintomas persistentes ou àqueles com achados suspeitos de TC. Mas mais estudos são necessários para uma recomendação firme.
Gerenciamento após um episódio de CAAD
Após um episódio de TCA, cerca de um terceiro terá um segundo TCA, e após um segundo episódio, outro terceiro terá outro ataque.73,74 Mas as evidências para definir o tratamento ideal após um episódio de TCA para prevenir um novo episódio são escassas.
A) Dieta rica em fibras
Após o episódio agudo ter sido resolvido, uma dieta rica em fibras é comumente recomendada para reduzir as recidivas. Mas, a TCR em dietas com alto teor de fibras em pacientes com TCA tem tido resultados inconsistentes. Uma revisão sistemática recentemente publicada da dieta com alto teor de fibras não poderia incluir qualquer estudo que investigue o papel das fibras na prevenção de recidivas de TCA.26,81 Alguns alimentos (sementes, pipoca e nozes) são classicamente evitados porque teoricamente entram, bloqueiam ou irritam o divertículo. Mas Strate et al. em seu grande e prospectivo estudo não encontraram associação com um aumento do risco de TCA. Portanto, a exclusão destes alimentos da dieta não deve ser recomendada.82 Além disso, a redução de peso e a cessação do tabagismo podem ter uma influência favorável na prevenção do TCA.9,83
B) Antibióticos
Há três revisões sistemáticas recentes que avaliaram o papel da rifaximina cíclica na prevenção da recorrência do TCA, mas não mostraram um benefício claro.46,84,85 Do ponto de vista fisiopatológico, uma explicação plausível da ineficácia da rifaximina na prevenção de recidivas pode ser que um tratamento cíclico pode não controlar a população bacteriana cólica durante todo o mês, uma vez que a população bacteriana cólica se recupera dentro de 7-14 dias após o fim da rifaximina. No entanto, uma recente TCR aberta espanhola mostrou que a rifaxina cíclica pode melhorar os sintomas e manter períodos de remissão após a TCA.86 As recidivas ocorreram em 10,4% dos pacientes aos quais foi administrada rifaxina mais fibra versus 19,3% de fibra isoladamente. Além disso, os pacientes diagnosticados pela primeira vez desde ≥1 ano tiveram um maior risco de exacerbação (OR 3,34, IC 95%: 0,01-12,18). Mas são necessários mais estudos uma vez que, actualmente, não podem ser feitas recomendações. Não há evidências para apoiar o uso de outros antibióticos neste cenário.
C) Probióticos
alguns estudos de rótulos abertos examinaram o papel dos probióticos na prevenção da recidiva da DAC. Giaccari et al., há mais de 20 anos, avaliaram o papel do Lactobacillus sp. após a rifaximina em 79 pacientes com estenose do cólon pós-diverticulite. 88% dos pacientes permaneceram assintomáticos por um período de 12 meses.87 Este estudo observacional foi o primeiro que sugeriu um possível papel dos probióticos neste cenário. Um estudo mais recente avaliou o tratamento combinado; balsalazida e VSL#3 (uma mistura probiótica de oito espécies). Depois de 12 meses, 73% dos sujeitos em terapia combinada eram assintomáticos comparados com 53% em monoterapia probiótica (p>0,05).52 Em resumo, os probióticos parecem ser eficazes na prevenção da recidiva da TCA, mas faltam estudos bem desenhados.
D) 5-ASA
TCRseverais duplo-cegos e abertos avaliaram o papel da mesalazina na prevenção da recidiva da TCA. Infelizmente a maioria deles não encontrou um benefício da mesalazina sobre o placebo na prevenção da recidiva.88-90 Raskin et al. publicaram recentemente dois TTRs duplo-cegos e placebo duplo-cegos de fase 3 (PREVENT1 e PREVENT2) que também mostram que a mesalazina não é superior ao placebo na prevenção da recidiva do ACD.91 Também o tratamento combinado, 5-ASA mais rifaximin, foi avaliado em vários estudos. Trivedi e Das revisaram dados de cinco TCR e um estudo aberto, envolvendo coletivamente mais de 600 pacientes, e concluíram que a combinação parece ser superior à rifaximina por si só para prevenir o TCA recorrente.92
E) Cirurgia
A até alguns anos atrás, a cirurgia eletiva era recomendada após dois ataques de TCA sem complicações ou um ataque de TCA complicado para reduzir a morbidade e mortalidade por recidiva. Mas a cirurgia eletiva também traz um risco aumentado de morbi-mortalidade.93 Por isso, é importante pesar a morbidade e mortalidade devido à cirurgia contra o risco de recidivas complicadas e gravidade dos sintomas.
Dados recentes mostram que a história natural do TCA é muito mais benigna do que se pensava no passado.73,94 O risco de recidiva a longo prazo é mais baixo do que se acreditava anteriormente, e os riscos a longo prazo de cirurgia de emergência subsequente (3-7%), morte (95 mostrou que 16% dos casos com primeiro TCA foram operados com urgência em comparação com apenas 6% nos casos recidivantes, e que a mortalidade de 30 dias no primeiro episódio também foi maior em comparação com eventos recorrentes (3% vs. 0%). De fato, a maioria dos pacientes com TCA complicada não tem histórico da doença.96 Também é proposto que o TCA recorrente pode proteger contra perfuração, possivelmente devido à formação de adesão causada pela inflamação.95 Portanto, uma política de cirurgia eletiva após o TCA não diminui a probabilidade de novas cirurgias (até 3%) e não protege totalmente contra recidivas. Por outro lado, melhores modalidades de diagnóstico e tratamento reduziram a morbi-mortalidade do TCA complicado. Devido a esses novos dados, a American Society of Colon and Rectum Surgeons, em sua mais recente diretriz, recomenda que a ressecção sigmóide eletiva após a recuperação do TCA seja feita caso a caso14 e considera que o número de episódios anteriores não é um bom indicador para a seleção de candidatos à cirurgia eletiva. Os médicos devem considerar a condição médica e idade do paciente, a freqüência e gravidade do(s) ataque(s) e a presença de sintomas persistentes após o episódio agudo.14
É muito difícil prever quais casos de TCA recairão. A gravidade graduada do primeiro episódio de TCA parece ser um preditor de uma história natural adversa. O TCA do lado esquerdo, >5cm de cólon envolvido e um abscesso retroperitoneal foram preditores de recidiva e devem ser levados em consideração.97 Não há consenso sobre se a idade jovem (82 De acordo com as evidências atuais, a idade não deve ser considerada como uma indicação para cirurgia eletiva, pois não parece estar relacionada a um curso grave da doença após um TCA medicamente tratado. Mas, levando em consideração que há um aumento da incidência do TCA em pacientes mais jovens, estudos adicionais são necessários para esclarecer esta questão específica.
Casos especiais são os indivíduos imunocomprometidos. Estudos de coorte indicam que esses pacientes tinham um alto risco de TCA recorrente complicado (um risco 5 vezes maior de perfuração), e um alto risco de cirurgia de emergência.98 Portanto, um limiar mais baixo para cirurgia eletiva pode beneficiá-los.14 Mas, Biondo et al. em seu estudo recente mostram que pacientes imunocomprometidos tiveram uma taxa de mortalidade significativamente maior, mas apenas no primeiro episódio. Portanto, a controvérsia está presente.99
Tratamento de seqüelaA) Fístula
Fístula ocorre quando um flegmão diverticular ou um abscesso se rompe em um órgão adjacente. Uma fístula aparece em menos de 5% dos pacientes com DCA. As mais frequentes são as fístulas colovesicais e colovaginais. Presumivelmente, a ressecção operatória em um único estágio com fechamento da fístula e anastomose primária poderia ser realizada na maioria dos pacientes. Outras fístulas como coloentérica ou coluterina são raras.100,101
B) Obstrução
Episódios recorrentes de TCA, que podem ser subclínicos, podem produzir estressamento crônico do cólon sem inflamação contínua. Pode ocorrer uma obstrução de grau elevado ou completa. Primeiro de tratar a obstrução, é necessário excluir uma etiologia maligna. Quando a neoplasia é suficientemente excluída e não há ACD, a dilatação endoscópica ou descompressão temporária com stent metálico pode ser uma opção terapêutica.102 Mais tarde, uma ressecção subsequente em um único estágio sem desvio pode ser realizada.
Gestão da colite segmentar associada à diverticulose
É definida como uma inflamação crônica da mucosa interdiverticular de um segmento do cólon envolvida. O reto e o cólon direito são poupados. Tornou-se em um distúrbio clínico e patológico distinto e freqüentemente se apresenta com fezes ensanguentadas. A patogénese é desconhecida. O espectro das alterações histológicas varia de uma inflamação não específica leve a uma doença inflamatória intestinal como as alterações. Devido a isso, o diagnóstico diferencial é muitas vezes difícil. A maioria dos pacientes se recupera completamente em algumas semanas ou meses. Alguns deles são inicialmente tratados com 5-ASA oral, mas provavelmente esses medicamentos não são necessários porque a maioria dos casos é resolvida espontaneamente.103
Conclusões
Em UDD sintomática, os objetivos do tratamento são prevenir complicações e reduzir os sintomas. De acordo com as evidências atuais, fibra mais rifaximina cíclica ou mesalazina mais probióticos parecem ser as terapias mais eficazes. No TCA, os antibióticos parecem continuar sendo a base do tratamento e um tratamento ambulatorial é considerado a abordagem ideal na grande maioria dos pacientes com TCA sem complicações. Entretanto, o tratamento hospitalar e os antibióticos intravenosos são necessários no TCA complicado. Atualmente, o papel da cirurgia de emergência está mudando. A maioria dos abscessos associados a diverticulite pode ser tratada com antibióticos intravenosos e/ou drenagem percutânea e a cirurgia de emergência será considerada tratamento padrão apenas em pacientes com peritonite. Finalmente, a cirurgia eletiva após a recuperação do TCA deve ser feita caso a caso.
A contribuições dos autores
Gargallo CJ, Sopeña F e Lanas A contribuíram igualmente para o desenho, redação e processo de revisão deste trabalho.
Conflito de interesse
Dr. Carla J. Gargallo e Dr. Federico Sopeña não relatam conflito de interesse. Dr. Angel Lanas tem sido conselheiro da AlfaWasserman.
